QUESTIONNAIRE 87
Corrigé
Enoncé
Microanalyse
La réalisation de microanalyse (elle nécessite un échantillon de 4mg
environ) sur une substance organique permet de déterminer la teneur en carbone
et hydrogène. Cette méthode consiste en une oxydation de l'échantillon; les
atomes de carbone se retrouvent sous forme de CO2, ceux d’hydrogène sous
forme de H2O.La
combustion d’un échantillon de 4,43mgd’une substance organique a
conduit à une augmentation de 6,92mg de la masse de l’absorbeur de vapeur
d’eau (perchlorate de magnésium), et de 13,42mg pour l’absorbeur de
CO2 (soude sur amiante).
1. Quels sont les pourcentages en masse de carbone et d’hydrogène dans
la substance étudiée ?
2. La substance étudiée contient-elle un autre élément ?
Données : masses molaires atomiques en g.mol-1 :
C : 12,011 ; O : 15,999 ; H
: 1,008.
Corrigé
microanalyse
1. La transformation mise en jeu peut être modélisée par :
CxHy + (x + y/4) O2 =
xCO2
+ y/2 H2O
Masses molaires moléculaires en g.mol-1 :
CO2 : 12,011+ (2*15,999)= 44,009
H2O : (2*1,008) + 15,999=
18,015
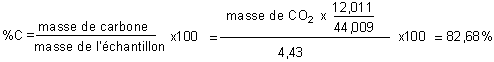
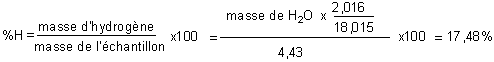
2. La somme des pourcentages en C et H donne :
82,68+17,48=100,16% donc la substance étudiée ne contient pas d’autres
éléments.