EXERCICE
160
L'analyse
organique d'un composé (A) CxHyOz a donné les
résultats suivants (composition massique) :
% de
carbone : 64,86
%
d'hydrogène : 13,51
Densité
de vapeur par rapport à l'air : 2,55
1-1)
Déterminer la formule moléculaire de (A).
1-2) Le
spectre I.R. de (A) est le suivant :
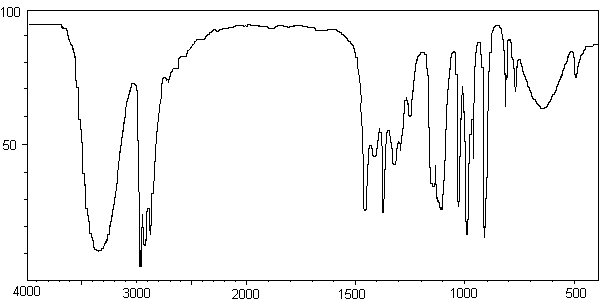
1-2-1) Pouvez-vous à partir de ce
spectre, identifier la fonction présente dans la molécule de (A) ?
1-2-2) Ecrire les quatre formules
développées possibles pour (A) et donner les noms des isomères correspondants.
1-3)
Sachant que la molécule de (A) présente un centre de chiralité,
1-3-1) Donner sa formule
semi-développée.
1-3-2) Représenter en représentation
de Cram les deux énantiomères en précisant pour chacun, la configuration
absolue R ou S. Justifier la réponse.
1-4) Le
composé (A) est oxydé par le mélange sulfochromique en un produit (B).
1-4-1) Ce composé (B) donne un
précipité avec la 2,4-DNPH ainsi qu'avec le diiode en milieu alcalin. Comment
ces réactions permettent-elles d'obtenir la structure de (B) ? Nommer (B).
1-4-2) Ecrire l'équation chimique de
la réaction d'oxydation de (A) en (B).
1-5) Le
spectre I.R. de (B) est le suivant :
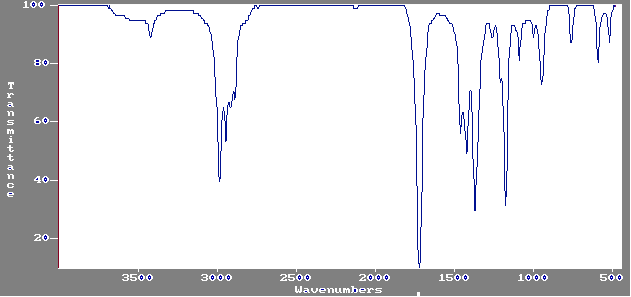
Permet-il
de confirmer la structure de (B) ?
1-6) Ce
produit (B) réagit mole à mole avec le benzaldéhyde en milieu basique à chaud.
On obtient deux produits (C) et (C') de même formule brute C11H12O.
1-6-1) Comment appelle-t-on les deux
réactions successives qui conduisent à la synthèse de (C) et de (C') ?
1-6-2) Donner la formule
semi-développée de (C) et celle de (C').
1-7) Le
produit (B) est traité par du bromure d'éthylmagnésium dans l'éther anhydre. On
obtient un produit (D), qui est ensuite hydrolysé pour donner un produit (E).
Ecrire les équations chimiques correspondantes ; donner la formule
semi-développée de (E).
Données :
Masses
molaires atomiques en g.mol-1 : M(O)
= 16,0 M(C) = 12,0 M(H) = 1,0 .
Formule
du benzaldéhyde :
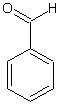
On
rappelle la relation donnant la masse molaire d'un gaz : M = 29 d.