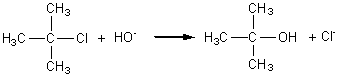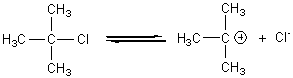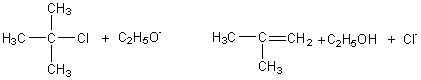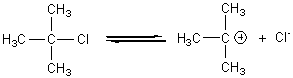BASICITE
ET NUCLEOPHILIE
RETOUR
AU SOMMAIRE
1) Définitions
:
1-1) Basicité :
C'est l'aptitude d'une molécule
ou d'un ion à fixer un proton selon l'équation : B
+ H+ = BH+ .
B est la base et BH+
son acide conjugué.
La basicité
est une notion liée à la thermodynamique ;
pour comparer les bases entr' elles, on utilise en effet la constante d'acidité
du couple BH+/B qui correspond à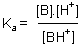
ou
bien on utilise une fonction dérivée, le pKa (pKa = -log(Ka)).
Plus le pKa d'un couple est petit, plus la base du couple est faible.
1-2) Nucléophilie :
La
nucléophilie est une propriété liée à
la présence, sur un atome d'une molécule ou d'un ion, d'une
paire d'électrons libre. Une espèce nucléophile est
attirée par les atomes de carbone de substrats ayant une faible
densité électronique (C+d
ou carbocation C+).
Pour
comparer les propriétés nucléophiles de deux
réactifs, on fait appel à des considérations cinétiques
; on compare en effet les constantes de vitesse k, des réactions
de ces deux réactifs dans un même solvant vis à vis
d'un même substrat ; celui ayant la plus grande constante de vitesse
est le plus nucléophile.
2)
Influence
de la basicité ou de la nucléophilie d'un réactif
sur l'évolution d'une réaction :
Une
espèce nucléophile est aussi une espèce basique, il
y a donc parfois compétition entre ces deux caractères et
l'issue d'une réaction dépend de celui de ces deux caractères
qui est prédominant.
Exemple
1
Hydrolyse
du 2-chloro-2-méthylpropane en milieu basique dilué :
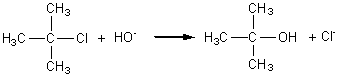
Le mécanisme est
le suivant (SN1 : Substitution nucléophile monomoléculaire)
:
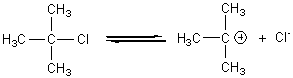
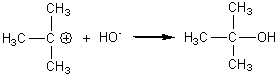
Le caractère nucléophile
de HO- l'emporte sur son caractère basique.
Exemple
2
Déshydrohalogénation
du 2-chloro-2-méthylpropane en présence d'éthanolate
de sodium à 550°C
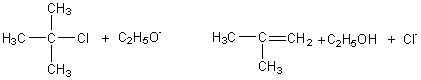
Il s'agit d'une élimination
monomoléculaire E1.
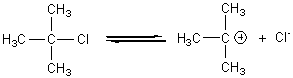
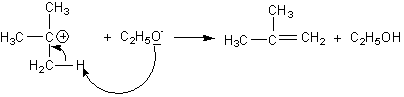
Le caractère basique
de C2H5O- l'emporte sur son caractère
nucléophile.