POINT DE FUSION
contrôle de la pureté des solides par la mesure de leur point de fusion
1) Etude théorique:
- La détermination du point de fusion d’un produit cristallisé permet de contrôler sa pureté ou de l’identifier.
- Le point de fusion d’un produit
contenant des impuretés est inférieur à celui du produit pur. Cet abaissement
du point de fusion est
proportionnel à la quantité d’impuretés présentes dans le mélange.
- Cette propriété est mise à profit pour évaluer la pureté des produits chimiques dont la température de fusion n’est pas trop élevée.
2) Détermination expérimentale d’un point de fusion:
2-1) Remarques:
- Avant toute mesure il faut être sûr que le composé est bien sec.
- Il se produit parfois des associations stables entre les molécules de solvant et les molécules de soluté. Les composés ainsi formés ont des températures de fusion différentes de celles du soluté seul.
Exemple : (C6H5)3CH
Pf = 92°C (C6H5)3CH
+ C6H6 Pf = 76°C
Il est donc nécessaire de détruire ces associations. Cela est possible en chauffant le composé à une température supérieure au point d’ébullition du solvant.
- Certaines substances fondent à
des températures différentes selon la structure de leurs cristaux. Le point de
fusion permet de connaître la variété allotropique du composé isolé.
Chaque variété allotropique correspond à un mode de cristallisation
différent qui donne au corps des propriétés physiques différentes.
2-2) Matériel :
- Il existe une grande variété d’appareils que l' on
peut regrouper en deux catégories, selon la méthode employée :
méthodes par tubes capillaires ou méthodes par plaques
chauffantes.
Appareils à tube capillaire :
- Appareils à bain d’huile : tube
de THIELE ; appareils électriques à bain d’huile.
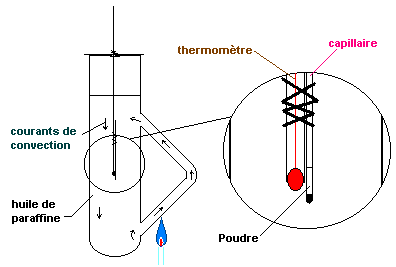
A l'aide de la flamme d'un bec
Bunsen, on porte l'huile à une température inférieure d'environ 30°C à la
température de fusion
de la poudre. Puis à l'aide de la
veilleuse on fait monter la température de l'huile d'environ 1°C toutes les 15
secondes. Au
moment précis où la poudre fond (on
voit le contenu du capillaire devenir transparent), on lit la température sur
la graduation
du thermomètre.
La précision du résultat obtenu (si
l'on a fait monter la température assez lentement) dépend du thermomètre; on
peut obtenir
le dixième de degré.
- Appareils électriques à bloc métallique.
Appareils à plaque chauffante :
- A lamelles.
- A gradient de température : banc de KOFLER.
- A fusion instantanée : bloc MAQUENNE.
- Au laboratoire de chimie on utilise principalement, pour des échantillons monocristallins et dans la gamme des températures de 50 à 250°C, le banc de Kofler.
2-3) Utilisation du banc de Kofler:
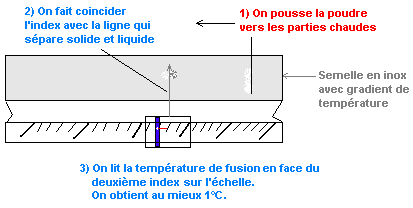
La semelle en "inox" de la plaque chauffante présente un gradient de
température allant de 50 à 250°C. Ceci permet donc, en déposant quelques
cristaux de solide dans la zone des basses températures et en les déplaçant
tout au long de la plaque vers les températures plus élevées, de repérer une
ligne de démarcation très nette entre la phase solide (cristaux non fondus) et
la phase liquide (cristaux fondus). En plaçant l'index d'un curseur sur la
ligne de séparation on peut lire la température indiquée par un deuxième index
sur une échelle.
Cette température est approximative il faut étalonner l’appareil en utilisant deux substances témoins dont les points de fusion encadrent le plus près possible la température de fusion de l’échantillon. On règle alors l’index à la température de l'une des substances étalon, on vérifie avec la seconde que l'indication est correcte (en cas de divergence, régler l'index avec la substance étalon dont la température de fusion est la plus voisine de celle du corps étudié). On reprend le composé et on détermine alors son point de fusion avec plus de précision.
Après chaque utilisation on nettoie la surface de la plaque chauffante avec du coton imprégné d’alcool en entraînant les restes solides vers les températures les plus élevées (se placer de préférence sous une hotte aspirante pour ne pas respirer les vapeurs qui s'échappent).