EXERCICE 144
Organomagnésien en synthèse organique :
Cet exercice a pour but d'étudier la préparation d'un
alcool par l'addition nucléophile d'un organomagnésien sur un aldéhyde suivie
d'une hydrolyse. La préparation de l'organomagnésien sera aussi abordée.
1) Etude du composé de départ :
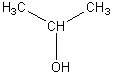
1-1) A quelle famille chimique appartient le composé (A) dont la formule
semi-développée est donnée ci-dessous ?
1-2)
Nommer le composé (A).
1-3) Les
pictogrammes suivants sont présents sur le flacon contenant (A). Préciser leur
signification :
 F
F XI
XI
1-4) Quelles précautions faut-il
prendre lors de l'utilisation de ce produit ?
1-5) Le propan-1-ol, noté (A'° est un isomère de (A).
1-5-1) Définir le terme "isomère".
1-5-2) Qu'obtient-on par oxydation de (A), de (A') par les ions permanganate en
milieu acide par exemple ? On donnera les formules semi-développées et les noms
des molécules obtenues.
2) Préparation d'un dérivé halogéné :
On fait réagir une solution aqueuse d'acide chlorhydrique sur le composé (A).
On obtient un composé (B) de formule moléculaire C3H7Cl.
2-1)
2-1-1) Ecrire l'équation de cette réaction.
2-1-2) Choisir parmi les termes suivants, ceux qui s'appliquent à cette
réaction : addition - réduction - élimination - substitution - radicalaire -
électrophile - oxydation - nucléophile.
2-2) Nommer le composé B obtenu.
3) Préparation d'un organomagnésien :
On introduit 4,00 g de (B) dans 40 mL d'éther diéthylique (ou éthoxyéthane). On
verse cette solution goutte à goutte sur 2,00 g de magnésium (sous forme de
tournure) dans de l'éther. Le montage est représenté ci-dessous.
3-1-1) Donner un nom aux 5 pièces de montage
numérotées de 1 à 5 dans le schéma ci-dessus.
3-1-2) Expliquer pourquoi l'éther,ainsi
que les réactifs doivent être anhydres.
3-1-3) Donner une méthode permettant de rendre l'éther anhydre.
3-1-4) Quel est le rôle de la garde à CaCl2 ?
3-2) Questions
sur la réaction :
3-2-1) Ecrire l'équation de la réaction de formation de l'organomagnésien.
3-2-2) Nommer l'organomagnésien (C) obtenu.
3-2-3) Calculer les quantités de matière de chacun des réactifs.
Données : Masses molaires atomiques en g.mol-1
: C : 12,0 H : 1,0 Cl :
35,5 Mg : 24,3
3-2-4) Vérifier qu'on utilise un excès de magnésium.
3-2-5) Utiliser un excès de magnésium et ajouter le dérivé halogéné
progressivement permet d'éviter une réaction parasite. Laquelle ? Ecrire son
équation bilan .
4) Préparation d'un alcool.
L'organomagnésien (C) réagit par addition nucléophile
avec le butanal pour donner, après hydrolyse,
l'alcool (D), dont la formule semi-développée est donnée ci-dessous :
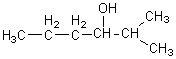
4-1)
Nommer l'alcool (D). A quelle classe appartient-il ?
4-2)
Ecrire l'équation des deux réactions permettant le passage de (C) à (D). Quel
est l'intérêt majeur de ce type de réaction en chimie organique ?
4-3)
L'alcool (D) est purifié par rectification (ou distillation fractionnée). Faire
le schéma annoté du montage à utiliser.