EXERCICE 172
Détermination de la structure d’un composé
aromatique
Données :
|
Élément |
H |
C |
O |
|
Numéro atomique |
1 |
6 |
8 |
|
Masse molaire (g.mol-1) |
1,0 |
12,0 |
16,0 |
On
cherche à déterminer la structure d’un composé J, additif de certaines huiles dont il augmente la viscosité.
Dans
un premier temps J est hydrolysé
en milieu basique. Après acidification du milieu réactionnel, un solide K cristallise et un composé liquide L est isolé. On analyse successivement
K et L pour déterminer la structure de J.
1) Détermination de la structure de K.
On
donne la formule brute de K : C7H6O2
ainsi que son spectre IR (ci-dessous) ; on précise également :
- qu’une solution aqueuse de K a un pH inférieur à 7,
- que K
est aromatique.
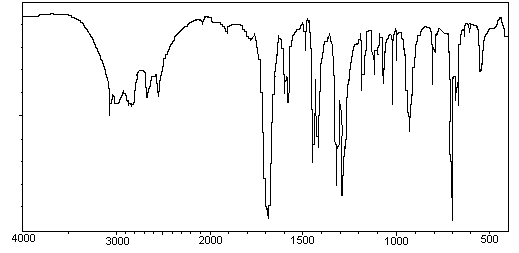
1-1) Identifier grâce au
tableau fourni en annexe les bandes qui
caractérisent le groupement fonctionnel présent dans K.
1-2) Donner la formule semi-développée
de K.
2) Détermination de la structure de L.
2-1) L de masse molaire ML
= 74,0 g.mol-1 est composé de 64,9 %
d’élément carbone et 13,5 % d’élément hydrogène, en masse.Déterminer
la formule brute de L, CxHyOz.
2-2) L est oxydé en un
composé M par le permanganate de
potassium en milieu sulfurique. La masse molaire de M est de 72,0 g.mol-1. On
réalise sur M successivement les
tests suivants :
- Test 1 : la
2,4-DNPH (2,4-dinitrophénylhydrazine) donne avec M un précipité orangé.
- Test 2 : le test du
miroir d’argent (réactif de Tollens) est négatif.
- Test 3 : en versant
M dans une solution de diiode en milieu basique, il apparaît un précipité jaune
pâle.
2-2-1) Indiquer les
renseignements fournis par chacun de ces tests.
2-2-2) En déduire la
formule semi-développée de M et
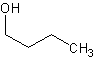
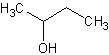
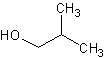
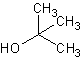
choisir, parmi les quatre formules ci-dessous, celle qui correspond à L.
|
|
|
|
|
2-2-3) Donner
l’équation de la réaction correspondant au test 3.
2-3) L existe sous la forme
de deux énantiomères.
2-3-1) Dessiner en
représentation de Cram un des deux énantiomères.
2-3-2) Indiquer la
configuration absolue de l’atome de carbone asymétrique dans la molécule
représentée : justifier la réponse en expliquant la démarche suivie.
3) Structure de J.
3-1) On peut synthétiser J en faisant réagir K avec L en milieu acide et en chauffant.
3-1-1) Écrire
l’équation de la réaction en donnant la formule semi-développée de J.
3-1-2) Donner les
caractéristiques cinétiques et thermodynamiques de cette transformation.
3-2) J peut être également
obtenu en faisant réagir L sur
le chlorure de benzoyle.
3-2-1) Écrire
l’équation de cette réaction.
3-2-2) Indiquer
l’intérêt de cette méthode de synthèse par rapport à celle proposée en 3-1)