EXERCICE 173
Des hydrocarbures particuliers : les terpènes
Les
terpènes sont des composés organiques naturels, très volatils contenant
habituellement dix, quinze ou vingt atomes de carbone. Ils sont biosynthétisés suite au couplage d'au moins deux entités
moléculaires à cinq atomes de carbone. La structure de ces entités ressemble à
celle du 2-méthylbuta-1,3-diène (isoprène).
Les
terpènes sont utilisés dans l'industrie des parfums (essence de lavande, rose),
comme insecticides (acide chrysanthémique), comme
condiments (extrait de clous de girofle) ou encore comme solvants (la térébenthine).
Partie 1
Un terpène dans le caoutchouc
Le
caoutchouc naturel produit par l'Hévéa est un polymère de l'isoprène (ou 2-méthylbuta-1,3-diène), appelé polyisoprène
et de formule :
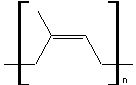
1-1) Représenter la formule semi-développée du
monomère du polyisoprène.
1-2) Écrire la formule semi-développée du motif de
ce polymère.
1-3) Préciser la configuration des doubles
liaisons de ce polymère.
1-4) Expliquer ce que l'on appelle vulcanisation
du caoutchouc.
Partie 2
Les terpènes dans les huiles essentielles
Les parties 2-1) et 2-2) sont totalement
indépendantes.
2-1) Détermination de la structure d'un terpène issu
de l'huile essentielle de lavande. On peut isoler de l'essence de lavande un
composé appelé á-terpinéol de formule brute C10H18O, que
l'on notera A. Dans le but de
déterminer sa structure, on réalise un certain nombre de caractérisations :
a)
l' α-terpinéol A décolore
une solution organique de dibrome.
b)
Lorsque l'on effectue son hydrogénation catalytique (action du dihydrogène en
présence de nickel), A conduit
au composé B de formule C10H20O.
c)
Le spectre IR de A présente,
entre autres, une bande vers 3200-3500 cm-1.
d)
B est déshydraté en milieu acide
pour conduire majoritairement au composé C (C10H18) et au composé minoritaire D (isomère de C).
e)
L'ozonolyse du composé C conduit
à 2 composés E et F. E est la 4-méthylcyclohexanone et F donne un test positif à la 2,4-dinitrophénylhydrazine (DNPH) et négatif au réactif de Tollens.
2-1-1) Quelle(s)
information(s) donnent les tests a) et b) ?
2-1-2) Quelle information
donne le spectre IR ? Justifier.
2-1-3) Donner la formule
semi-développée de F et écrire
l'équation du test à la DNPH.
2-1-4) Donner la formule
semi-développée de C.
2-1-5) Sachant que C est obtenu par déshydratation de B, en déduire les deux formules
possibles pour B.
2-1-6) Pour choisir la bonne
formule pour B, on a enregistré
son spectre RMN du 1H. Celui-ci présente, entre autres, les signaux
suivants :
|
Déplacement
chimique (ppm) |
Multiplicité
du signal |
Nombre
de protons attribués au signal |
|
0,95 |
doublet |
3
H |
|
1,15 |
singulet |
6
H |
Identifier
la formule semi-développée de B en
justifiant et attribuer les signaux aux protons correspondants.
2-1-7) Donner la formule
semi-développée de l'isomère D de
C obtenu au cours de la déshydratation
de B. Expliquer pourquoi C est le composé majoritaire.
2-1-8) L'ozonolyse de A suivie d'une hydrolyse en milieu
réducteur conduit à la formation d'un composé unique G possédant un groupe acétyle (CH3-CO-). En déduire la
formule semi-développée de A.
2-2) Synthèse d'un terpène issu de l'huile
essentielle d'une plante aromatique. Dans cette partie, on propose une voie de
synthèse d'un terpène, l'α-curcumène, contenu
dans l'huile essentielle de l'Immortelle. L'Immortelle est une plante aromatique
présente dans le bassin méditerranéen. Cette synthèse est proposée à partir du
4-aminotoluène, noté H, dont la formule est :
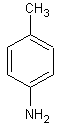
a)
H est traité à 0 °C par une
solution aqueuse de nitrite de sodium en présence d'acide sulfurique, ce qui conduit
à la formation du composé I. On
ajoute alors au composé I du
cyanure de cuivre (I) en présence d'un excès de cyanure de potassium pour
obtenir après chauffage à 50 °C le composé J.
b)
J est hydraté et hydrolysé en
milieu acide pour conduire à K ;
le spectre IR de K présente
notamment une bande large vers 2500-3100 cm-1 et une bande plus
étroite vers 1680 cm-1.
c)
K est porté à reflux avec un
excès d'éthanol en présence de traces d'acide fort pour conduire à L.
d)
L est traité en milieu anhydre
par deux équivalents de bromure de méthylmagnésium
pour conduire après hydrolyse légèrement acide au composé M.
e)
M est déshydraté par chauffage
en milieu acide ; on obtient N,
de formule brute C10H12 ;
f)
la réaction de N avec le bromure
d'hydrogène (HBr) en présence de peroxyde de benzoyle
donne O.
g)
O réagit dans l'éther diéthylique anhydre avec du magnésium pour donner P. P réagit avec l'oxyde d'éthylène (ou époxyéthane)
; on obtient Q après hydrolyse
en milieu acide.
h)
La réaction de Q avec le
trioxyde de chrome dans la pyridine donne R de formule brute C12H16O.
i)
R conduit après réaction avec un
réactif approprié à l'α-curcumène de formule :
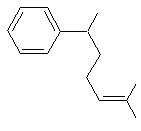
2-2-1) Donner les formules
semi-développées des composés I à
R.
2-2-2) Interpréter les
données spectroscopiques relative à K.
2-2-3) Pourquoi utilise-t-on
un large excès d'éthanol lors de l'étape K _ L ?
2-2-4) Justifier la régiosélectivité de la réaction f), dont le mécanisme sera
détaillé.
2-2-5) Justifier le choix de
l'éther diéthylique anhydre comme solvant au cours de
la réaction g).
2-2-6) A propos de l'étape
i) :
2-2-6-1) Donner
la formule semi-développée du réactif nécessaire pour transformer R en á-curcumène
en une seule étape.
2-2-6-2) Proposer
une synthèse de ce réactif à partir du 2-bromopropane.
2-2-6-3) Combien
de stéréoisomères présente l'á-curcumène
? Justifier.
2-2-6-4) L'
α-curcumène isolé de la plante Immortelle est
appelé (-)-α-curcumène. Que signifie la notation
(-) ?