EXERCICE 41
Corrigé
Enoncé:
1) En
présence de chlorure d'aluminium anhydre le chlorure d'acétyle (ou chlorure d'éthanoyle) réagit sur le benzène. Il se forme A.
a) Ecrire l'équation bilan de
la réaction.
b) Donner le nom de A.
c) Quel est le mécanisme de la
réaction ?
2) Le composé A subit une chloration en présence
de FeCl3. On obtient essentiellement un dérivé B substitué en
position 3 (méta) par rapport au premier substituant .
a) Ecrire l'équation bilan de
la réaction.
b) Quel en est le mécanisme ?
Justifier l'orientation de cette réaction.
Corrigé:
1)
a) Il s'agit d'une substitution électrophile du type Friedel et Crafts. Cette substitution est une acylation par un
chlorure d'acyle.
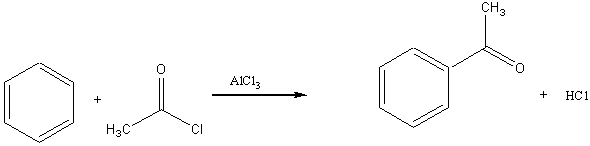
b) Le nom du composé A obtenu est : méthyl phényl cétone.
c) Les différentes étapes du mécanisme de la réaction peuvent se résumer à :
- Formation de l'ion acylium R-C(+)=O par réaction
entre le chlorure d'acyle et chlorure d'aluminium.
- L'ion acylium formé donne une substitution
électrophile sur le noyau benzénique.
2)
Il s'agit d'une deuxième substitution électrophile sur le noyau benzénique.
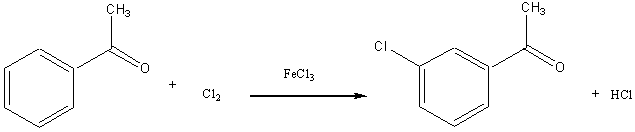
Le mécanisme de cette deuxième substitution est étroitement lié à la présence
et à la nature du premier substituant.
Les règles d'Hollemann donnent la solution de
l'orientation de cette deuxième substitution.
Le groupement "cétone" lié lors de la première substitution attirant
les électrons appauvrit le noyau aromatique et défavorise
une deuxième substitution électrophile ; les positions les moins défavorisées
sont les positions méta.