SPECTROSCOPIE INFRAROUGE

Table des nombres d'onde des vibrations de valence et de déformation.
|
Liaison |
Nature |
Nombre d'onde(cm-1) |
Intensité |
|
O-H alcool libre |
Valence |
3580-3670 |
F; large |
|
Csp-H |
Valence |
3300-3310 |
m |
|
O-H alcool lié |
Valence |
3200-3400 |
F |
|
N-H (amines+imines) |
Valence |
3100-3500 |
m |
|
N-H (amides) |
Valence |
3100-3500 |
F |
|
Csp2-H |
Valence |
3000-3100 |
m |
|
Csp2-H aromatique |
Valence |
3030-3080 |
m |
|
Csp3-H |
Valence |
2800-3000 |
F |
|
Csp2-H aldéhyde |
Valence |
2750-2900 |
m |
|
O-H acide carboxylique |
Valence |
2500-3200 |
F à m; large |
|
C=C |
Valence |
2100-2250 |
f |
|
C=N |
Valence |
2120-2160 |
F ou m |
|
C=O anhydride |
Valence |
1700-1840 |
F; 2 bandes |
|
C=O chlorure d'acyle |
Valence |
1770-1820 |
F |
|
C=O ester |
Valence |
1700-1740 |
F |
|
C=O aldéhyde et cétone |
Valence |
1650-1730 |
F |
|
C=O acide |
Valence |
1680-1710 |
F |
|
C=O amide |
Valence |
1650-1700 |
F |
|
C=C |
Valence |
1625-1685 |
m |
|
C=C aromatique |
Valence |
1450-1600 |
variable;3 ou 4 bandes |
|
N=O |
Valence |
1510-1580 |
F; 2 bandes |
|
C=N |
Valence |
1600-1680 |
F |
|
N-H amine ou amide |
Déformation |
1560-1640 |
F ou m |
|
Csp3-H |
Déformation |
1415-1470 |
F |
|
Csp3-H(CH3) |
Déformation |
1365-1385 |
F;2 bandes |
|
P=O |
Valence |
1250_1310 |
F |
|
C-O |
Valence |
1050-1450 |
F |
|
C-N |
Valence |
1020-1220 |
m |
|
C-C |
Valence |
1000-1250 |
F |
|
C-F |
Valence |
1000-1040 |
F |
|
Csp2-H de-CH=CH- |
Déformation |
950-1000 |
F |
|
Csp2-H aromatique |
Déformation |
730-770 et 690-770 |
F ;2 bandes |
|
Csp2-H aromatique |
Déformation |
735-770 |
F |
|
Csp2-H aromatique |
Déformation |
770-800 et 685-720 |
F et m; 2 bandes |
|
C-Cl |
Valence |
700-800 |
F |
|
C-Br
|
Valence
|
600-750
|
F
|
Les différentes
Vibrations d'une molécule triatomique:
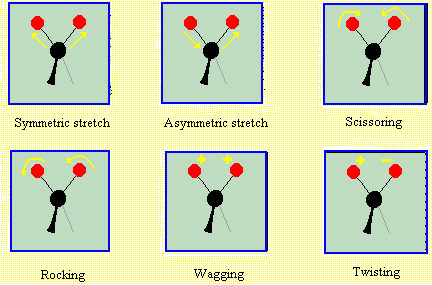
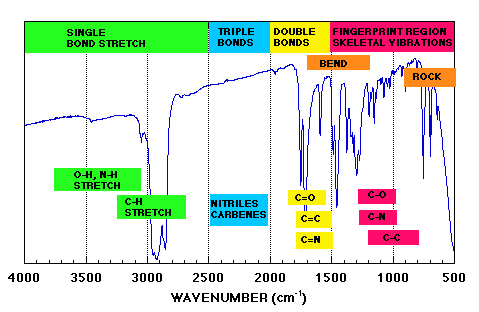
Les principales régions d'un spectre IR:
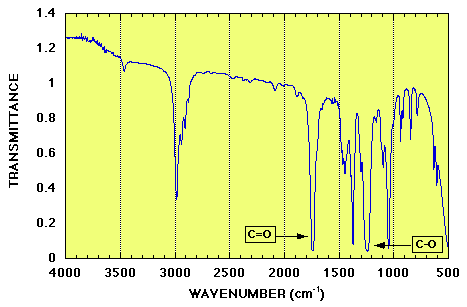 Spectre de l'acétate d'éthyle
Spectre de l'acétate d'éthyle
|
Acide
hexanoïque (comparaison avec l'hexane sans nom ni commentaire) |
Acide
hexanoïque (comparaison avec l'hexane avec noms; sans commentaire) |
Acide
hexanoïque (comparaison avec l'hexane avec noms et commentaires) |
||||||
|
Anhydride
butanoïque (comparaison avec l'acide sans nom ni commentaire) |
Anhydride
butanoïque (comparaison avec l'acide avec nom; sans commentaire) |
Anhydride
butanoïque (comparaison avec l'acide avec noms et commentaires) |
Aniline
(spectre commenté) |
|||||
|
Dibenzylidène acétone (cinnamon) |
||||||||
|
Hexène
(comparaison avec l'hexane; sans nom, ni commentaire) |
Hexène
(comparaison avec l'hexane; avec noms) |
Hexène
(comparaison avec l'hexane; avec noms et commentaires) |
||||||
|
Propionamide (commenté) |
2-méthylbut-2-ène |
|||||||
|
|
|
|
|
|
|
|
|