LA
VOIE DE L'ACIDE SHIKIMIQUE
Jacques BARON
avec la collaboration de
Gérard GOMEZ
Plan de l'étude
1) Biosynthèse des
acides aminés aromatiques
3) Du chorismate à
la phénylalanine et à la tyrosine
3-1)
De l'acide préphénique à la phénylalanine
3-2)
De l'acide préphénique à la tyrosine
4) Du
chorismate au tryptophane
4-1)
Du chorismate à l'anthranilate
4-2)
De l'anthranilate au N-phosphoribosyl anthranilate
4-3)
Du N-phosphoribosyl anthranilate à l'énol-1-carboxyphénylamino-1'-
déoxyribulose-5-phosphate
4-4)
De l'énol-1-carboxyphénylamino-1'-
déoxyribulose-5-phosphate à l'indol-3-glycérol phosphate
4-5)
De l'indol-3-glycérol phosphate au tryptophane
Annexe 1 Glycolyse
Annexe 2 Du
glucose à l'érythrose-4-phosphate
Annexe 3 Vers
l'acide gallique
Annexe 4 Vers
l'acide quinique
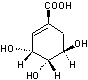
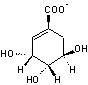
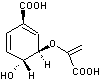
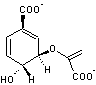
L'acide shikimique et sa base
conjuguée (shikimate) ont pour formules
|
|
|
|
Acide shikimique |
Shikimate |
La voie de
biosynthèse de l'acide shikimique à partir du glucose est une voie du monde
végétal qui conduit à certains acides aminés et, juste en amont, à l'acide
quinique (quinquina) (Voir annexe 4) et à l'acide gallique (galles de chêne) (Voir annexe
3).
Le schéma
général de ces transformations est le suivant
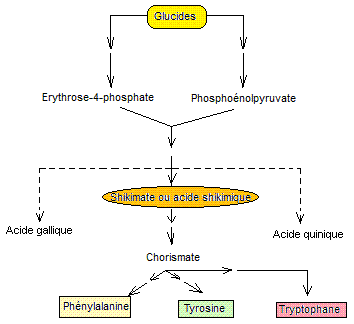
1) Biosynthèse
des acides aminés aromatiques
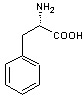
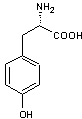
Nous nous proposons de décrire en
détail la voie de l'acide shikimique dans la synthèse de trois acides aminés
aromatiques, la phénylalanine, la tyrosine et le tryptophane,
|
|
|
|
|
Phénylalanine |
Tyrosine |
Tryptophane |
Leur biosynthèse emprunte la voie de
l'acide shikimique (ou du shikimate, sa base conjuguée) qui conduit à l'acide
chorismique (ou au chorismate, sa base conjuguée).
|
|
|
|
Acide
chorismique |
Chorismate |
Le point de départ de la biosynthèse
de ces acides aminés aromatiques est la condensation du phosphoénolpyruvate
(PEP) (voir annexe 1) et de l'érythrose-4-phosphate
(voir annexe 2) qui aboutit au 2-céto-3-désoxy-D-arabino-heptulosonate-7-phosphate
(ou DAHP) un composé en C7 qui se cyclise ; deux étapes
supplémentaires conduisent au shikimate ; trois autres étapes et l'on obtient
le chorismate.
Le détail est le suivant :

Considérations sur la nomenclature
concernant le DAHP.
* Le nom du DAHP montre que c'est un
dérivé de l'heptulose, c'est-à-dire un heptose à fonction cétone. Il n'existe
pas de noms pour désigner tous les stéréo-isomères des oses à plus de 6
carbones.
Le préfixe "arabino"
sert à préciser la structure de cet heptose au niveau des centres chiraux.
* S'agissant d'acide heptulosonique,
il faut savoir qu'on désigne aujourd'hui par "acide ulosonique" un
acide dérivé d'un monosaccharide cétonique dans lequel le groupe hydroxyle en C1
a été oxydé en acide carboxylique. Comme en pratique le groupe cétonique est en
C2 la formule générale d'un acide ulosonique est CH2OH -
(CHOH)n – CO - COOH
Remarque 2 :
Les étapes 2a, 2b,2c constituent
l'étape 2 de passage du DAHP au 3-déshydroquinate.
Toutes les réactions (étapes 1 à 7)
nécessitent des enzymes
|
Réaction -1- |
DAHP synthase |
|
Réactions -2- |
3-déshydroquinate synthase (DHQ
synthase) |
|
Réaction -3- |
3-déshydroquinate déshydratase
(DHQ déshydratase) |
|
Réaction -4- |
Shikimate déshydrogénase |
|
Réaction -5- |
Shikimate kinase |
|
Réaction -6- |
5-énolpyruvylshikimate-3-phosphate
synthase |
|
Réaction -7- |
Chorismate synthase |
3) Du chorismate à la
phénylalanine et à la tyrosine
Le chorismate est d'abord transformé
en préphénate par réarrangement de Claisen sous l'action du chorismate mutase
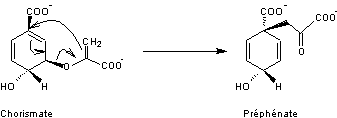
3-1) De l'acide préphénique à la phénylalanine
Deux étapes sont nécessaires enfin
pour passer de l'acide préphénique (acide conjugué du préphénate) à la
phénylalanine
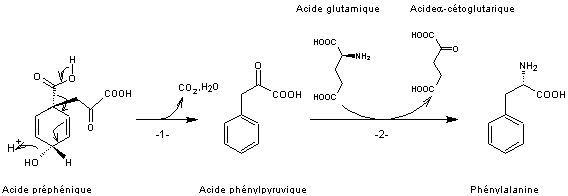
Réaction -1- L'acide préphénique subit une décarboxylation oxydative
avec élimination du groupe hydroxyle sous forme d'eau pour donner de l'acide
phénylpyruvique
Réaction -2- L'acide phénylpyruvique subit une transamination par
l'acide glutamique et un enzyme aminotransférase pour donner la phénylalanine ;
l'acide glutamique est transformé en acide α-cétoglutarique.
3-2) De l'acide préphénique à la tyrosine
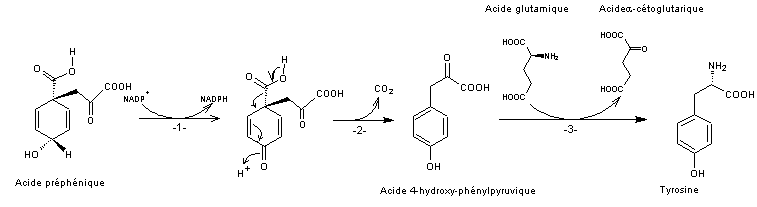
Réaction -1- L'acide préphénique subit une oxydation par le couple
NADP+/NADPH (-OH en 4 est transformé en =O) et l'enzyme
déshydrogénase.
Réaction -2- Une décarboxylation conduit à l'acide
4-hydroxy-phénylpyruvique.
Réaction -3- L'acide 4-hydroxy-phénylpyruvique subit une
transamination par l'acide glutamique et un enzyme transaminase pour donner la
Tyrosine ; l'acide glutamique est transformé en acide α-cétoglutarique.
4) Du chorismate au tryptophane
Le passage du chorismate au
tryptophane se déroule en plusieurs étapes résumées puis détaillées ci-après

*Signification de quelques
abréviations
- PRPP : Phosphoribosylpyrophosphate
-
PPi : Pyrophosphate inorganique
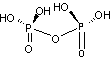
-
GAP : Glycéraldéhyde-3-phosphate
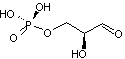
* Les enzymes nécessaires à ces
réactions
|
Réaction -1- |
Anthranilate synthase |
|
Réaction -2- |
Phosphoribosyl anthranilate
transférase |
|
Réaction -3- |
Phosphoribosyl anthranilate
isomérase |
|
Réaction -4- |
Indol-3-glycérol phosphate
synthase |
|
Réaction -5- |
Tryptophane synthase |
4-1) Du chorismate à l'anthranilate (étape 1)
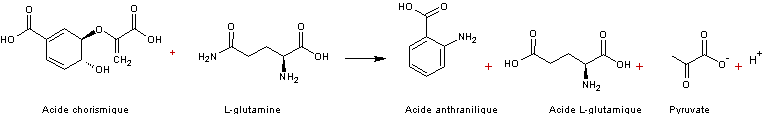
Le mécanisme correspondant à cette
première étape et qui fait intervenir l'anthranilate synthase, comporte 6
paliers.
On en donne ci-dessous deux qui
correspondent à la formation de l'acide anthranilique et du pyruvate
-
il y a eu antérieurement formation d'ammoniac
à partir de la L-glutamine
L'ammoniac agit en tant que
nucléophile se fixant sur l'acide chorismique ; il y a déplacement de liaisons
et élimination d'eau à partir de l'hydroxyle de l'acide chorismique et d'un
hydrogène de l'ammoniac.
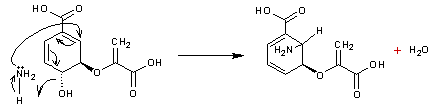
-
L'intermédiaire formé se dissocie en acide anthranilique et en acide pyruvique
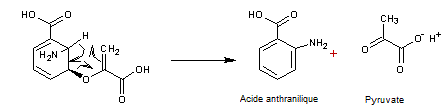
4-2) De l'anthranilate au N-phosphoribosyl anthranilate (étape
2)

4-3) Du N-phosphoribosyl anthranilate à l'énol-1-carboxyphénylamino-1'-
déoxyribulose-5-phosphate (étape 3)
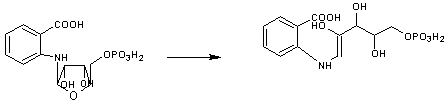
4-4) De l'énol-1-carboxyphénylamino-1'-
déoxyribulose-5-phosphate à l'indol-3-glycérol phosphate (étape 4)
Il s'agit d'une décarboxylation
suivie de la formation du noyau indole par cyclisation
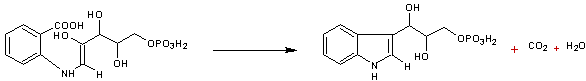
4-5) De l'indol-3-glycérol phosphate au tryptophane (étape
5)
L'enzyme catalysant cette réaction
se décompose en deux sous-unités :
- Le
tryptophane synthase (sous-unité α) catalyse une rupture aldolique de
l'indol-3-glycérol phosphate pour donner l'indole et le
glycéraldéhyde-3-phosphate
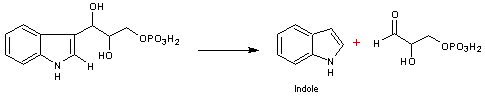
- Le
tryptophane synthase (sous-unité β) catalyse la réaction finale qui fait
intervenir la sérine, le coenzyme PLP (Phosphate de pyridoxal) avec formation
du tryptophane et élimination d'eau.

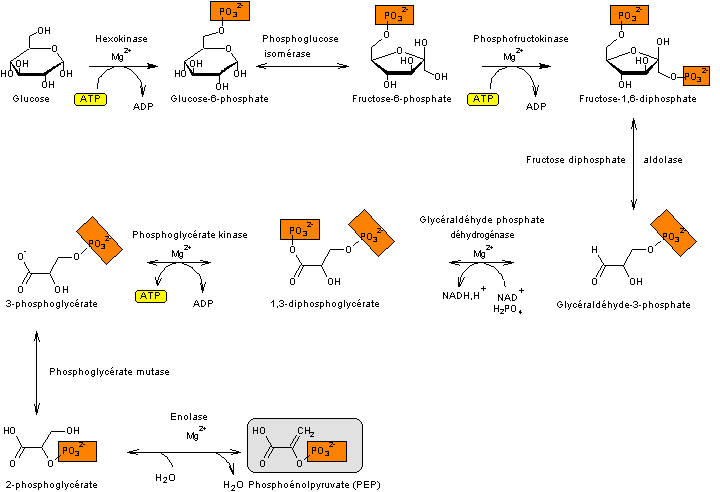
Annexe 1
Glycolyse
Du glucose au PEP
(Phosphoénolpyruvate)
Du glucose à l'érythrose-4-phosphate
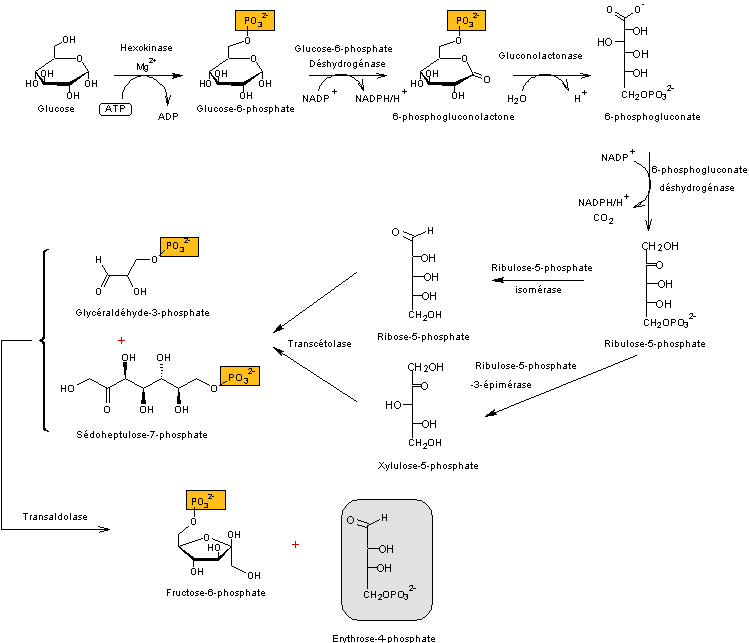
Remarque : Les transformations qui s'opèrent entre pentoses, comme
par exemple le ribulose et le xylulose, pour donner un nouveau couple d'oses
sont connues sous le nom de "transformations des pentoses".
Vers l'acide gallique

|
Réaction -1- |
DAHP synthase |
|
Réactions -2- |
3-déshydroquinate synthase (DHQ
synthase) |
|
Réaction -3- |
3-déshydroquinate déshydratase
(DHQ déshydratase) |
|
Réaction -4- |
Shikimate déshydrogénase |
Vers l'acide quinique

|
Réaction -1- |
DAHP synthase |
|
Réactions -2- |
3-déshydroquinate synthase (DHQ
synthase) |
|
Réaction -3- |
Quinate déshydrogénase |