EXERCICE 19
Corrigé
Enoncé :
Un composé organique A, contenant du
carbone, de l'hydrogène, de l'azote et de l'oxygène, a la composition
centésimale massique suivante : carbone 40,45%, hydrogène 7,86%, azote
15,73%. Sa masse molaire est MA = 89 g.mol-1.
Mc =12 g.mol-1
MH=1 g.mol-1
MO=16 g.mol-1
MN=14 g.mol-1
MCl=35,5 g.mol-1
1) Quelle est la
formule brute de A ?
2) Par réduction de A
on obtient une monoamine saturée B de formule moléculaire C3H9N,
qui réagit avec le nitrite de sodium en milieu acide chlorhydrique pour donner
un alcool D. Quelles sont les formules possibles pour B ?
3) L'oxydation de D
donne un produit E de masse molaire 58 g.mol-1
; celui-ci réagit avec la 2,4-DNPH et ne réduit pas la liqueur de Fehling.
Identifier A,B,C,D,E (nom et formule semi-développée).
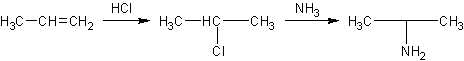
4) Donner un chemin de
synthèse pour arriver à B à partir du propène.
Corrigé :
1) Posons
la formule moléculaire générale de A : CxHyNzOw
12x/40,45 = y/7,86 = 14z/15,73 = 89/100
Soit x = 40,45.89/(12.100) = 3 y = 7,86.89/100 = 7 z = 15,73.89/(14.100) = 1 La masse molaire nous permet de
trouver w = (89 – (12.3 + 7.1 + 14.1))/16 = 2
A : C3H7NO2
2) C3H7NO2 + 3 H2
→ C3H9N + 2H2O
Les formules possibles pour B :
CH3-CH2-CH2-NH2 propanamine
![]() 2-méthyléthanamine
2-méthyléthanamine
3)
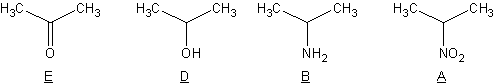
4)