LES
ORGANO-MAGNESIENS
Ou réactifs de Grignard
1) Formule
générale
2) Nomenclature
3) Préparation
4) Réactions importantes
5) Action du dioxygène
6) Action des dihalogènes
7) Résumé
R-MgX en pratique, X est Cl,Br, ou I (mais la chimie du fluor est à part dans bien des domaines); R est un radical hydrocarboné quelconque .
Halogénure + nom du radical R- + magnésium.
ex: C2H5-MgCl chlorure d’éthylmagnésium
Une seule méthode de préparation:
R-X + Mg
-------> R-MgX dans l’éther anhydre (ou le tétrahydrofuranne)
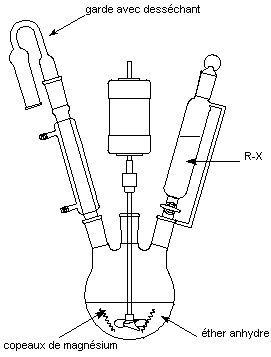
Le magnésien est ensuite utilisé directement dans l’éther; il n’est jamais isolé.
Très nombreuses mais seulement de deux types:
* Réactions avec les composés à hydrogène mobile
Rd--MgXd+ + Ad--Hd+ ----------> R-H + A-Mg-X
L’écriture A-Mg-X est symbolique; le résultat dépend de la nature de A.
ex1:
R-MgX + H2O ----------> R-H + X-Mg-OH (½ MgX2 + ½ Mg(OH)2)
Les magnésiens doivent être préparés à l’abri de l’humidité.
ex2:
![]()
Les composés à hydrogène mobile sont: l’eau, les alcools, les phénols, tous les acides, l’ammoniac et les amines, ........
Remarque: ces réactions conduisent le plus souvent à la destruction du magnésien et sont à éviter.
*Additions sur les composés à groupement C=O (presque toujours suivies d’une hydrolyse)
![]()
![]()
ex:
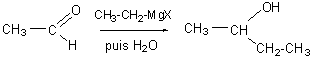
c’est-à-dire un alcool secondaire.
Les composés à groupement C=O sont :
Les aldéhydes, les cétones, les chlorures d’acyle, les anhydrides d’acide, les esters, le dioxyde de carbone.
Remarque 1: dans R-C(OH)=O le groupement C=O ne réagit pas de cette façon. L’acide réagit par son H (composé à H mobile).
Remarque 2: On peut ajouter les nitriles R-CN mais il n’y a jamais addition sur une double liaison éthylénique ou une triple liaison acétylénique.
R-MgX + ½ O2 ----------> R-O-MgX
Les magnésiens doivent être préparés à l’abri de l’air
R-MgX + X’2 ----------> R-X’ + Mg(X)X’ (½ MgX2 + ½ MgX’2)
La réaction n’est simple que si X’ est plus lourd que X; elle est utilisée au dosage des magnésiens (X’2 étant I2).