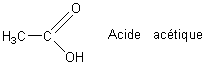
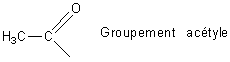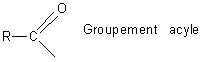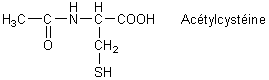ACIDE ACETIQUE
(Wolfgang WERNER – Münster)
Le terme français vinaigre donne un aperçu de la composition
de cet acide issu du vin et utilisé, entre autres, comme condiment.
Lors de la fermentation alcoolique du jus de raisin, le sucre (glucose) qu'il
contient se transforme en éthanol et dioxyde de carbone. C'est l'énergie
résultant de cette transformation qui permet à la levure saccharomyces
cerevisiae, dont les spores se trouvent partout et qui entrent avec le
raisin dans le moût, de se multiplier.
Le processus de fermentation se déroule à l'abri de
l'oxygène de l'air, on parle de processus anaérobie (du grec aer qui
signifie l'air et an- préfixe privatif). Le bilan des réactions
enzymatiques connues qui interviennent dans ce processus, peut être décrit par
l'équation suivante:
Le jus de raisin n'est pas le seul à pouvoir fermenter,
c'est aussi le cas de toutes les solutions glucosées ; c'est ainsi que l'on
obtient le "vin de pomme" (cidre) à partir du jus de pomme. Les
solutions glucosées aqueuses qui contiennent plus de 100 à 250g de sucre par
litre, ne fermentent plus. Les solutions que l'on obtient peuvent atteindre une
concentration maximale en alcool de 15% en volume ; un taux plus important
empêcherait la fermentation.
Si on laisse du vin à l'air libre à température ambiante, il
deviendra acide (en latin vinum acidum). Par acide, on n'entend pas ici
l'acidité naturelle du jus non fermenté (moût). Il faut aussi qu'apparaisse
l'odeur caractéristique de l'acide acétique (illustration 1), on dit alors que le vin est piqué. Les romains
connaissaient et utilisaient le vinaigre.
L'appellation vinaigre décrit bien cette réaction parasite. Le vin devient
aigre, du latin acer, aigre, acéré. L'anglais en a tiré le terme
"vinegar" ; même association de mots, en espagnol et en portugais
"vinagre".
C'est Antoine de Lavoisier (1743-1794) qui a découvert que
la formation du vinaigre correspondait à l'oxydation de l'alcool.
C'est ce même Lavoisier qui a formé le mot oxygène: il a supposé que cet
élément était contenu dans tous les acides et a assemblé les termes grecs
"oxys" acide et "genein" former.
C'est à Louis Pasteur (1808-1873) que nous devons la
découverte de la nature biochimique du processus de formation du vinaigre. A
partir de 1865, sur la base des recherches de Pasteur, la production
industrielle de vinaigre a connu un grand essor. La bactérie du vinaigre "aceto-bacter" se développe dans le vin non
bouché. Les petites mouches qui sont fortement attirées par le vin placé à
l'air libre et qu'on appelle mouches du vinaigre (drosophiles) véhiculent
l'aceto-bacter. Les bactéries de l'acide acétique forment une couche à la
surface que l'on appelle la mère du vinaigre. L'aceto-bacter utilise pour vivre
l'énergie libérée par l'oxydation. Les processus qui ont lieu en présence
d'oxygène de l'air sont dits aérobies. Toute solution
alcoolique diluée peut donner de l'acide acétique ; dans ce cas le taux
d'alcool correspond à la quantité d'acide acétique qui résultera de la
transformation.
Interruption du processus de formation du vinaigre.
Lors de la fermentation du vin, le processus de transformation du vin en
vinaigre est indésirable. C'est pourquoi on ferme les fûts de moût en
fermentation avec des dispositifs qui laissent sortir le dioxyde de carbone formé
sans permettre à l'air de pénétrer.Le dispositif employé empêche non seulement
la pénétration de l'oxygène de l'air mais aussi celle de l'aceto-bacter et
d'autres microorganismes présents dans l'air ambiant qui tous contribuent à la
détérioration du vin . De cette manière, le vin jeune lui, au moins, est
protégé. Reste le problème du stockage et du transport ; on sait d'après des
fouilles que dans l'Egypte ancienne, le vin était contenu dans des tonneaux
bouchés par des petits morceaux de bois ; les grecs et les romains qui furent à
l'origine de la diffusion du vin et de la viniculture en Europe, utilisaient
aussi cette technique. Pour rendre les amphores étanches ils utilisaient en
outre de l'argile ou du plâtre. Ils auraient aussi utilisé de l'écorce de
chênes-lièges, arbres courants dans le bassin méditerranéen. L'utilisation du
liège est pourtant tombée en désuétude. L'utilisation
de la résine de pin pour rendre les amphores étanches, conférait au vin un goût
particulier. C'est de cette pratique qu'est tiré le nom "Retsina". Le
Retsina que l'on trouve aujourd'hui en Grèce en est un descendant proche.
Le vin de l'antiquité ne se consommait pas pur, on l'aromatisait avec des
herbes et des épices ; ces additifs permettaient également une meilleure conservation
du vin. La technique consistant à accroître la durée de conservation du vin par
ébullition avec les épices était déjà en usage chez les romains. On n'a compris
que plus tard que cette pasteurisation détruisait les bactéries et les
champignons. L'adjonction de SO2
entrave l'activité des bactéries de l'acide acétique.
C'est au XVIIème siècle que
l'on commence à utiliser des bouteilles en verre pour y
conserver le vin. Ces bouteilles étant fermées à l'aide de bouchons de chanvre
trempés dans de l'huile. Le nom "Dom Pérignon" moine bénédictin à
Hautvilliers près d'Epernay évoque immédiatement le champagne ; mais ce qui est
à retenir c'est qu'il fut le premier à fermer ses bouteilles à l'aide de
bouchons de liège (1688). En ce qui concerne les bons crus, les bouchons en
liège n'ont jamais été supplantés.
Les sels anorganiques de l'acide acétique.
Sucre de plomb: Afin de sucrer
leur vin, les romains faisaient épaissir du jus de raisin dans des récipients
de plomb ou d'argile recouverte d'une couche de vernis au plomb ; on obtenait
ainsi un sirop destiné à améliorer la qualité du vin. Plus tard, ils ont aussi
dissous du plomb dans le vinaigre. Le vin ainsi amélioré était destiné à la haute société de Rome.
On a découvert dans les ossements humains de cette époque d'importantes
quantités de plomb, de sorte qu'on suppose que la chute de l'empire romain est
en partie liée à un empoisonnement massif par le plomb.
Au moyen-âge, on ajoutait encore le sucre de plomb (Pb(CH3COO)2)
et également le blanc de plomb (PbCO3)
afin d'améliorer le vin, bien que la toxicité du plomb qui pouvait s'avérer
mortelle fût connue.
L'adjonction de plomb permettait non seulement d'adoucir le vin mais aussi
d'éliminer des acides, car il se forme de l'oxalate de plomb et du tartrate de
plomb.
Samuel Hahnemann (1755 –1843) que nous connaissons comme fondateur de
l'homéopathie était un pharmacien versé dans la chimie. La liqueur de Hahnemann
pour tester le vin était une solution acidifiée et saturée en "gaz
hépatique" („Schwefelleberluft“), c'est-à-dire en sulfure d'hydrogène,
solution qui, en présence de plomb, se transformait en PbS et donnait au vin
traité une couleur sombre.
Vert de gris: Si l'on trempe du
cuivre dans du vinaigre, il se forme peu à peu une couche verte d'acétate de
cuivre basique, que l'on appelle vert de gris, particulièrement sur la face
supérieure en contact avec l'air. On a gratté cette couche et on l'a utilisée
comme pigment en peinture. La patine sur les toits de cuivre correspond, elle, a du carbonate de cuivre basique.
En 1800, Ignaz von Mitis a découvert à
Vienne, un pigment d'un vert intense composé d'un mélange d'acétate et
d'arsénite de cuivre, qu'on a dans un premier temps appelé vert de Mitis. C'est
après la première fabrication industrielle de cette substance à Schweinfurt
qu'on lui a donné le nom de vert de Schweinfurt. Sous l'influence de
microorganismes, se développent, à partir de ce pigment "grand teint"
et de son liant, des composés organiques avec l'arsenic qui, inhalées pouvaient
conduire à des empoisonnements. C'est pourquoi ce pigment a été qualifié de
"vert poison" (en français vert criard). En raison de sa toxicité, le
vert de Schweinfurt a été interdit dès 1882 mais a été utilisé encore quelques
années comme insecticide.
Essigsaure Tonerde*
Cet ancien remède de bonne femme correspond à une solution acide d'acétate
d'aluminium. Son effet astringent est à imputer à l'aluminium, tandis que
l'effet anti-inflammatoire est à mettre au compte de l'acide acétique ou plutôt
de l'ion acétate.
* Note de l'auteur: Cette solution se trouve dans la
pharmacopée allemande, mais ni dans la pharmacopée européenne, ni dans la
pharmacopée française. Cette solution à usage externe est inconnue et n'est pas
commercialisée en France.
Vinaigre
Il est évident que partout où l'on connaissait le vin on connaissait aussi
l'acide acétique. En effet le vinaigre était déjà utilisé comme condiment dans
la cuisine des égyptiens, des grecs et des romains. Les chinois eux aussi
l'avaient déjà produit il y a plus de 4000 ans.
Le vinaigre balsamique (Ital.: aceto balsamico) est un vinaigre particulier
dont on trouve pour la première fois la trace à Modène aux environs de l'an
1600. L'appellation vinaigre balsamique n'est pas protégée et ne garantit donc
ni l'origine, ni la qualité de ce produit.
Les soldats romains utilisaient de l'eau de vinaigre comme boisson
rafraîchissante. On comprend ainsi mieux, pourquoi ils ont tendu du vinaigre à
Jésus sur sa croix.
Outre son utilisation comme condiment, le vinaigre est aussi fréquemment
utilisé pour ses propriétés de conservation. On connaît depuis le XVIIème siècle , les légumes et le poisson en
conserve (cornichons et harengs).
L'acide acétique et ses sels sont autorisés comme moyens de conservation ou
d'acidification sans qu'une limite supérieure des quantités soit fixée.
L'acide acétique est soluble non seulement dans l'eau mais aussi dans les
matières grasses. Il transperce les parois des cellules des microorganismes et
dénature les protéines. Certaines sortes de pains peuvent contenir entre 0,2 et
0,4% d'acétate de sodium (E262). Les récipients
où l'on conserve le pain et les réfrigérateurs devraient être lavés à l'eau
vinaigrée afin de les protéger de la moisissure.
Dans la première moitié du XXème
siècle la théorie des radicaux était la préoccupation principale des chimistes.
C'est pourquoi on n'est pas sûr que les noms radical acétyle et radical acyle (illustration 2) viennent de Berzélius ou de Liebig.
En tous cas à l'époque, un radical était un groupe d'atomes qui en tant que
tels pouvaient être substitués les uns aux autres. Aujourd'hui un radical est
caractérisé par un électron non apparié.
L'acétylène (illustration 3) a été ainsi nommé par
J.B.Dumas (1800-1884) qui a mené des expériences avec ce gaz présentant des
propriétés semblables à l'éther, mais non acide et n'ayant pas d'odeur acide et
qui a obtenu l'acide acétique.
Biochimie
L'acide acétique "activé" ou l' AcétylCoA sont des appellations
courantes pour l' Acétylcoenzyme A. Il s'agit d'une substance clé dans le cycle
de l' acide citrique, aussi bien pour construire que pour métaboliser les
acides gras. Durant ce processus le groupement acétyle de l'acide acétique est
transféré. Le transfert du groupe acétyle depuis l'acétylcholine sur le groupe
OH de la sérine de l'acétylcholinestérase (illustration
4) est une des réactions centrales qui permet la compréhension de
l'activité de ce neurotransmetteur.
Le transfert du groupement acétyle de l'aspirine (illustration
5) sur le reste de sérine de la cyclooxygénase (illustration
4) empêche que cette enzyme forme les médiateurs de douleur et
d'inflammation que sont les prostaglandines.
Le transfert du groupement acétyle depuis l'acétylcystéine (illustration 6) sur les molécules du mucus conduit à
une réduction de la viscosité et facilite l'expectoration (mucolyticum).
De même que pour l'éthanol, il existe aujourd'hui des procédés industriels permettant la fabrication de l'acide acétique sur lesquels il ne sera pas possible ici de s'étendre non plus que sur les réactions connexes.
Johann Rudolf Glauber (1604-1668) décrit en 1658 dans son opéra chimicae non seulement le sulfate de sodium, auquel il a donné son nom, mais aussi comment obtenir du vinaigre de bois par une distillation sèche du bois. Mais il fallut encore 160 ans pour montrer que ce vinaigre de bois était identique au vinaigre de vin. L'acide des romains était l'acetum, acide acétique, cela vient du latin acer (acide, acéré). De ce terme sont dérivés les termes français acide et anglais acid. L'acetum a assez tôt franchi les alpes en direction du nord et est devenu en vieil allemand du IXème siècle essich. Le mot Säure est d'origine germanique. On peut dire que les appellations Essigsäure, acide acétique et acetic acid sont des pléonasmes.
|
|
TRADUCTION EN FRANCAIS : Anne-Sophie GOMEZ