SYNTHESE DU 3-NITROBENZALDEHYDE
1) Données
1-1) Sécurité :
Le port des lunettes est obligatoire durant la manipulation.
- Acide nitrique
fumant: très corrosif .Vapeurs toxiques et irritantes.
- Acide sulfurique concentré: très corrosif. Provoque des
brûlures au contact de la peau
- Benzaldéhyde: dangereux par absorption ou inhalation.
- Ether de pétrole: très inflammable.
- 3-nitrobenzaldéhyde: irritant
pour la peau.
- Toluène: toxique, inflammable.
1-2) Constantes physiques :
- Acide
nitrique fumant :
M = 63,02 g/mol
d = 1,42
Pur à 98 % en masse.
- Benzaldéhyde :
M = 106,12 g/mol
Liquide huileux qui s'altère à l'air
d = 1,0415
Eb = 178,1°C
Peu soluble dans l'eau. Miscible à l'alcool et l'éther.
- Ether de
pétrole :
d = 0,65 à 0,66
Eb = 30 à 60°C
Insoluble dans l'eau, soluble dans les hydrocarbures.
- 3-nitrobenzaldéhyde
M = 151,12 g/mol
Solide jaune pâle
d = 1,2792
Fusion : température inférieure à 65°C.
Peu soluble dans l'eau, très peu soluble dans l'éther de pétrole. Très soluble
dans le toluène à 20°C.
Isomères de position du produit préparé :
Ortho (F = 45°C) Para (F = 106°C)
Peu solubles dans l'eau et l'éther de pétrole. Très soluble dans le toluène.
Impuretés acides se formant éventuellement lors de la nitration :
Très peu solubles dans l'eau.
Non solubles dans le toluène. Solubles dans l'éther de pétrole.
2) Mode opératoire :
2-1) Préparation du 3-nitrobenzaldéhyde
:
Dans un réacteur de 500 mL équipé
d'une agitation, d'un thermomètre, d'un réfrigérant ascendant, et d'une ampoule
de coulée, introduire un mélange de 11 mL d'acide
nitrique fumant et de 25 mL d'acide sulfurique
concentré.
Refroidir à 0° C dans un mélange glace-sel.
Verser sous agitation 31 g de benzaldéhyde pur en veillant à
ce que la température ne dépasse pas 5°C. L'opération dure environ une heure.
Veiller à ce que l'agitation soit suffisante pour éviter la formation de deux
phases.
Lorsque l'addition est terminée, chauffer progressivement
jusqu'à 40°C, laisser refroidir, puis verser très lentement le mélange
réactionnel sur de la glace pilée en agitant vigoureusement. Commencer avec
250g de glace et en ajouter au cours de l'opération de façon à ce qu'il reste
toujours un peu de glace.
Ajouter à ce mélange 8 g de carbonate de sodium solide, en agitant fortement.
Filtrer sur buchner. Laver le précipité avec 50 mL d'eau.
Essorer de façon à éliminer le plus complètement possible la
partie huileuse accompagnant le produit. Faire fondre celui-ci en présence de
100 mL d'une solution de carbonate de sodium à 5 %.
Agiter 10 minutes puis refroidir dans un bain de glace, tout
en agitant vigoureusement. Filtrer sur büchner.
Laver à l'eau jusqu'à pH neutre. Bien essorer.
Sécher sur papier filtre. Peser le produit humide.
Sécher à l'étuve à 40°C jusqu'à masse constante, un
prélèvement m1 d'environ 5 g. Peser. Recristalliser un second
prélèvement m2 de 5 g de la façon suivante :
Dissoudre 5 g de produit brut dans le minimum de toluène.
Dans la solution toluènique tiède ajouter par petites
quantités et sous agitation de l'éther de pétrole sensiblement à la même
température jusqu'à l'obtention d'un trouble permanent.
Refroidir dans la glace en agitant vigoureusement.
Séparer l'aldéhyde ainsi purifié. Sécher sur papier filtre,
à l'étuve à 40°C jusqu'à masse constante. Peser.
Prendre la température de fusion du produit pur. Présenter
les produits.
2-2) Analyse :
Effectuer une CCM en déposant sur une même plaque : le
benzaldéhyde, les 3-nitrobenzaldéhyde préparés (brut
et pur), le commercial et l'acide 3-nitrobenzoique.
Les échantillons de 0,1 g environ sont dissous dans le minimum d'acétone.
L'éluant est un mélange de toluène et d'acétate d'éthyle 3/1, avec quelques
gouttes d'acide acétique. La révélation est faite en exposant la plaque à la
lumière ultra-violette (254 nm).
3) Questions :
3-1) Questions sur la préparation :
3-1-1)
Pourquoi doit-on utiliser pour la préparation du benzaldéhyde fraîchement
distillé ? De quelle impureté veut-on se débarrasser ?
3-1-2)
Ecrire l'équation bilan de la réaction de nitration du benzaldéhyde.
3-1-3) Quels
sont les produits secondaires formés lors de la nitration?
3-1-4)
Pourquoi doit-on utiliser impérativement l'acide nitrique fumant?
3-1-5) Quels
sont les rôles joués par l'acide sulfurique?
3-1-6)
Pourquoi la température du mélange réactionnel ne doit-elle pas dépasser 10°C?
3-1-7)
Pourquoi l'utilisation de la glace et une agitation vigoureuse sont-elles
indispensables lorsqu'on dilue le mélange réactionnel?
3-1-8) Les
traitements de la phase solide par les solutions de carbonate de sodium à 5% en
excès ont pour but d'éliminer certains composés se formant lors de la nitration
:
a- Quels sont-ils?
b- Ecrire l'équation générale des réactions ayant lieu lors du traitement.
c- Quel est le but du lavage à l'eau?
3-1-9)
Justifier l'utilisation du mélange des deux solvants toluène et ether de pétrole pour la recristallisation.
3-2) Partie
quantitative :
3-2-1)
Calculer les quantités de matière de benzaldéhyde et d'acide nitrique mises en
jeu.
3-2-2) En déduire
la masse théorique de 3-nitrobenzaldéhyde obtenue.
3-2-3)
Donner les expressions littérales des rendements R1 et R2 en
produit brut et pur. En déduire celle du rendement R3 de la
recristallisation.
3-3) Questions sur l'analyse :
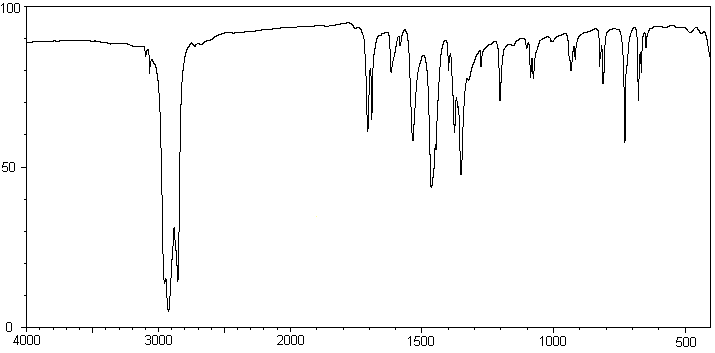
Les spectres I.R. du benzaldéhyde,
et celui du 3-nitrobenzaldéhyde sont donnés
ci-dessous.
Quelles sont les bandes d'absorption des vibrations communes aux deux produits,
et celles qui les différencient?
A quoi est du l'épaulement à 3250 cm-1 observé sur le spectre du
benzaldéhyde?
Spectre
IR du benzaldéhyde
:
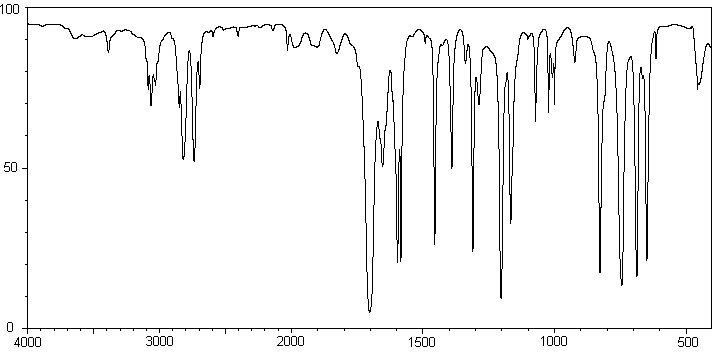
Spectre
IR du 3-Nitrobenzaldéhyde :