EXERCICE 119
Formule
de l'alanine
:
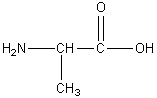
Lorsqu’on dissout de l’alanine dans l’eau,
elle est principalement sous forme d’ion dipolaire.
1) Ecrire les deux couples acido basiques relatifs à la
mise en solution de l’alanine dans l’eau.
2) Calculer le pH d’une solution aqueuse d’alanine à 0,10 mol.L-1.
Sous quelle forme trouve-t-on l’alanine en solution aqueuse ?
3) A 100mL de cette solution on ajoute sans variation de volume nHCl
= 1.10-2
mole d’acide chlorhydrique.
Calculer, le pH de la solution obtenue.
Données : alanine : pKa1 = 2,3 ; pKa2 = 9,9.
Pour simplifier l’écriture des équations de réactions on pourra noter l’amphion ou zwitterion : AH+
-.