REACTION DE
MAILLARD
Gérard GOMEZ
Plan de
l'étude :
1) La réaction de
Maillard et les aliments
1-1) Définitions
1-2) Influence de la nature des glucides sur la réaction de Maillard
1-3) Influence de la nature des acides aminés sur la réaction de
Maillard
1-4) Quelques classes de composés issus de la réaction de Maillard
2) La réaction
de Maillard dans l'organisme
2-1) La glycosylation
2-2) La glycation
Annexe : Louis
Camille Maillard
1) La
réaction de Maillard (voir annexe) et les aliments :
1-1) Définitions :
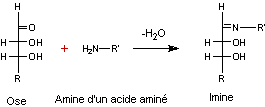
C'est une réaction entre
la fonction carbonyle
|
|
d'un ose et la fonction
amine (-NH2) d'une protéine ou d'un acide aminé, à chaud.
Il se forme une imine, qui
se réarrange (réarrangement d'Amadori) et conduit à une cétone qui peut alors
réagir elle aussi avec une autre fonction amine. Il peut ainsi se produire une
polymérisation qui aboutit à des produits bruns.
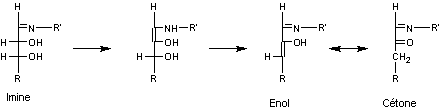
Réarrangement d'Amadori:
La réaction de Maillard est favorisée à pH compris entre 4 et 7, gamme de pH de
la plupart des aliments et donne les produits bruns de la bière.
C'est ainsi aussi que
l'on obtient la teinte d'un brun plus ou moins foncé de la croûte du pain, du
café torréfié, du sucre de canne roux, de la viande grillée, …...
Cette réaction intéresse beaucoup
l'industrie agro-alimentaire car elle conditionne fortement le développement
d'arômes et de textures croustillantes.
Signalons que la réaction de
Maillard peut présenter quelques inconvénients :
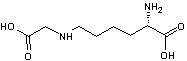
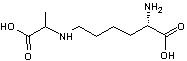
Elle rend inassimilable la lysine (acide aminé essentiel) qui a
subi cette transformation dans certains produits en conserves. Il se trouve que
cet acide aminé en particulier est plus spécialement mis en jeu dans le
phénomène.
Les produits qui se forment lors de
la réaction de Maillard (MRP pour Maillard Reaction Products, ou AGEs pour
Advanced Glycation End-products ou PTG pour Produits Terminaux de Glycation)
dans les aliments à forte teneur en sucre et en présence d'acides aminés sont
très nombreux et n'ont pas tous été identifiés. Pris dans leur ensemble les MRP sont néphrotoxiques à fortes doses. Certains d'entre eux
présentent des effets mutagènes et d'autres à l'inverse ont un effet protecteur
de la mutagénèse.
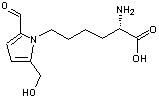
Parmi les nombreux composés
identifiés on trouve les furannoses : hydroxyméthylfurfural, furanosine, furfuraldéhyde.
Les données toxicologiques ne
permettent pas en 2019 l'établissement d'une DJT (dose journalière tolérable)
pour les MRP.
Le schéma simplifié de la réaction de Maillard (adapté de Hodge, 1953) est le suivant :
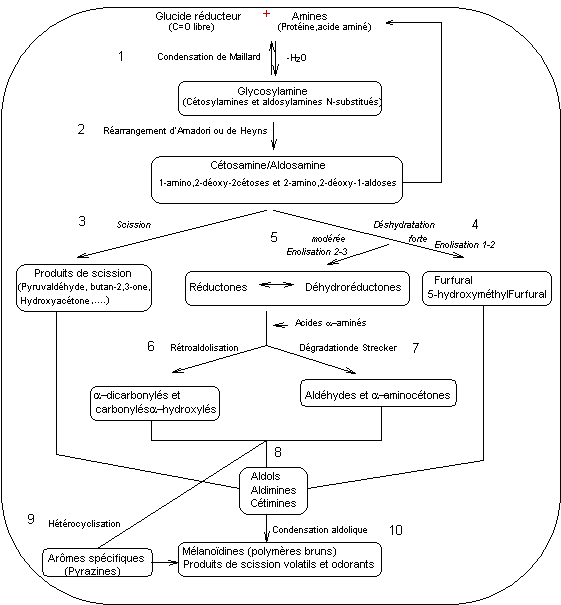
Le
détail des étapes numérotées de 1 à 10 est le suivant :
-1- Condensation
de Maillard :

Remarque :
Avec un
cétose on obtient
:
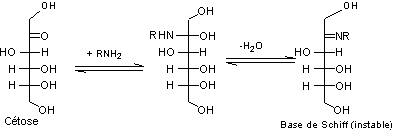
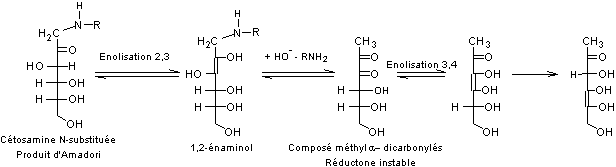
-2- Réarrangement
d'Amadori – Réarrangement
de Heyns:
En
partant d'un aldose et notamment par action d'un acide aminé la base de
Schiff subit rapidement un réarrangement
d'Amadori et on aboutit à une cétosamine :
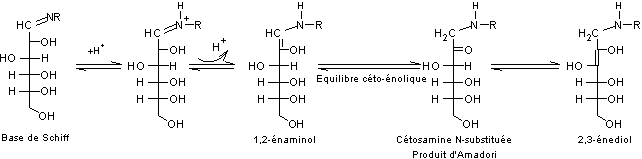
En
partant d'un cétose la base de Schiff subit un réarrangement de Heyns et on
aboutit à une aldosamine :
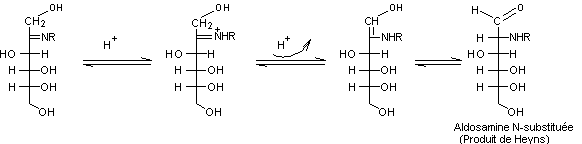
-3- Produits de
scission :
|
|
|
|
|
Pyruvaldéhyde ou Méthylglyoxal |
Butan-2,3-one ou Diacétyle |
Hydroxyacétone |
-4- Déshydratation
forte :
Elle est
favorisée en milieux acides.
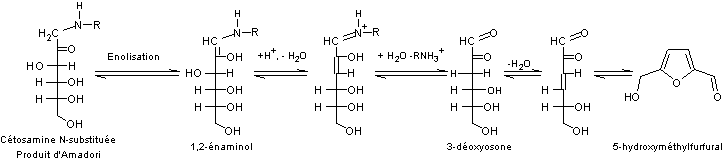
La
polymérisation du 5-hydroxyméthylfurfural donne des produits bruns
(mélanoïdines) :
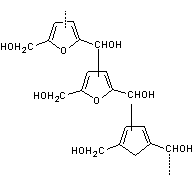
-5- Déshydratation modérée :
Elle se
produit en milieu neutre ou légèrement alcalin.
-6 et 7- Dégradations
de Strecker

-8,9,10- Scission,
condensation et polymérisation :
Ces
réactions finales donnent des produits volatils,odorants et colorés en brun par
des mélanoïdines.
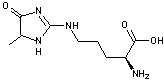
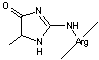
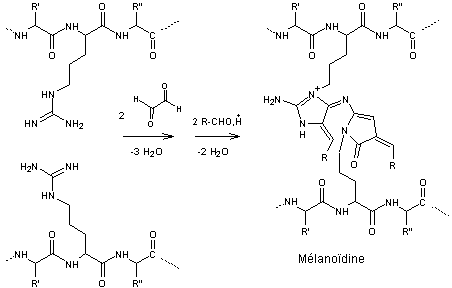
Schéma
de synthèse de mélanoïdines à partir de réductones et de résidus d'arginine
(d'après Hofmann, 1988)
1-2) Influence de la
nature des glucides sur la réaction de Maillard :
Plus le
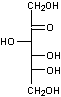
nombre d'atomes de carbones est petit plus le glucide est réactif ; les cétoses
sont plus réactives que les aldoses.
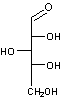
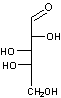
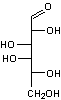
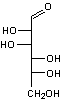
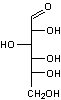
Ainsi
le D-xylose est plus réactif (>) que le L-arabinose > D-fructose >
D-galactose > D-mannose > D-glucose > maltose > lactose
>saccharose.
|
|
|
|
|
|
|
|
D(+)-Xylose |
L(+)-Arabinose |
D(-)-Fructose |
D(+)-Galactose |
D(+)-Mannose |
D(+)-Glucose |
Un glucide
sous forme hémiacétalique ne donne pas de réaction de brunissement. C'est le
taux de forme ouverte qui conditionne la réactivité :
|
% de forme ouverte |
|||
|
|
pH 6,6 |
pH 7,0 |
pH 7,5 |
|
D-Glucose |
0,012 |
0,022 |
0,04 |
|
D-Mannose |
0,04 |
0,06 |
0,1 |
|
D-Ribose |
10 |
18,5 |
30 |
1-3) Influence de
la nature des acides aminés sur la réaction de Maillard :
La
nature des acides aminés influe aussi sur la réactivité :
|
Acides aminés |
Réactivité relative |
|
L-Glycocolle |
100 |
|
L-Alanine |
100 |
|
D,L-Ornithine |
400 |
|
L-Lysine |
480 |
(D'après
"Réactions de brunissement" Stéphane Bouquelet- Professeur -
Université des sciences et technologies de Lille – 20 avril 2016).
1-4) Quelques classes de composés
issus de la réaction de Maillard : (van Boekel, 2006)
|
Famille chimique |
Molécules |
Arôme
associé |
Exemple d'aliment |
|
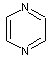
Pyrazines |
|
cuit,
rôti, toasté, céréales cuites |
aliments
chauffés en général |
|
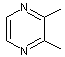
Alkylpyrazines |
|
noix,
rôti |
café |
|
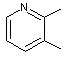
Alkylpyridines |
|
vert,
amer, astringent, brûlé |
café, orge, malte |
|
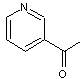
Acylpyridines |
|
cracker |
produits céréaliers |
|
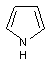
Pyrroles |
|
céréales |
céréales, café |
|
Furannes, furanones, pyranones |
|
sucré-doux, brûlé, âcre, caramel |
aliments chauffés en général |
|
Oxazoles |
|
vert, noix, sucré-doux |
cacao, café, viande |
|
Thiophènes |
|
viande |
viande cuite |
2) La réaction de Maillard dans l'organisme :
La fixation
d'un glucide réducteur sur une protéine ou un peptide peut avoir lieu dans le
corps humain. Il existe deux types d'assemblage qui conduisent tous les deux à
des glycoprotéines mais qui sont fondamentalement différents.
2-1) La
glycosylation :
Elle se fait
par voie enzymatique et est un phénomène qui intervient normalement lors de la
biosynthèse de certaines protéines membranaires ; des oligosaccharides
s'ajoutent à la protéine en voie d'élaboration,
- soit au niveau d'un
atome d'azote (N-glycosylation)

- soit au niveau d'un
atome d'oxygène (O-glycosylation)

(Schémas extraits de PLANET VIE
(ENS-Eduscol) Glycosylation et glycation : Quelles différences ? Publication le
20 février2014 – dernière modification le 30 septembre 2016).
La
glycosylation n'est pas une réaction de Maillard.
2-2) La
glycation :
C'est une
réaction chimique (non enzymatique) qui se produit spontanément entre un
glucide et une protéine, qui dépend de la concentration en glucide et de la
température (elle se produit de façon significative à 37°C) et qui conduit à
des produits, AGEs (pour Advanced Glycation End-products) désignés en français
par PTG (Produits Terminaux de Glycation) qui s'accumulent dans l'organisme
(vaisseaux sanguins notamment) et participent au vieillissement, à la survenue
et au développement de l'artériosclérose, l'insuffisance rénale, la
rétinopathie diabétique et la cataracte.
Ces AGEs
résultent de la glycation des protéines et lipoprotéines au niveau des -NH2
libres des lysines et arginines.
La glycation
est une réaction de Maillard.
Le schéma
ci-dessous résume les chemins menant du glucose aux AGEs ou PTG :
(d'après Advanced glycation end-products : a review
R.Singh, A.Barden, T.Mori, L.Beilin
Dpt of medicine, University of western Australia and West Australian Heart
Research Institute, Perth, Australia)
Diabetologia Springer-Verlag 2001

Quelques
formules :
- D'α-oxoaldéhydes :
|
|
|
|
|
Glyoxal |
Méthylglyoxal |
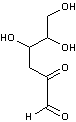
3-DG ou 3-déoxyglucosone |
- D' AGEs :
|
|
|
|
|
CML ou N-6-CarboxyMéthylLysine |
CEL ou
N-6-CarboxyEthylLysine |
Pyrraline |
|
|
|
|
|
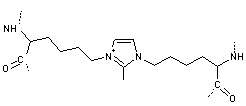
GOLD ou GlyOxal-Lysine-Dimère |
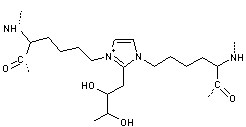
MOLD ou MéthylglyOxal-Lysine-Dimère |
DOLD ou DéOxyglucasone-Lysine-Dimère |
|
ou
|
ou
|
ou
|
|
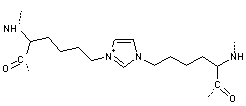
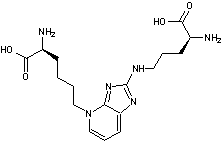
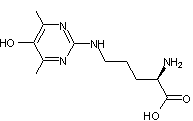
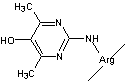
Pentosidine |
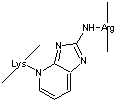
5-Hydro-5-méthyl-imidazole |
Argpyrimidine |
On estime
que 10% seulement des AGEs retrouvés in vivo ont une origine
alimentaire.
Remarque :
La
pentosidine est naturellement fluorescente et cette propriété explique
l'augmentation de la fluorescence observée dans le collagène, où elle se forme
majoritairement, au cours du vieillissement ou au cours de certaines
pathologies telles le diabète de type 1 ou lors d'un dysfonctionnement rénal.
La fluorescence est devenue une méthode globale (assez approximative tout de
même) d'évaluation du taux de glycation dans les tissus biologiques.
2-3) L'hémoglobine
glyquée :
Parmi les
protéines qui subissent la glycation, l'une d'entre elles est particulièrement
intéressante à observer, c'est l'hémoglobine.
La glycation
de l'hémoglobine conduit à de l'hémoglobine glyquée (HbA1c) découverte dans les
années 1970, qui est un marqueur du taux de glucose fixé par l'hémoglobine dans
les 3 mois qui précèdent la prise de sang.
Ce taux
permet de suivre l'état de la glycémie chez le patient sur une longue période
alors que l'évaluation de la glycémie à jeun n'est qu'un reflet instantané de
cet état.
Les globules
rouges ont une demi-vie de 120 jours environ ; après ils sont dégradés dans la
rate et dans le foie.
Le glucose
se fixe de manière irréversible sur l'hémoglobine et s'accumule progressivement
dans les globules rouges.
Une prise de
sang tous les 3 mois permet à un laboratoire d'analyses de mesurer le taux
d'hémoglobine des globules rouges ayant fixé du glucose durant toute leur vie.
On peut ainsi apprécier l'équilibre glycémique pendant deux à trois mois.
Un diabète
est considéré comme équilibré si le taux d'HbA1c est inférieur ou égal à 7%.
Louis
Camille Maillard,
né le 4
février 1878 à Pont-à-Mousson (Meurthe et Moselle) mort le 12 mai 1936 à Paris
est un médecin et chimiste français.
Son
importante contribution aux travaux sur les réactions entre acides aminés et
sucres est considérée comme majeure ; on a donné son nom à l'ensemble de ces
réactions complexes.