LES PETROLES,
des hydrocarbures jusqu'en C 40,
au moins.
1) Origine
– Composition – Distillation fractionnée :
Les
pétroles sont des mélanges complexes d'hydrocarbures qui se sont formés par
fermentation de matières organiques et décomposition de microorganismes marins
enfouis il y a plusieurs centaines de millions d'années et qui ont été soumis
aux effets combinés de la température, de la pression et à l'action de
bactéries. Les hydrocarbures formés ont été maintenus sous des couches de
roches imperméables et ont imbibé une roche appelée "roche magasin".
Les
pétroles bruts se présentent sous forme d'une huile très visqueuse, de couleur
foncée à reflets marron ou vert sombre et à odeur variable mais le plus souvent
désagréable.
Leur
composition varie suivant leur provenance : ceux du Moyen- Orient, du Sahara,
de Pennsylvanie pour ne citer qu'eux, sont formés essentiellement d'alcanes,
ceux du Texas de cyclo-alcanes ; ceux du Caucase et d'Indonésie de
cyclo-alcanes et de carbures aromatiques.
Ils
subissent un premier traitement qui est une distillation fractionnée permettant
de recueillir des groupes de composés (groupes appelés "coupes
pétrolières") dont les points d'ébullition se situent dans un intervalle
donné.
Le
résultat de ce fractionnement permet d'avoir un aperçu de la composition d'un
pétrole, des températures d'ébullition des composés obtenus dans une coupe,
ainsi que l'ordre de grandeur de leurs quantités respectives.
|
Températures auxquelles les fractions sont
recueillies |
Fractions recueillies |
Types d'hydrocarbures présents dans ces
fractions. |
Quantités en % en masse. |
|
Jusqu'à 40°C |
Alcanes linéaires ou ramifiés de C1 à C4. Gaz naturels : méthane
et éthane Gaz livrés en
bouteilles ou en tubes : propane et butane. Gaz de pétrole liquéfié (GPL) servant de carburant ; c'est un mélange de propane et de
butane. |
1 à 2% |
|
|
40-180°C |
Hydrocarbures de C5(*) à C10 Plus de 100 composés ont été répertoriés
(linéaires et ramifiés, cycliques et aromatiques) : alcanes, cycloalcanes et
arènes |
15 à 30% |
|
|
180°C-230°C |
Hydrocarbures de C11 à C12 Carburant utilisé dans les réacteurs d'avions. Une partie de cette fraction qui n'est pas
utilisée en tant que carburant est "craquée" en alcanes et alcènes
plus simples. |
5 à 10% |
|
|
230°C à 305°C |
Hydrocarbures de C13 à C17 Utilisés comme carburant des moteurs diesel et
comme combustible dans les chaudières domestiques |
5 à 10% |
|
|
305°C à 405°C |
Fuels lourds
et lubrifiants légers (huiles) |
Hydrocarbures de C18 à C25. Les fuels lourds sont après traitement, utilisés
comme carburant dans les gros moteurs diesel lents et très puissants
(bateaux) ou comme combustibles (centrales thermiques ou fours de
cimenteries) ; ce sont des produits à forte viscosité qui doivent être
réchauffés avant utilisation et de densité voisine de 0,920 à 15°C. La
densité est une caractéristique importante ; elle doit être la plus faible
possible pour permettre une décantation rapide de l'eau qui accompagne le
fuel et qui est l'un des traitements qu'on doit lui faire subir avant
utilisation. Les huiles sont paradoxalement appelées huiles
minérales (pour rappeler leur provenance du sous-sol) mais sont bien des
produits organiques puisque constituées de mélanges d'hydrocarbures. Elles
sont essentiellement utilisées comme lubrifiants des organes mécaniques des
moteurs et machines diverses. Il ne faut pas les confondre avec les huiles de
synthèse utilisées aussi comme lubrifiants des moteurs et qui appartiennent à
diverses familles chimiques. |
10 à 30% |
|
405°C à 515°C |
Hydrocarbures de C26 à C38 Les paraffines se présentent sous forme d'un
solide blanc plus ou moins transparent, inodore dont le point de fusion se situe
suivant leur composition entre 35°C et 70°C. Elles constituent un agent
d'enrobage (fruits, confiseries) classé additif alimentaire E905. La vaseline est une substance grasse, molle,
incolore, insoluble dans l'eau, utilisée comme lubrifiant et entrant dans la
composition des pommades. |
Environ 10% |
|
|
Résidus de distillation |
Hydrocarbures de C39 à C40 Ce sont des substances totalement imperméables à
l'eau et ayant un fort pouvoir adhésif. Les bitumes servent à fabriquer des
enrobés répandus sur les chaussées routières (ils sont alors associés à des
granulats et portent le nom d'asphalte) mais aussi à réaliser des chapes
d'étanchéité sur les toitures des bâtiments ou dans les bassins de rétention. |
Environ 15% |
(*)
Les trois hydrocarbures saturés en C 5 ont respectivement pour point
d'ébullition :
- Le pentane 36,10°C
- Le 2-méthylbutane : 27,88°C
- Le 2,2-diméthylpropane 9,48°C
Ils
devraient en toute rigueur être classés dans la première coupe obtenue
(fraction recueillie jusqu'à 40°C) ; en fait on en recueille effectivement une
partie dans la première coupe, mais on en recueille aussi (en solution dans les
autres hydrocarbures) dans la deuxième coupe, celle des essences.
Traditionnellement on dit que le pentane est l'hydrocarbure saturé à la plus
faible masse molaire constituant les essences.
Remarque
: Au-delà de
400°C les fractions
recueillies sont redistillées sous pression réduite ce qui permet un
abaissement des points d'ébullition.
2)
La désulfuration des produits pétroliers
:
Les
pétroles bruts contiennent en moyenne entre 1,5 et 2,5% de soufre.
Il
convient de réduire ce taux dans les carburants et les combustibles afin
d'éviter que le rejet du soufre dans l'atmosphère sous forme d'oxydes
(essentiellement SO2) n'engendre des pollutions telles que les
pluies acides. De plus le soufre est un poison des catalyseurs utilisés dans
les pots catalytiques d'échappements (automobiles) mais aussi dans les
opérations de raffinage.
La
législation européenne évolue et devient de plus en plus draconienne en la
matière ; ainsi en 1994 la limite tolérée était de 1g par kg d'essence et 2g
par kg de gas-oil ; après des baisses successives elle est passée à 10mg par kg
pour les deux types de carburant.
Le
soufre est présent sous forme organique solubilisée, essentiellement des
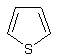
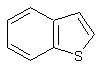
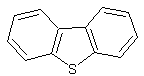
composés thiocycliques (thiophène, benzothiophène ou dibenzothiophène) plus ou
moins alkylés et des mercaptans (thiols) :
|
Thiophène |
Benzothiophène (ou thianaphtène) |
Dibenzothiophène |
Mercaptans |
|
|
|
|
R-SH |
·
Le procédé le plus classique de désulfuration,
consiste à traiter le produit à désulfurer par de l'hydrogène à haute
température (>300°C) et à des pressions de plusieurs dizaines voire
plusieurs centaines de bars (ainsi pour le gas-oil il faut chauffer à 370°C
sous une pression de 60 bars) en présence de catalyseurs, des oxydes
métalliques (principaux métaux : Mo, Co, Ni, Pt, W, Pd) finement répartis dans
de l'alumine.
Les produits soufrés sont dans ces conditions
transformés en sulfure d'hydrogène (H2S) un gaz qui constitue une
source de soufre. Ce procédé est appelé hydrodésulfuration abrégé en HDS.
·
Pour les kérosènes, les gaz livrés en
bouteilles ou le GPL, la désulfuration
consiste à leur enlever les thiols (RSH) qu'ils contiennent, qui leur
donne une odeur nauséabonde et les rend corrosifs. Pour cela on les traite par
de la soude ; les thiols se transforment en thiolates (RSH → RS- )
qui conduisent à des disulfures (R-S-S-R) que l'on élimine par décantation
aqueuse. Cette opération s'appelle l'adoucissement.
·
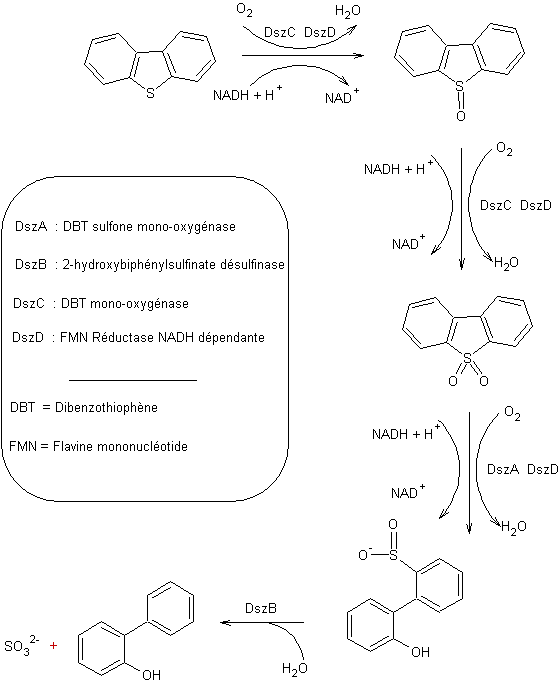
Des techniques de désulfuration
microbiologiques ont été étudiées, utilisant la souche Rhodococcus erythropolis IGTS8 (ATCC n° 53968) ou d'autres,
voisines ; cette souche est capable d'enlever le soufre du dibenzothiophène en
aérobiose par oxydation spécifique du soufre selon une voie métabolique
dénommée voie des 4S ou voie Dsz et l'on aboutit à du 2-hydroxydiphényle et des
ions sulfites.
3)
Craquage (terme anglais "cracking")
:
Les
coupes obtenues lors du fractionnement des pétroles bruts ne correspondent pas,
en général, à la demande. Il y a souvent un excédent de fractions lourdes et
les fractions légères sont produites en quantités insuffisantes. On fait donc
subir aux fractions lourdes (fuels lourds …) des traitements conduisant à la
rupture des longues chaînes carbonées et à la formation de chaînes plus courtes
(essences). C'est ce que l'on appelle le craquage. On parvient à ce résultat
par chauffage en présence d'un catalyseur (craquage catalytique) ou par
chauffage en présence de vapeur d'eau (vapocraquage) ou encore par chauffage en
présence d'hydrogène (hydrocraquage).
On
peut traduire ces opérations en équations en les appliquant à de petites
molécules pour la clarté de l'exposé :
- Craquage catalytique : Les
catalyseurs utilisés sont de type zéolithe (aluminosilicates) cristallisé.
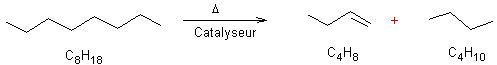
La
rupture de la chaîne ne se produit pas obligatoirement entre C4 et C5 comme
dans l'exemple que nous avons choisi, mais peut se produire entre C1 et C2 ou
entre C2 et C3 ou encore entre C3 et C4.
D'une
façon générale on peut écrire :
![]()
avec
x = y + y'
On
obtient un mélange d'alcanes et d'alcènes constituant une essence.
- Vapocraquage :
C'est
un craquage thermique mais, en pratique, on fait agir de la vapeur d'eau, dont
la pression contribue de façon appréciable à la pression totale de l'opération.
L'expérience montre que ce craquage thermique donne beaucoup de gaz. C'est
pourquoi on en est venu plutôt à un craquage catalytique pour avoir de
l'essence.
Avec
un alcane léger on peut en outre avoir formation de deux alcènes :
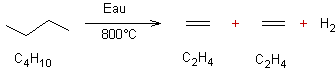
Les
alcènes sont source de très nombreuses synthèses et sont à la base d'une
florissante pétrochimie.
- Hydrocraquage :
Lors
de la désulfuration par le procédé HDS, il peut se produire
un craquage.
4)
Reformage (terme anglais "reforming")
:
C'est
une opération qui s'adresse habituellement aux essences ; elle permet
d'améliorer leur indice
d'octane c'est-à-dire leur qualité en temps que carburant, en augmentant
leur pouvoir antidétonant, c'est-à-dire leur résistance à l'auto-inflammation
par compression ; Les chaînes linéaires sont ramifiées ou cyclisées, la
cyclisation supposant une déshydrogénation.
4-1) Isomérisation :
A
500°C , sous pression et en présence de platine, les chaînes linéaires se
ramifient :
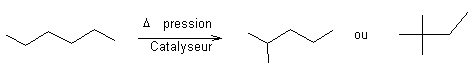
4-2) Cyclisation :
Les
chaînes linéaires se cyclisent et conduisent à des cycloalcanes :
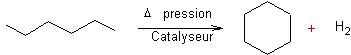
4-3) Déhydrocyclisation :
Un
alcane perd de l'hydrogène et se cyclise pour donner un composé aromatique :
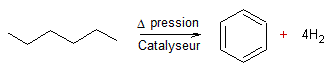
5)
Les débuts de l'industrie pétrolière :
Le
premier forage pétrolier a lieu à Titusville en Pennsylvanie en août 1859 par
l'américain Edwin L. Drake. Le pétrole affleure alors presque le sol, puisque
la profondeur du puits est de 23m. Ce premier forage marque le début de
l'exploitation industrielle du pétrole.
C'est
aussi dans cette région qu'est implantée la première raffinerie des Etats-Unis.
Le saviez-vous : au tout début le raffinage est seulement destiné à recueillir
le pétrole pour lampes d'éclairage (pétrole lampant), le reste étant réinjecté
dans le sol.
6)
Et maintenant des "algo-pétroles"
:
Des
recherches sont menées au niveau des micro-algues pour développer des filières
de production de biomasse et de biocarburant.
Les
micro-algues sont des organismes photosynthétiques unicellulaires intéressants
car en capturant le dioxyde de carbone et grâce à la lumière elles croissent
rapidement et produisent des métabolites intéressants tels que polysaccharides,
pigments et lipides.
Leurs
atouts par rapport aux plantes supérieures est d'avoir un rendement supérieur
(en métabolites transformables en biocarburant), de ne pas être en compétition
avec la production alimentaire ; de plus elles sont très diverses et s'adaptent
facilement à plusieurs milieux.
Leurs
constituants polysaccharidiques permettraient la production de bioéthanol ou de
biogaz et leurs constituants lipidiques les bio-fuels ou biodiesels. On a
calculé que la production de carburants à partir de micro-algues pourrait représenter
20000 à 60000 litres d'huile par hectare, par an, contre 6000 litres d'huile de
palme, un des meilleurs rendements terrestres.
On
donne parfois à ces carburants le nom d'algo-carburants.