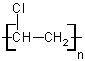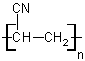LES TEINTURES
Fixation des colorants sur les
fibres textiles
Plan de l'étude :
3-2)
Colorants acides
3-3)
Colorants basiques
3-4)
Colorants réactifs
4-1)
Colorants indigoïdes
4-2)
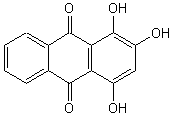
Colorants à structure anthraquinonique
9)
Vue d'ensemble sur la coloration des matières plastiques
10)
Conclusion
La fixation des colorants sur les
fibres textiles :
Il
s'agit le plus souvent de réactions chimiques mais dans certains cas, la
substance colorante peut-être dispersée dans la matière à teindre sans qu'il y
ait de véritables liaisons.
Les
teintures et l'impression relèvent de techniques différentes mais nous
n'aborderons que le point de vue chimique.
Dans
la pratique, il faut prévoir des substances, selon les circonstances, pour
ajuster le pH, rendre le milieu suffisamment ionique, ou des agents
dispersants, etc…
Enfin,
cet article concerne l'utilisation de colorants synthétiques ou naturels dans
des pays aux ressources très diverses.
1) Nature des fibres
:
Pratiquement
la matière à teindre se présente sous forme de fibres, en écheveaux ou tissées.
Si
nous excluons les fibres d'amiante (interdites), les fibres de carbone et les
fibres métalliques (par exemple les fils d'or) pour lesquelles une teinture
n'est, en principe, pas justifiée, on distingue :
·
Les fibres végétales, qui sont
constituées de cellulose : coton, lin, chanvre, jute, ramie, sisal, …..
Chimiquement on est en présence d'une multitude (des milliers) de groupes –OH,
disposés sur un enchaînement à base de
β-D-glucopyrannose-1,4-β-D-glucopyrannose :
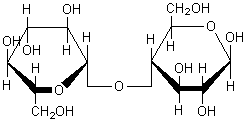
·
Les fibres animales, qui sont de
nature protéinique : laine du mouton et poils d'autres animaux (chèvre,
chameau, lama, alpaga, ….), ainsi que les sécrétions de ver à soie (Bombyx du
mûrier). Chimiquement, on est en présence d'un grand nombre de molécules
reliées les unes aux autres par des groupements peptidiques –CO-NH-. Aux
extrémités de la chaîne, il y a des groupes –NH2 ou –COOH.
·
Les fibres artificielles qui sont –par
définition- des fibres naturelles modifiées : cellulose régénérée (coton
mercerisé, viscose), acétate de cellulose.
·
Les fibres synthétiques, qui sont des
polymères. Ces macromolécules sont élaborées à partir de diverses molécules qui
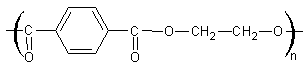
en sont les monomères. Quelques exemples de polymères :
|
|
|
|
|
|
Poly vinyle chloré |
Poly acrylonitrile |
Polyamide |
Polyester (poly téréphtalate d'éthylène glycol) |
|
|
|
·
Nous dirons un mot de la coloration
des fibres de verre.
Pour décrire le comportement des
substances colorantes vis-à-vis du support, il est nécessaire de classer
celles-ci en plusieurs catégories :
¾
Colorants directs :
Il n'y a qu'à mettre le colorant en
présence du support, dans un milieu convenable (solution) :
·
Pour les colorants dits
"substantifs", des liaisons hydrogène ou des liaisons de Van der
Waals suffisent.
·
Pour les colorants acides et basiques,
il s'agit de véritables réactions chimiques acide-base avec des fonctions
présentes sur le support.
·
Avec les colorants dits
"réactifs", il s'établit des liaisons covalentes. La teinture est
très résistante mais ce procédé n'est pas très courant car il met en jeu des molécules
qui ne sont pas très répandues.
¾
Colorants de cuve :
Après mise en présence, il faut laisser se
produire spontanément une réaction chimique sur la fibre retirée du bain (en
pratique une oxydation à l'air) pour que la couleur apparaisse.
¾
Colorants développés :
Après avoir fixé un premier composant sur la
fibre, on ajoute dans le bain, un deuxième composant qui réagit avec le premier
; ainsi, la synthèse du colorant s'effectue sur la fibre elle-même.
¾
Colorants par mordançage :
La fixation du colorant s'effectue
par l'intermédiaire d'un "mordant", espèce qui assure le lien entre
colorant et fibre grâce aux liaisons de coordination qu'il permet de mettre à
profit.
¾
Colorants métallifères :
On met en présence fibre et
colorant, celui-ci étant un complexe d’un ion métallique (Cu2+, Cr3+,
…..) réalisé avec une ou deux molécules organiques. La présence du métal
modifie la couleur due à la molécule organique seule, généralement en la renforçant.
¾
Colorants au soufre :
Il faut dissoudre le colorant dans une solution
de sulfure de sodium (Na2S), puis réaliser une oxydation.
¾
Colorants et pigments dispersés :
Les colorants en solution ou en émulsion et
les pigments – donc des solides- sont introduits et se dispersent dans la
matière à colorer. Il faut souvent ajouter un "véhiculeur" pour
faciliter la pénétration ; les éléments colorants sont simplement emprisonnés.
3-1) Colorants
substantifs :
Le lien entre colorant et matière à teindre
est assuré par des liaisons hydrogène et des liaisons de Van der Waals.
¾
Exemple : avec le bleu de méthylène
sur cellulose ou fibre protéinique
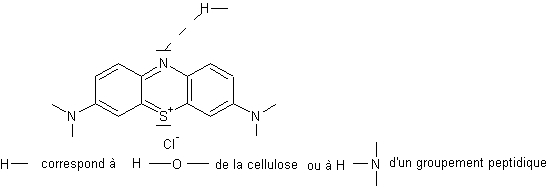
Si on trempe un tissu dans le bleu de
méthylène, il se colore mais, rincé abondamment à l'eau, la teinte a tendance à
disparaître parce que le colorant est entrainé.
En général, ce type d'association est faible
et la teinture n'est pas solide.
¾
Cependant, si les dimensions de la
molécule de colorant sont adaptées à la structure du produit à teindre, on
obtient un résultat convenable. C'est le cas de plusieurs bis-azoïques sur la
cellulose.
La distance des groupes -N=N- dans les
bis-azoïques à groupes immédiatement voisins est 1,08 nm. Le motif
correspondant au cellobiose dans la cellulose mesure 1,03 nm.
Ainsi le rouge congo teint parfaitement la
cellulose car sa molécule s'adapte bien au support comme le montre le schéma
ci-dessous où apparaissent les liaisons hydrogène entre le rouge congo et la
cellulose.
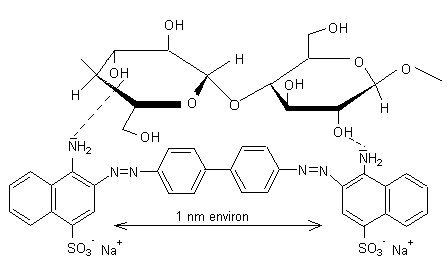
Confirmation : le triacétate de
cellulose ne fixe pas le rouge congo
3-2) Colorants acides
:
Leur molécule comporte une ou plusieurs
fonctions acide ; en solution il apparaît donc des anions
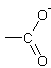 ,
-SO3- , -O- …..d'où leur appellation : colorants
anioniques.
,
-SO3- , -O- …..d'où leur appellation : colorants
anioniques.
Ils forment des liaisons ioniques avec des
supports à sites cationiques, essentiellement –NH3+ et plus
généralement
![]() des fibres
protéiniques ou des polyamides en milieu acide.
des fibres
protéiniques ou des polyamides en milieu acide.
¾
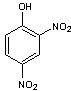
Un exemple qu'on peut souligner est
l'acide picrique :
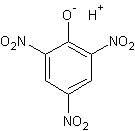
C'est un acide fort.
Il teint en jaune la laine, le nylon, … Il
n'agit pas sur le coton.
¾
On trouve également les groupes  et -SO3-, des substances
à fonction carboxylique, sulfonique, qui favorisent la teinture en tant
qu'adjuvants.
et -SO3-, des substances
à fonction carboxylique, sulfonique, qui favorisent la teinture en tant
qu'adjuvants.
·
On peut citer :
Le bleu acide 45, dérivé anthraquinonique
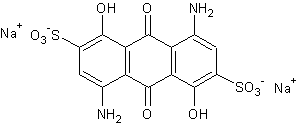
ou le jaune acide 1 dérivé de nitronaphtol
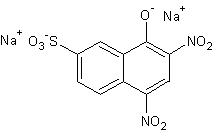
·
La crocétine
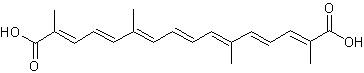
Issue des stigmates du safran (Crocus sativus) très cultivé en Iran, en
Inde, en Grèce, en Espagne, soluble dans l'eau, teint la laine et la soie en
jaune intense et même en orangé car elle est accompagnée de petites quantités
de caroténoïdes voisins. Le safran du cachemire tire davantage sur le rouge.
·
Plusieurs dérivés hydroxylés de
l'anthraquinone, porteurs d'un groupe –COOH, issus des Coccidés (cochenilles),
donnent à la soie des teintes vermillon, écarlate, cramoisi, carmin très
prisées.
L'acide carminique, pour prendre un exemple,
est présent sous forme de sel de potassium d'un glucoside qui ne s'hydrolyse
pas facilement dans les conditions de teinture.
Sur les –NH3+ de la
soie, dans un milieu convenable, on a :
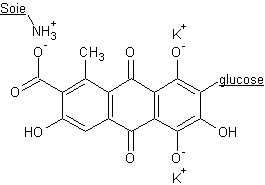
3-3) Colorants
basiques :
Ils comportent des cations d'où leur
autre appellation : colorants cationiques, essentiellement ![]() .
Ils forment des liaisons ioniques avec des supports à sites anioniques,
notamment les
.
Ils forment des liaisons ioniques avec des supports à sites anioniques,
notamment les  terminaux de la laine, de la soie, des
polyamides et aussi les -SO3-, des fibres acryliques
greffées (polyacrylonitrile sulfoné).
terminaux de la laine, de la soie, des
polyamides et aussi les -SO3-, des fibres acryliques
greffées (polyacrylonitrile sulfoné).
¾
Nous trouvons ici les dérivés azotés
du triphénylméthane
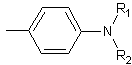 sous la forme
sous la forme 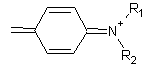 d'un
des noyaux.
d'un
des noyaux.
Il existe toute une série de violets
obtenus avec des molécules comportant plus ou moins de –CH3 sur les
atomes d'azote ; plus il y a de –CH3, plus la teinte est foncée.
Exemple : le violet cristal
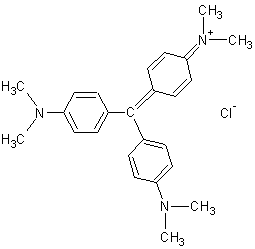
Si on supprime un groupe –N(CH3)2
on obtient le vert malachite :
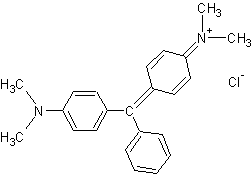
¾
La berbérine est un colorant naturel,
présent dans de nombreuses espèces végétales, notamment les mahonia (famille
des berberidacées) et l'épine-vinette (Berberis
vulgaris), qui permet de teindre très facilement d'un beau jaune.
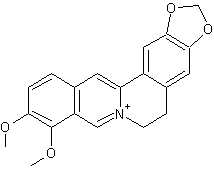
Cation berbérinium
3-4) Colorants
réactifs :
Ils forment, avec le support, de
véritables liaisons covalentes. La teinture est très solide.
Mais ces circonstances sont
exceptionnelles et les formules des composés colorants sont bien particulières.
Il faut que le colorant ait le
groupe vinylsulfone –SO2-CH=CH2 ou le groupe triazine
chloré :
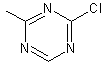
qui sont, en l'espèce, des groupes
réactifs.
Appelons T le reste d'une molécule
comportant un de ces groupes. Traitons de la cellulose Cell-OH, en mettant
symboliquement en évidence l'un de ses multiples groupes –OH.
Les équations mises en jeu sont :
·
Soit
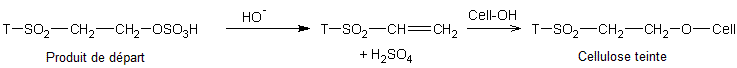
·
Soit
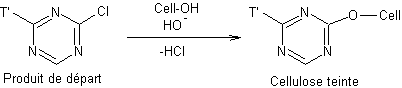
Pour donner une idée de ces
molécules colorantes, nous citerons comme exemple :
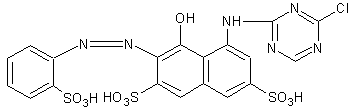
On distingue la molécule chromophore
liée au groupe réactif.
Dans la laine, les sites –NH- et NH2
réagissent comme les –OH cellulosiques. Ce type de teinture se développe, de
nouveaux groupes réactifs voient le jour. Dans les recherches les plus
récentes, les chromophores sont encore le plus souvent azoïques ou
anthraquinoniques mais ils peuvent être liés à des groupes vinyliques
diversement activés ou à d'autres hétérocycles azotés halogénés.
4-1) Il
s'agit essentiellement des colorants indigoïdes.
L'expression "colorants de
cuve", traditionnelle, tient son origine dans le fait que cette méthode de
teinture ne nécessitant pas une température supérieure à 50°C, on s'est servi
de cuves en bois ou en céramique et non de récipients métalliques susceptibles
d'être chauffés. Cette pratique ancestrale a perduré jusqu'à nos jours.
¾
L'indigo
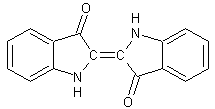
·
On souhaiterait tremper le tissu dans
le colorant en solution mais le problème est que le colorant n'est pas soluble.
Il le devient si on l'a soumis à une réaction de réduction mais il est alors
pratiquement incolore (leucodérivé).
Alors on imprègne le tissu avec la solution
incolore puis on l'expose à l'air. L'oxydation fait apparaître la forme
colorée.
La réduction se fait avec du dithionite de
sodium Na2S2O4
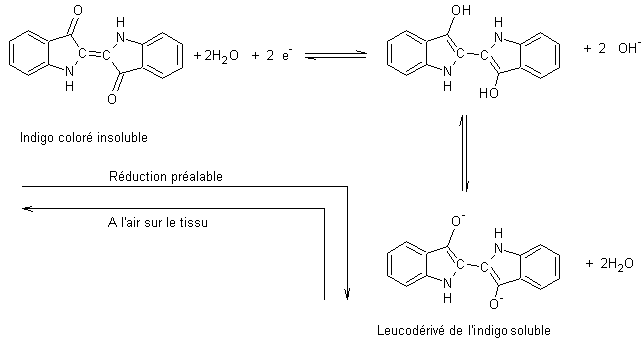
Le système est couplé avec
![]()
pour la réduction, et avec
![]()
pour l'oxydation.
·
Le leucodérivé se fixe sur la cellulose
par liaisons hydrogène. En schématisant la cellulose par cell-OH :
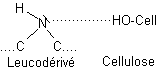
La forme colorée précipite sur et à
l'intérieur des fibres ; grâce à la structure réalisée on obtient une teinture
très résistante ("jeans").
·
Le leucodérivé se fixe sur laine,
soie, nylon par liaisons ioniques. Pour être simple, représentons un élément de
ces diverses fibres par

On s'adaptera aisément à tous les cas suivant
les molécules terminales des chaînes d'acides aminés ou de polyamides
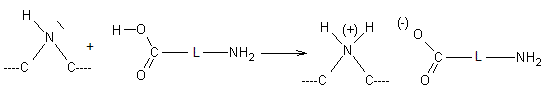
Leucodérivé
¾
La pourpre :
·
C'est une teinte d'un violet tirant
sur le rouge, quelquefois sur le bleu, composée de colorants chimiquement très
proches de l'indigo, obtenue à partir de coquillages des mers chaudes et même
tempérées, les murex et les pourpres. Beaucoup d'espèces atteignent de grandes
tailles, pouvant dépasser 20 cm.
Dans l'Antiquité, autour de la méditerranée,
certaines teintes étaient si prestigieuses que des empereurs s'en sont réservé
l'exclusivité
·
Comme dans le cas de l'indigo, le
précurseur est incolore. C'est un liquide présent dans une glande du mollusque
vivant. Par rapport à l'indoxyle, précurseur de l'indigo, les molécules
comportent en général du brome et du soufre.
Exemple type :
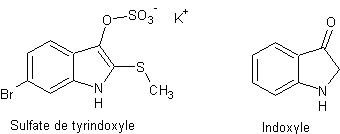
La couleur apparaîtra après extraction du
liquide (il faut casser la coquille), sous l'effet de l'oxygène de l'air et de
la lumière. Il se dégage des gaz nauséabonds (mercaptans R-SH).
On peut obtenir par exemple :
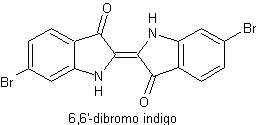
·
Pour teindre, on trempe le tissu dans
une cuve où on a mis à macérer le jus d'un très grand nombre de coquillages, le
plus possible à l'abri de de l'air et de la lumière. On observe le résultat à
la sortie de la cuve ; il y a alors effet de l'air et de la lumière.
On peut encore observer la mise en pratique
de cette méthode dans certaines contrées d'Amérique centrale.
De nos jours on peut obtenir le
6,6'-dibromo indigo par synthèse, à l'échelle industrielle.
4-2) Enfin,
en utilisant des colorants à structure anthraquinonique et des agents
oxydants comme l'eau oxygénée H2O2 pour la dernière
étape, on peut obtenir des teintes très variées.
Exemple : Bleu d'indanthrène
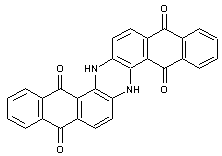
La
partie quinonique de la molécule, par réduction (Na2S2O4,….)
prend une structure phénolique

5)
Colorants développés :
¾
On appelle ainsi des colorants qui
sont synthétisés sur la fibre. En pratique, la synthèse est une copulation avec
un phénol et le colorant est un azoïque :
![]()
- Cette méthode convient bien à la
cellulose. Le β-naphtol est très employé d'où l'appellation "teinture
au β-naphtol" qu'on emploie parfois pour la pratique de la teinture
par colorants développés.
- Le rouge de p-nitroaniline dit
"rouge para" donne de très bons résultats. Les fibres de cellulose
sont trempées dans une solution alcaline de β-naphtol ; il s'exerce des
liaisons hydrogène et des forces de Van der Walls. Puis les fibres sont
retirées, égouttées et trempées dans une solution refroidie du diazoïque de la
p.nitroaniline (le milieu acide transforme le phénate en phénol). Enfin on
rince et on met à sécher. On obtient une belle couleur rouge.
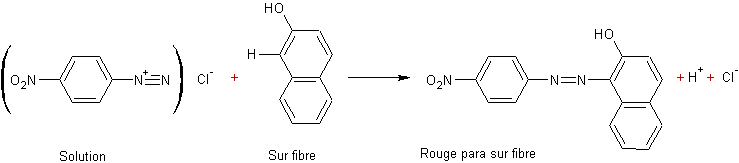
¾
Le colorant apparaît sur la fibre. La
teinture "rouge para" a été très pratiquée dans le passé (torchons).
Mais on peut envisager l'emploi :
v Pour
le diazoïque appelé "développeur" beaucoup de dérivés de l'aniline.
v Pour
la copulation, comme "agents de couplage" des anilides type :
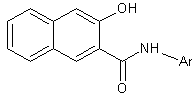
où on voit toujours le groupe β-Naphtol.
6)
Colorants à mordants :
·
Principe :
La fixation du colorant se fait
grâce à la présence d'un intermédiaire : le mordant :
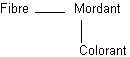
Ces intermédiaires sont de deux types :
·
Soit un ion métallique : Al3+,
Cr3+, Fe3+, ou Fe2+, Cu2+, ….
C'est par chélation que le mordant est relié
à la fois à la fibre et au colorant. Les mordants sont des solutions d'alun,
d'acétate d'aluminium, de sels ferriques, de sels chromiques ; dans ce dernier
cas, ces colorants à mordants, très utilisés pour teindre la laine, sont
appelés "colorants au chrome". On utilise K2Cr2O7
mais c’est Cr3+ qui est présent dans le complexe ; la réduction peut
se faire grâce à l’acide formique (![]() réducteur ) employé pour ajuster le pH.
réducteur ) employé pour ajuster le pH.
·
Soit un polyphénol.
Les liaisons font intervenir les doublets des
atomes d'oxygène, donneurs d'électrons
![]()
Ou encore les hydrogènes
des –OH (liaisons hydrogène).
Remarque : comme ces
substances sont également des tanins, on parle de
"mordançage au tannin".
Le mordançage des fibres peut se
faire avant teinture ou en présence du colorant. En pratique, le choix de la
méthode repose sur diverses considérations : possibilité de réaction, teinte
recherchée (qui ne sera pas forcément
celle du colorant) et maintenant
toxicité de certains éléments (Cr3+).
¾
Mordançage à l'alun :
·
L'alun ordinaire a pour formule Al2(SO4)3,
K2SO4, 24 H2O ou ( AlK(SO4)2,
12 H2O).
C'est le type d'une famille de composés
isomorphes (Mlll)2(SO4)3, MlSO4,
24 H2O.
Il est choisi pour des raisons de commodité
mais l'élément déterminant Al3+ peut provenir de Al2(SO4)3
ou Al(CH3COO)3.
Les composés apportant Cr3+
donnent aussi d'excellents résultats.
·
Expérience utilisant l'alizarine :
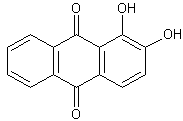
C'est une poudre rouge orangé ; dissolvons-la
dans une solution de soude, on obtient une solution rouge-violet ; ajoutons une
solution contenant Al3+, on obtient un colorant rouge vif
gélatineux.
Les colorants gélatineux sont appelés
"laques".
On peut teindre un morceau de tissu de coton
en le trempant dans cette solution.
On peut écrire, en représentant
schématiquement la cellulose par
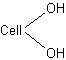 et en milieu alcalin dilué :
et en milieu alcalin dilué :
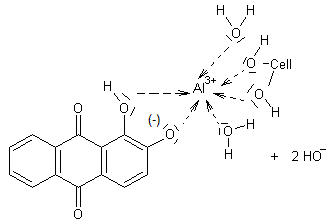
Mais on peut envisager d'autres possibilités
:
-
remplacer les deux molécules d'eau par une autre molécule d'alizarine ou par
deux autres –OH cellulosiques
-
ioniser le deuxième –OH de l'alizarine (soude plus concentrée) d'où un deuxième
![]() .
.
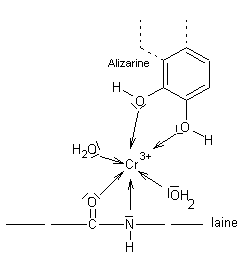
Dans le cas de la laine, qui se teint aussi
très bien, les liaisons covalentes de coordination issues des –OH de la
cellulose sont remplacées par des liaisons issues de l'azote et de l'oxygène
des groupes ![]()
.
·
Enfin l'alizarine
peut être remplacée par toute une série de dérivés hydroxylés de
l'anthraquinone, certains d'ailleurs présents à côté de l'alizarine dans la
racine de garance :
|
|
|
|
|
|
|
|
|
Purpurine |
|
Xanthopurpurine |
Pseudopurpurine |
Rubiadine |
|
|
|
|
|
|
|
¾
Mordançage au tanin :
·
Les tanins sont des polyphénols
présents en abondance dans certains arbres : chêne (notamment dans les galles),
châtaignier, pistachier (pourtour méditerranéen), sumac (Chine, Japon, Laos),
acacia à cachou (versant sud de l'Himalaya, Thaïlande, …..).
·
Certains tanins sont des hétérosides
mais leur hydrolyse libère facilement deux molécules fondamentales. Selon le
cas ces molécules sont :
|
|
|
|
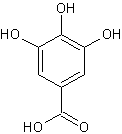
Acide
gallique |
Acide
ellagique |
Par leurs multiples fonctions phénol ou
phénate (en milieu alcalin) ils peuvent produire des chélations ou donner des
liaisons hydrogène, autant de "dents" pour accrocher la cellulose ou
les protéines d'une part et certains colorants d'autre part.
En ce qui concerne la couleur obtenue, on
peut s'en servir pour teindre directement en jaune, roux ou brun.
·
Un deuxième groupe de tanins, présents
dans des plantes, ne donnent pas lieu à hydrolyse. Ce sont des anthocyanes. Par
exemple la gallo catéchine :
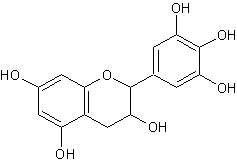
Ils teignent directement, donnant des tons
plus rouges et plus intenses.
·
Ainsi, beaucoup de tanins sont des
mordants mais, ils peuvent aussi apporter eux-mêmes la couleur, tout au moins
dans une certaine gamme.
·
Enfin, l'addition de sels de fer
donne, avec les phénols, des colorants noir, gris, brun (le fer est
probablement complexé) et ces colorants peuvent, eux aussi, se fixer sur les
fibres.
Remarque : tannage
Le tannage des peaux, pour les rendre
imputrescibles et donner des cuirs, peut se faire par action du tanin de chêne
sur les fibres dermiques de la peau, le collagène.
Le fait que le tannage puisse se faire aussi
avec l'alun fait penser à rapprocher mordançage et tannage. Mais on ne compte
pas sur le tannage pour obtenir la couleur définitive d'un cuir ; on fait appel
ensuite, par exemple à des amines aromatiques, notamment l'aniline.
¾
On les a définis jadis comme des
colorants qui se fixent sur les fibres mais qui ne donnent une teinte
définitive stable qu'après avoir été trempés dans une solution de sulfate de
cuivre (CuSO4).
¾
Exemple1 : On peut traiter
des tissus par un colorant naturel jaune à base de flavonols et issu du
"pied d'alouette jaune" (Delphinium
zalil), le kaempférol et des molécules voisines.
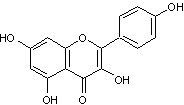
La solution de ce colorant, additionnée de Na2CO3,
donne une teinte jaune d'or ; mais si on ajoute un peu de CuSO4, on
obtient un très joli vert. Le métal se fixe sur ces molécules (flavones,
anthocyanes, ….) par complexation mettant en jeu deux –OH voisins ou un –OH et
un C=O voisins.
¾
Exemple2 :
On trempe un morceau de tissu de coton dans
une solution aqueuse d'un colorant bleu turquoise, la phtalocyanine de formule
:
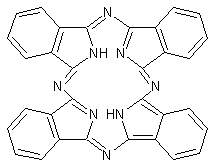
On ajoute du sulfate de sodium et on chauffe
à ébullition. On retire le morceau de tissu, on le rince et on le sèche. Il est
d'un bleu assez clair. Ensuite, on trempe ce tissu dans un mélange en solution
aqueuse de sulfate de cuivre et d'acide acétique. On porte à 80°C pendant
quinze minutes ; puis on retire le tissu, on le rince et on le sèche. Il est
devenu d'un bleu soutenu, il s'est formé de la phtalocyanine de cuivre de
formule :
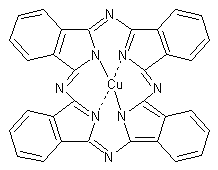
¾ Ces
deux exemples montrent que l’incorporation d’un ion métallique peut modifier
une teinture.
Les
mécanismes de liaison du colorant à la fibre sont de divers types connus :
forces de Van der Waals, liaisons hydrogène, mordançage, colorants acides, …..
Ce
sont des colorants dus à des complexes métalliques.
On
peut considérer en principe qu’avec les colorants métallifères on fait agir un
sel métallique sur un colorant de base puis on traite la fibre ; le colorant
est dit « pré-métallisé » .Alors que dans le mordançage, on traite la fibre avec un sel métallique puis on
ajoute le colorant mais les techniques évoluent .
¾
Exemple d'un colorant azoïque qui a
fixé du chrome Cr3+
Avec
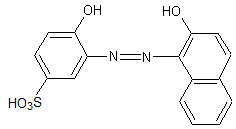
On a :
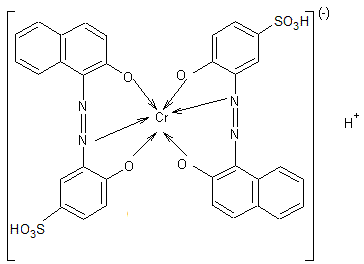
Grâce
à ses groupements –SO3H, ce colorant se fixera sur les parties
basiques de la fibre, par exemple –NH- de la laine.
8)
Colorants au soufre :
8-1) On peut teindre
avec des colorants obtenus par fixation du soufre sur des composés
·
à noyau benzène diversement substitué
(amines aromatiques, dérivés nitrés, phénols, ….)
|
|
|
|
|
·
à noyau hétérocyclique, le plus
souvent azoté
|
Exemple : dérivé de
pyrazine |
|
·
et d'autres encore, à masse molaire
plus ou moins élevée.
Exemple de réaction entre le soufre et une
molécule de ce type
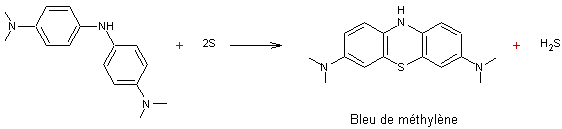
Mais
on constate que le bleu de méthylène ne peut pas servir à teindre les fibres de
façon durable.
8-2) On réserve l'appellation
"colorants au soufre" à des substances organiques soufrées qui
teintent les fibres parce qu'elles ont été retenues au sein de celles-ci grâce
à une insolubilisation.
Ce
sont essentiellement les fibres cellulosiques qui se prêtent bien à
l'opération.
Le
produit de la fixation du soufre sur une molécule appropriée (parfois un
mélange de deux molécules différentes) est insoluble dans l'eau. On peut lui
donner une forme soluble en le réduisant par action du sulfure de sodium en
milieu alcalin. Il est alors apte à être absorbé par la fibre. De ce fait, il
est intéressant d'utiliser, si ce n'est pas le soufre lui-même, des
polysulfures alcalins.
En
effectuant ensuite une oxydation, par l'eau oxygénée ou des composés halogénés
oxydants, le produit devient insoluble et reste emprisonné.
Le
procédé rappelle les colorants de cuve.
8-3) La structure des
colorants obtenus est généralement mal connue. C'est pourquoi ces matières
colorantes sont désignées par la nature de leur(s) composant(s) de départ.
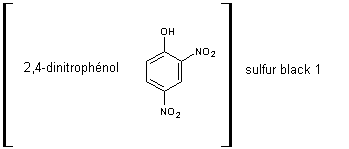
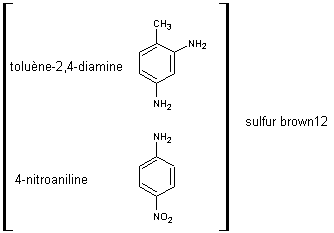
Dans
les colorants au soufre, il peut y avoir des atomes de soufre dans les noyaux
et dans les chaînes.
On
a mis en évidence, par exemple,
|
les
cycles thiazole |
et dibenzothiazinone |
|
|
|
Une
molécule de type Col-SH peut, par oxydation, donner Col-S-S-Col.
9)
Vue d'ensemble sur la coloration des matières plastiques :
Affinité des matières plastiques
– Colorants :
¾
Certaines matières plastiques peuvent
se teindre comme les fibres cellulosiques ou protéiniques à cause de leur
structure moléculaire qui est comparable.
Exemples : acétate de cellulose acétylé à 60%
Polyamides, à rapprocher de la laine et
de la soie.
¾
On peut aussi greffer au polymère des
groupements qui permettront la teinture.
Exemple : polyacrylonitrile greffé avec –SO3H.
¾
Mais s'agissant de liaisons entre
matières colorantes et matières plastiques, on peut dire que, la plupart du
temps, il n'y a pas affinité.
Mise en œuvre de la coloration
¾ Il
peut arriver que la matière colorante soit soluble dans un solvant du polymère.
Exemple : le benzène dissout le polystyrène ;
l'alizarine est également soluble dans le benzène.
On parle alors de colorants plastosolubles.
¾ Le
plus souvent, la matière colorante est insoluble, c'est-à dire qu'il n'y a pas
de solvant compatible ; on a alors à faire à des pigments.
·
On peut employer des pigments
d'origine minérale (oxydes, sels,….).
Quelques exemples :
|
A base de |
Couleur |
|
Ti, Zn |
Blanc (TiO2 des appareils ménagers) |
|
Cd |
Jaune |
|
Co, Mn |
Violet |
|
C |
Noir (noir de carbone des pneus) |
Ils sont stables à la chaleur et aux UV,
conviennent bien pour exposition à l'extérieur.
·
Les pigments de nature organique sont
des molécules plus ou moins riches en doubles liaisons.
Quelques exemples :
|
Nature |
Couleur |
|
Azoïques |
Jaune, orangé, rouge |
|
Phtalocyanines |
Vert, bleu |
|
Dérivés d'oxydation de l'aniline |
Noir |
¾ En
pratique, couramment, colorants liquides ou pigments sont mélangés
progressivement à la matrice polymère à l'état visqueux (avant extrusion le cas
échéant), permettant d'obtenir des objets colorés dans la masse, transparents
dans le cas des colorants, opaques dans le cas des pigments.
Ce sont des matières colorantes
dispersables.
Exemples :
·
Polyéthylène, polychlorure de vinyle,
polyacrylonitrile,….opaques, teintés dans la masse.
·
Plaques transparentes et colorées en
polyméthacrylate de méthyle, polycarbonate,….
¾ Mais
il arrive également qu'on soit amené à mettre en œuvre un
"véhiculeur", molécule capable de rapprocher l'espèce colorante de la
matière plastique, notamment en fils, et de pénétrer entre les fibres pour
favoriser la migration de la couleur. Le véhiculeur, très peu soluble dans
l'eau, est en émulsion et joue le rôle de solvant entre espèce colorante et
polymère. Au cours de la teinture, à chaud, le véhiculeur s'évapore. Au
refroidisement, l'espèce colorante reste emprisonnée.
Exemple : on peut teindre ainsi des
polyesters à l'anthraquinone ou au rouge de paranitroaniline avec le diphényle
comme véhiculeur.
¾ Remarque
: le verre, en blocs, en lames ou en fibres est teinté par dispersion puisque
la masse de verre en fusion reçoit des pigments minéraux divers en fonction de
la teinte à obtenir. Mais dans cette structure cristalline semi-ordonnée de
silicates, il peut y avoir des liaisons chimiques résultant de l'action du pigment
coloré sur les éléments fondamentaux du verre.
10)
Conclusion :
Pour conclure ce sujet sur les
teintures, nous nous appuierons sur deux constatations :
¾ L'élasthane
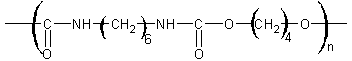
un polyuréthane aux propriétés élastiques
remarquables peut se teindre par la presque totalité des méthodes précédemment
exposées (colorants acides, basiques, réactifs, par mordançage, dispersés).
¾ La
curcumine, issue des rhizomes de curcuma est un colorant extrêmement répandu en
Inde et dans le sud-est asiatique :
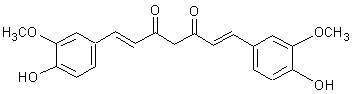
Elle teint d'un jaune éclatant pratiquement
n'importe quelle matière.
Les robes des bonzes en sont un magnifique
exemple.
Au vu des formules, on peut supposer
que différents types de liaisons interviennent.
En teinture, les modes de liaisons
support-colorant ne sont pas toujours bien connus.
Ces techniques, qui sont
ancestrales, gardent encore une partie de leurs secrets.