Plan de l'étude : Plan
général des synthèses
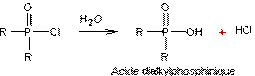
ACIDES
PHOSPHINIQUES ET DERIVES
|
|
·
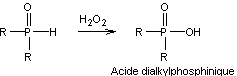
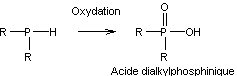
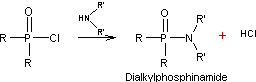
Oxydation des oxydes de phosphines
secondaires ou des phosphines :
ACIDES
PHOSPHONIQUES ET DERIVES
|
|
|
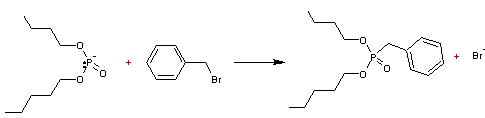
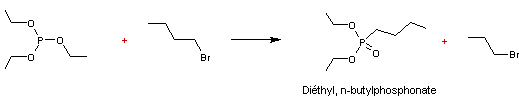
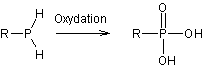
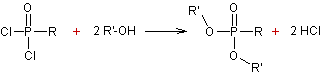
On obtient
un alkylphosphonate.
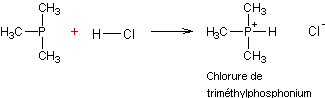
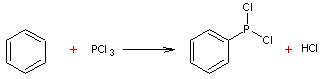
- Substitution des arènes par le
trichlorure de phosphore
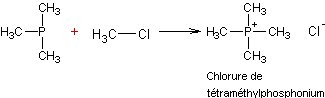
- Halogénures
de phosphonium et phényllithium :
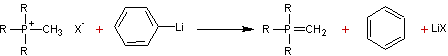
Exemple :
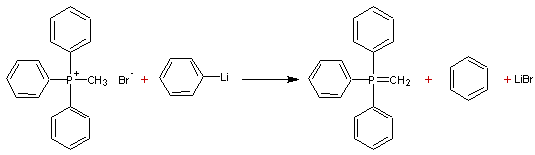
Le
produit obtenu est le méthylènetriphénylphosphorane.
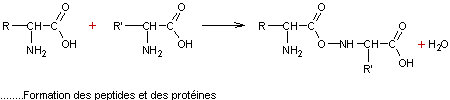
Remarque : Dans
certaines conditions il y a cyclisation avec formation d'azalactone
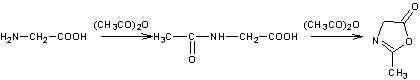
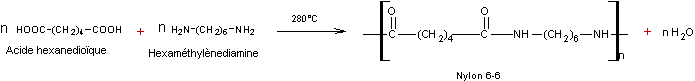
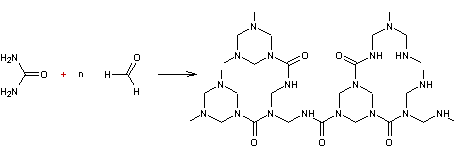
Ce
sont des résines urée-formol.
- Polymérisation
par condensation de mélamine et de méthanal :
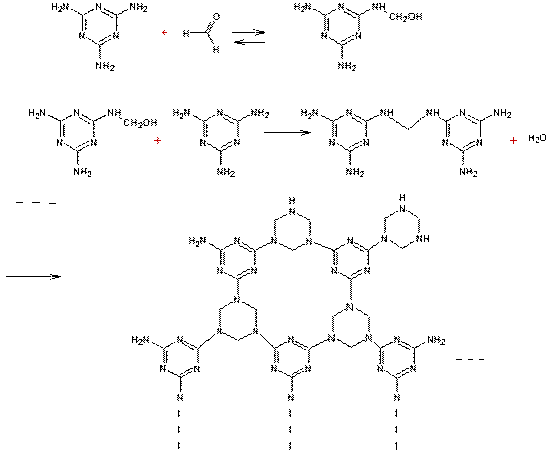
Ce
sont des résines mélamine-formol.
Exemple 1
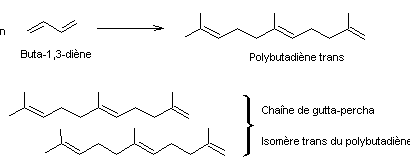
Exemple 2
Réaction de Diels-Alder
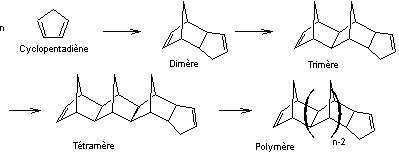
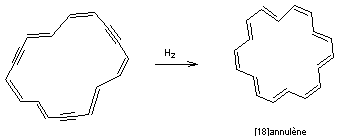
|
Polymérisation
par condensation des anhydrides avec les alcools |

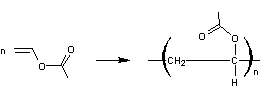
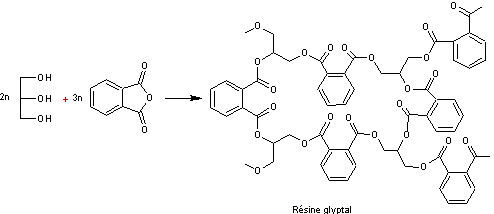
·
Polymérisation par condensation des
esters avec les alcools
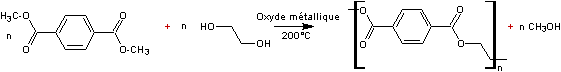
|
|
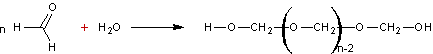
On obtient le paraformaldéhyde qui peut
reconduire au formaldéhyde par chauffage intense.
Si l'on chauffe en présence d'acide dilué
on obtient le trimère :
![]()
Trioxyméthylène
![]()
C'est une cire.
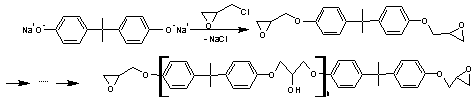
C'est un prépolymère, la résine
diglycidyléther du bisphénol A (DGEBA) :
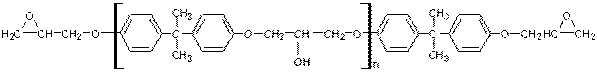
C'est une résine qualifiée d'époxyde ou
même d'époxy.
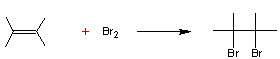
Exemple 1
![]()
Exemple 2
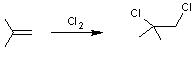
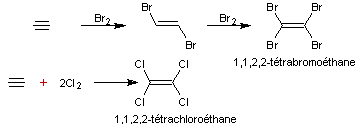
![]()

![]()
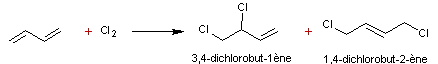
![]()
![]()
![]()
- Electrolyse des acides carboxyliques dans le fluorure d'hydrogène
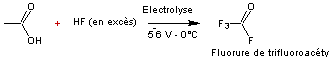
![]()
![]()
![]()
On peut généraliser
![]()
Avec un aldéhyde :
![]()
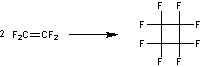
- Polymérisation
par addition de l'acrylonitrile :
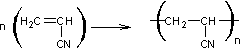
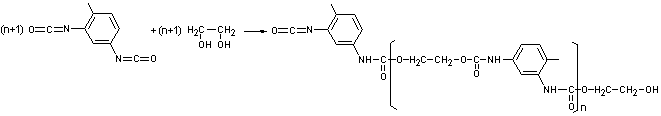
- Polymérisation
par condensation de diisocyanates et d'alcools
- Cycloadditions-1,3
des alcènes
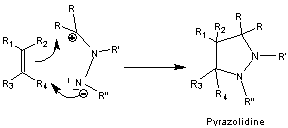
- Cyclisation des hydrazones des cétones α-β-insaturées :

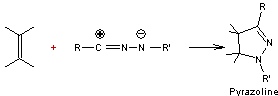

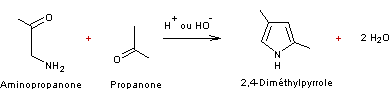
- Condensation des α-aminocétones avec des composés carbonylés (Synthèse de
Knorr)
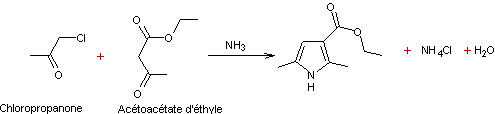
- Condensation des composés α-chlorocarbonylés avec des β-cétoesters et des amines (Synthèse de Hantzsch)
- Condensation des composés 1,4-dicarbonylés
avec l'ammoniaque
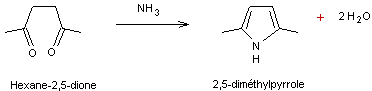
Par oxydation du lactose ou du galactose
on obtient l'acide mucique :
![]()
Le sel d'ammonium de cet acide donne par
chauffage le pyrrole :
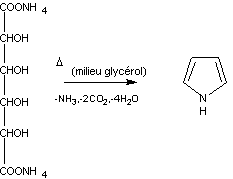
Le pyrrole donne par hydrogénation
catalytique la pyrrolidine.
![]()
Remarque :
L'hydrogénation partielle du pyrrole donne
les pyrrolines ou azolines ou dihydropyrroles :
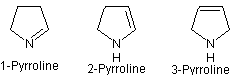
PYRROLINES (ou azolines)
- Cycloaddition
-1,3 des alcenes

- Condensation
des composés carbonylés α-β insaturés avec les arylamines (Skraup)
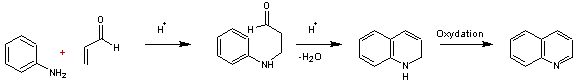
Il s'agit d'une réaction
de condensation d'un aldéhyde ou d'une cétone a,b-insaturé avec l'aniline ou une amine aromatique
primaire ayant une position ortho libre en milieu acide et en présence d'un
agent oxydant.
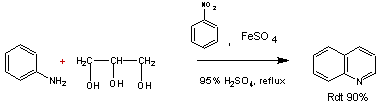
La synthèse de la
quinoléine elle-même peut être menée avec le glycérol comme molécule qui
donnera l'acroléine et le nitrobenzène comme oxydant en présence d'acide
sulfurique (milieu acide) ; le sulfate de fer (II) modérant la réaction qui
peut être violente :
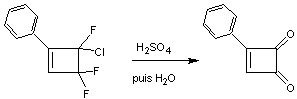
On obtient le phénylcyclobutadiènoquinone,
un solide jaune cristallisé, plus stable que l'orthobenzoquinone.
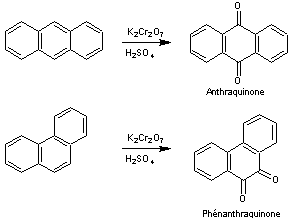
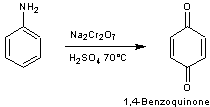
Exemple 1
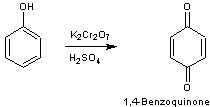
Mécanisme :
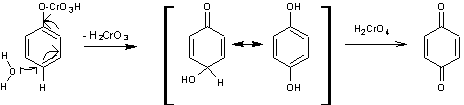
Exemple 2 :
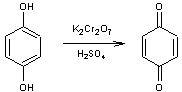
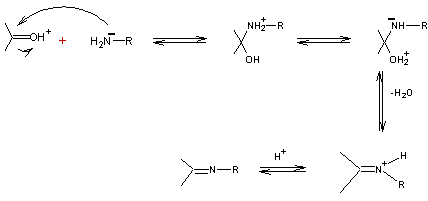
- Condensation
des aldéhydes et des cétones avec des amines I :
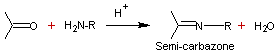
Mécanisme :
Il y a compétition entre deux réactions :
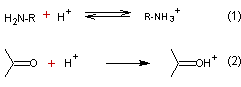
La réaction (1) est nuisible a la suite. Il
faut donc se placer dans une zone de pH telle que la réaction (2) soit
prédominante (pH 3).
Les étapes suivantes sont rapides :