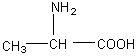
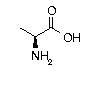
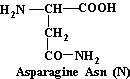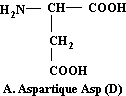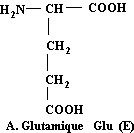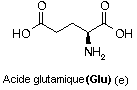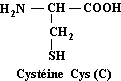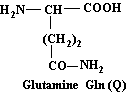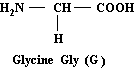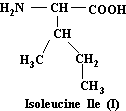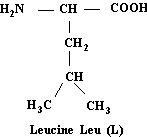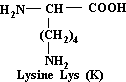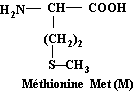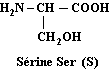AMINOACIDES
C3H7NO2
Masse
molaire :
89,09g.mol-1
Fusion :
297°C
|
Point isoélectrique |
pH =6,00 |
|
pKa du COOH |
pKa=2,33 |
|
pKa du NH3+ |
pKa=9,71 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 16,69
Très
répandue
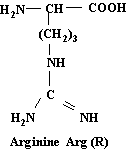
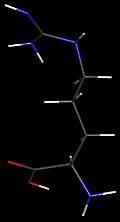
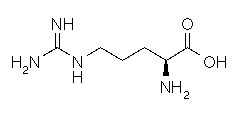
C6H14N4O2
Masse
molaire :
174,20g.mol-1
Fusion :
244°C
|
Point isoélectrique |
pH =10,76 |
|
pKa du COOH |
pKa=2,03 |
|
pKa du NH3+ |
pKa=9,00 |
|
pKa de l'acide conjugué du R |
pKa=12,10 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : très soluble : 18,26g.
Très
abondante dans les histones et les protamines.
En allemand Arginin (1886)
et en français Arginine (1898) ; du radical latin argentum, le nitrate
d'arginine ayant un aspect argenté.
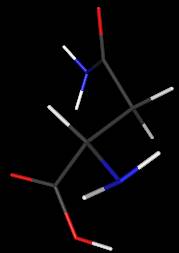
Asparagine
C4H8N2O3
Masse
molaire :
132,12g.mol-1
Fusion :
235°C
|
Point isoélectrique |
pH =5,41 |
|
pKa du COOH |
pKa=2,16 |
|
pKa du NH3+ |
pKa=8,73 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 2,51
Fréquente
dans les protéines basiques des noyaux cellulaires.
La forme
dextrogyre (R) a un goût sucré, alors que la forme lévogyre (S) a un goût amer.
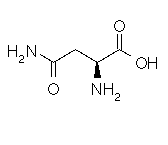
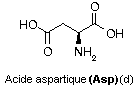
Acide aspartique
C4H7NO4
Masse
molaire :
133,10g.mol-1
Fusion :
270°C
|
Point isoélectrique |
pH =2,77 |
|
pKa du COOH |
pKa=1,95 |
|
pKa du NH3+ |
pKa=9,66 |
|
pKa de l'acide du R |
pKa=3,71 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 0,504
Très
répandu
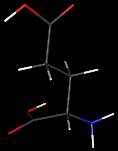
Acide glutamique
C5H9NO4
Masse
molaire :
147,13
g.mol-1
Fusion :
160°C
|
Point isoélectrique |
pH =3,22 |
|
pKa du COOH |
pKa=2,16 |
|
pKa du NH3+ |
pKa=9,58 |
|
pKa de l'acide du R |
pKa=4,15 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 0,86
Additif
alimentaire(E620): exhausteur de goût
Fréquent
dans les protéines.
Bétaïne
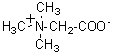
Plus
généralement on donne le nom de bétaïnes aux composés du type:
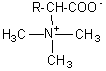
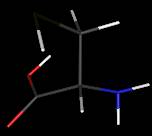
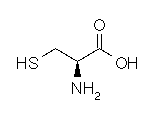
Cystéine
C3H7NO2S
Masse
molaire :
121,16
g.mol-1
Fusion :
240°C
|
Point isoélectrique |
pH =5,07 |
|
pKa du COOH |
pKa=1,91 |
|
pKa du NH3+ |
pKa=10,28 |
|
pKa de l'acide du R |
pKa=8,14 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : très soluble
Structure
secondaire des protéines grâce à sa fonction thiol SH.
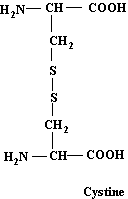
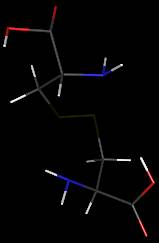
C6H12N2O4S2
Masse
molaire :
240,30
g.mol-1
Fusion :
260°C
|
Point isoélectrique |
pH =5,02 |
|
pKa du COOH |
pKa =1,50 |
|
pKa du NH3+ |
pKa =2,05 |
|
pKa des R |
pKa = 8,80 et 10,5 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 0,17
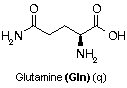
Glutamine
C5H10N2O3
Masse
molaire :
146,14
g.mol-1
Fusion :
185°C
|
Point isoélectrique |
pH = 5,65 |
|
pKa du COOH |
pKa=2,18 |
|
pKa du NH3+ |
pKa=9,00 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 4,2
Transport
et mise en réserve de NH3 et groupes amines.
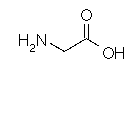
Glycine
C2H5NO2
Masse
molaire :
75,07
g.mol-1
Fusion :
290°C
|
Point isoélectrique |
pH = 5,97 |
|
pKa du COOH |
pKa=2,34 |
|
pKa du NH3+ |
pKa=9,58 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 23,9
Additif alimentaire: E640 : Exhausteur de
goût
Gélatine.
La glycine a
été détectée pour la première fois sur la comète 67P/Tchourioumov-Guérassimenko
par la sonde européenne Rosetta.
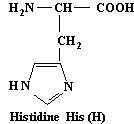
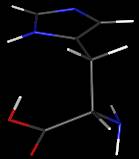
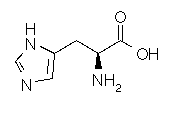
Histidine
C6H9N3O2
Masse
molaire :
155,15
g.mol-1
Fusion :
287°C
|
Point isoélectrique |
pH =7,59 |
|
pKa du COOH |
pKa=1,70 |
|
pKa du NH3+ |
pKa=9,09 |
|
pKa de l'acide conjugué du R |
pKa=6,04 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 4,35
L'histidine a été isolée la
première fois en 1896 par Albrecht Kossel (1853-1927) un médecin allemand qui
l'a découverte dans la sturamine qui est une
protamine issue du sperme d’esturgeon. Le terme
histidine forgé en allemand à partir du grec histion (tissu) est utilisé en
français depuis 1899.
|
Point isoélectrique |
pH =5,82 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 20°C) : 34,5
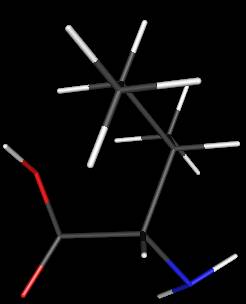
Isoleucine
Acide aminé essentiel
C6H13NO2
Masse
molaire :
131,17
g.mol-1
Fusion :
284°C
|
Point isoélectrique |
pH =6,02 |
|
pKa du COOH |
pKa=2,26 |
|
pKa du NH3+ |
pKa=9,60 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 3,42
Peu
répandue.
L'isoleucine
existant dans les protéines est le stéréoisomère S,S (le premier S étant le
carbone asymétrique n°2). Un autre stéréoisomère peu répandu est épimère du premier (il se rencontre dans
certains peptides bactériens; on le rencontre également dans le sérum ou
l'urine de sujets atteints de leucinose, maladie héréditaire dans laquelle le
catabolisme de l'isoleucine et des autres acides aminés ramifiés est bloqué).
Il n'a pas reçu de nom particulier mais a été désigné par "l'autre
isoleucine", alloisoleucine (en grec allos veut dire
l'autre). Le même cas a eu lieu pour la thréonine.
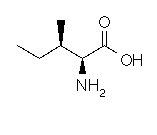
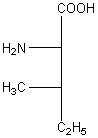
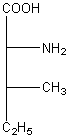
Configurations
absolues de l'isoleucine et de l'alloisoleucine :
|
|
|
|
L-isoleucine |
D-isoleucine |
|
|
|
|
L-alloisoleucine (2S,3R-isoleucine) |
D-alloisoleucine (2R,3S-isoleucine) |
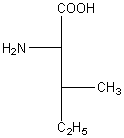
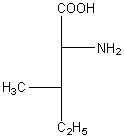
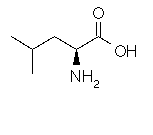
Leucine Acide aminé essentiel
C6H13NO2
Masse
molaire :
131,17
g.mol-1
Fusion :
293°C
|
Point isoélectrique |
pH =5,98 |
|
pKa du COOH |
pKa=2,32 |
|
pKa du NH3+ |
pKa=9,58 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 2,38
Très
fréquente dans dans la plupart des protéines.
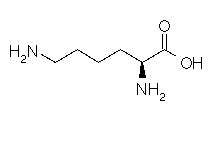
Lysine
Acide aminé essentiel
C6H14N2O2
Masse
molaire :
146,19
g.mol-1
Fusion :
224°C
|
Point isoélectrique |
pH =9,74 |
|
pKa du COOH |
pKa=2,15 |
|
pKa du NH3+ |
pKa=9,16 |
|
pKa de l'acide conjugué du R |
pKa=10,67 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 0,58
Abondante
dans les histones.
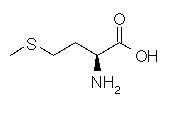
Méthionine Acide aminé essentiel
C5H11NO2S
Masse
molaire :
149,21
g.mol-1
Fusion :
281°C
|
Point isoélectrique |
pH =5,74 |
|
pKa du COOH |
pKa=2,16 |
|
pKa du NH3+ |
pKa=9,08 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 20°C) : 5,6
Peu
abondante; donneuse de groupement CH3 .
La méthionine est un acide α-aminé essentiel, non synthétisé
par l'homme et les animaux ; il faut donc qu’il puisse être puisé dans la
nourriture. Cet acide α-aminé étant présent en faible quantité dans les
céréales, il faut apporter un complément alimentaire à de nombreux animaux. Le
principal débouché de la méthionine (environ 90 % de la production) est
l’alimentation animale, notamment celle de la volaille (2 à 3 g/kg d'aliment,
soit au total 4 à
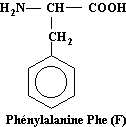
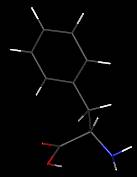
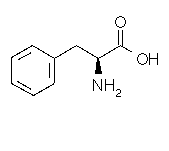
Phénylalanine
Acide aminé essentiel
C9H11NO2
Masse
molaire :
165,19
g.mol-1
Fusion :
283°C
|
Point isoélectrique |
pH =5,48 |
|
pKa du COOH |
pKa=2,18 |
|
pKa du NH3+ |
pKa=9,09 |
Solubilité
dans l'eau au point isoélectrique
(en
g/100g, isomère L, à 25°C) : 2,79
Très
répandue.
Biosynthèse
à partir de l'acide shikimique chez les végétaux supérieurs :
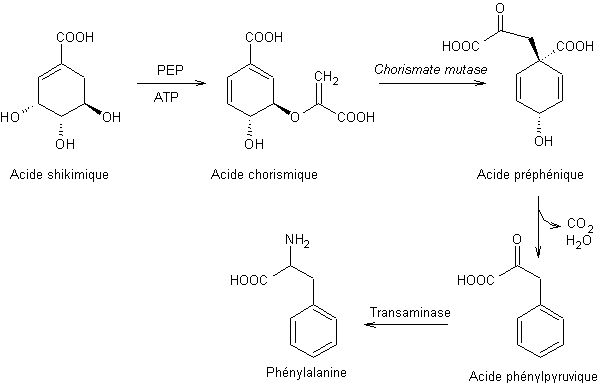
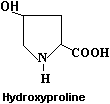
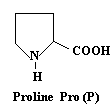
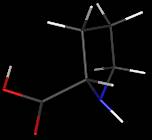
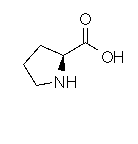
Proline
C5H9NO2
Masse
molaire :
115,13
g.mol-1
Fusion :
221°C
|
Point isoélectrique |
pH =6,30 |
|
pKa du COOH |
pKa=1,95 |
|
pKa du NH3+ |
pKa=10,47 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 162,5
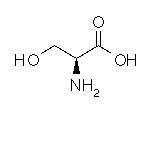
Sérine
C3H7NO3
Masse
molaire :
105,09
g.mol-1
Fusion :
228°C
|
Point isoélectrique |
pH =5,68 |
|
pKa du COOH |
pKa=2,13 |
|
pKa du NH3+ |
pKa=9,05 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 25
Dans
les phosphoprotéines (caséine, jaune d'oeuf).
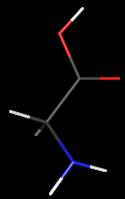
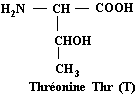
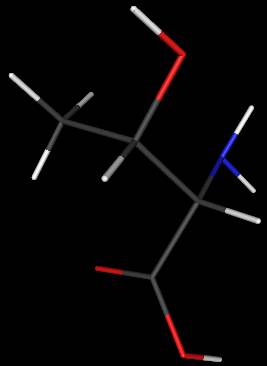
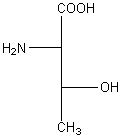
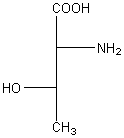
Thréonine Acide aminé essentiel
C4H9NO3
Masse
molaire :
119,12
g.mol-1
Fusion :
256°C
|
Point isoélectrique |
pH = 5,60 |
|
pKa du COOH |
pKa= 2,20 |
|
pKa du NH3+ |
pKa= 8,96 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 9,06
Homologue
supérieur de la sérine.
La thréonine
existant dans les protéines est le stéréoisomère S,R (le S étant celui du
carbone asymétrique n°2). Un autre stéréoisomère peu répandu est épimère du premier. Il n'a pas reçu de nom
particulier mais a été désigné par "l'autre thréonine", allothréonine
(en grec allos veut dire l'autre). Le même cas a eu lieu pour
l'isoleucine.
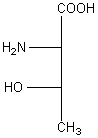
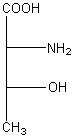
Configurations
absolues de l'isothréonine et de l'alloisothréonine :
|
|
|
|
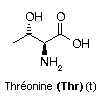
L-thréonine |
D-thréonine |
|
|
|
|
L-allothréonine |
D-allothréonine |
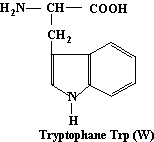
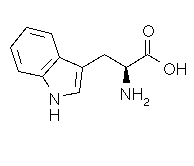
Tryptophane
Acide aminé essentiel
C11H12N2O2
Masse
molaire :
204,23
g.mol-1
Fusion :
289°C
|
Point isoélectrique |
pH =5,89 |
|
pKa du COOH |
pKa=2,38 |
|
pKa du NH3+ |
pKa=9,34 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 1,32
L'isomère
lévogyre a un goût neutre alors que l'isomère dextrogyre est sucré.
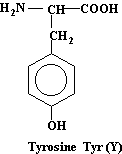
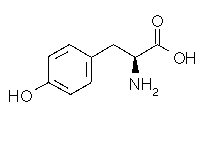
Tyrosine
C9H11NO3
Masse
molaire :
181,19
g.mol-1
Fusion :
343°C
|
Point isoélectrique |
pH = 5,66 |
|
pKa du COOH |
pKa= 2,24 |
|
pKa du NH3+ |
pKa= 9,04 |
|
pKa de l'acide du R |
pKa= 10,10 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 20°C) : 0,051
Son
métabolisme conduit à des hormones et à des pigments.
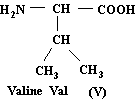
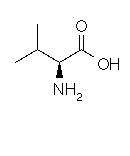
Valine
Acide aminé essentiel
C5H11NO2
Masse
molaire :
117,15
g.mol-1
Fusion :
315°C
|
Point isoélectrique |
pH = 5,96 |
|
pKa du COOH |
pKa= 2,27 |
|
pKa du NH3+ |
pKa= 9,52 |
Solubilité dans l'eau au point
isoélectrique
(en
g/100g, isomère L, à 25°C) : 8,8
En
petite quantité dans toutes les protéines.
|
ACIDES a-aminés "NEUTRES" |
Tyrosine Tyr |
|
Glycine Gly |
Tryptophane Try |
|
Alanine Ala |
ACIDES a-aminés "ACIDES" |
|
Valine Val |
Acide aspartique Asp |
|
Leucine Leu |
Acide glutamique Glu |
|
Isoleucine Ileu |
ACIDES a-aminés "BASIQUES" |
|
Sérine Ser |
Lysine Lys |
|
Thréonine Thr |
Arginine Arg |
|
Méthionine Met |
Histidine His |
|
Cystéine CySH |
ACIDES a-aminés CARBONYLES
|
|
Proline Pro |
Asparagine Asn |
|
Phénylalanine Phe |
Glutamine Gln |