CONFIGURATION ABSOLUE
1) Position du
problème :
Une molécule possédant un carbone asymétrique, a deux énantiomères (+) dextrogyre et (-)
lévogyre (si l'on souhaite les distinguer par leur action respective sur la
lumière polarisée), ou deux stéréoisomères R, S (si on souhaite les distinguer
par la position de leurs atomes dans l'espace). Il n' y a aucune relation
systématique entre ces deux désignations, cela veut dire que pour certaines
molécules, le stéréoisomère R sera (-) et pour d'autres molécules il sera (+)
et de même pour le stéréoisomère S.
exemple :acide lactique
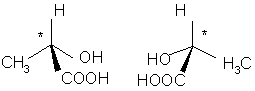
Trouver le type de stéréoisomère (R ou S) auquel appartient une molécule de représentation spatiale donnée c'est rechercher sa configuration absolue. Cela peut se faire en utilisant par exemple la notation de Cahn-Ingold-Prelog .
2)
Notation de Cahn-Ingold-Prelog :
2-1) Classement des substituants d'un
carbone asymétrique :
On
donne un numéro à chaque atome directement lié à un carbone asymétrique (atomes
de rang 1), 1 étant prioritaire par rapport à 2 et ainsi de suite. On attribue
le numéro 1 à l'atome ayant le plus grand Z (numéro atomique); ainsi dans le
cas de l'acide lactique ![]() c'est l'oxygène du OH qui aura le numéro 1 et H
lié au carbone asymétrique le numéro 4.
c'est l'oxygène du OH qui aura le numéro 1 et H
lié au carbone asymétrique le numéro 4.
Si deux
atomes sont identiques (C de CH3 et de COOH dans l'acide
lactique) on compare les atomes portés par ces deux atomes (atomes de rang 2);
celui portant un atome de Z supérieur aura priorité (ici le numéro 2 sera donné
au C de COOH car il porte un O alors que l'autre (CH3)ne porte que
des H ). Si l'indétermination subsiste, on continue...ainsi un COOH aura
priorité par rapport à un CH2OH.
En
cas de double ou de triple liaison on remplace formellement celles-ci par deux
ou trois liaisons simples.
Dans
le cas de l'acide lactique on aura donc:
Z(H)
<Z(C)<Z(O) donc H aura le numéro 4 et O (du OH) le numéro 1.
Pour
les deux carbones de rang 1 il y a indétermination et nous ne pouvons pas leur
attribuer les numéros 2 et 3. On fait donc appel au rang 2:
Pour
le carbone du dessous, l'atome de Z le plus élevé de rang 2 est l'atome
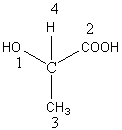
d'hydrogène (Z=1); pour le carbone de droite c'est un des oxygène (Z=8). C'est
donc le carbone de droite qui aura le numéro 2 et le carbone du dessous le
numéro 3. Au total:
Deuxième
exemple: L' orciprénaline
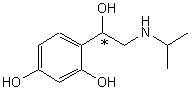 Soit, en décomposant la molécule:
Soit, en décomposant la molécule:
L'oxygène
de rang 1 aura le numéro 1 et l'hydrogène de rang 1 le numéro 4.
Pour
attribuer les numéros 2 et 3 aux carbones de rang 1 il faut aller au rang 2 de
ces atomes:
Pour
le carbone du bas, c'est l'azote de rang 2 qui a le plus fort Z (Z=7); le
carbone de gauche est lié à 3 autres atomes de carbone (Z=6). Il faut donc attribuer
le numéro 2 au carbone de rang 1 du bas et le numéro 3 à celui de rang 1 de
gauche.
Au
total:
Troisième
exemple: Une molécule de
structure voisine de celle de l'orciprénaline
On décompose la
molécule:
Comme
pour le deuxième exemple on attribue à l'oxygène le numéro 1 (Z=8) et à l'hydrogène
le numéro 4 (Z=1). Pour départager les deux carbone de rang 1 il faut examiner
les atomes qui leur sont liés et qui sont dits au rang 2:
Le
carbone de rang 1 du bas est lié à 3 atomes, deux H et un C. C'est le C qui
possède le plus fort Z (Z=6). Le carbone de gauche est lié à 3 atomes de
carbone, donc l'atome de rang 2 de Z le plus fort pour ce carbone de gauche est
aussi un carbone. On ne peut conclure en comparant les deux premiers atomes de
rang 2 de Z le plus élevé pour chaque atome de carbone de rang 1.
On
examine le deuxième atome de rang 2 au Z le plus élevé pour le carbone de rang
1 du bas: c'est un H (Z=1). Pour le carbone de rang 1, à gauche le deuxième
atome au rang 2 qui lui est lié, de Z le plus élevé est encore un carbone
(Z=6). On s'arrête là et on conclut que c'est le carbone de rang 1 de gauche
qui porte le numéro 2.
Au
total:
2-2) Examen de la molécule afin de lui attribuer la
configuration R ou S :
On
représente la molécule en représentation de Cram ; l'observateur regarde dans
l'axe de la liaison C*-4 de C* vers 4; si la rotation 1,2,3 se fait dans le
sens des aiguilles d'une montre, on dit que le stéréisomère observé est R.
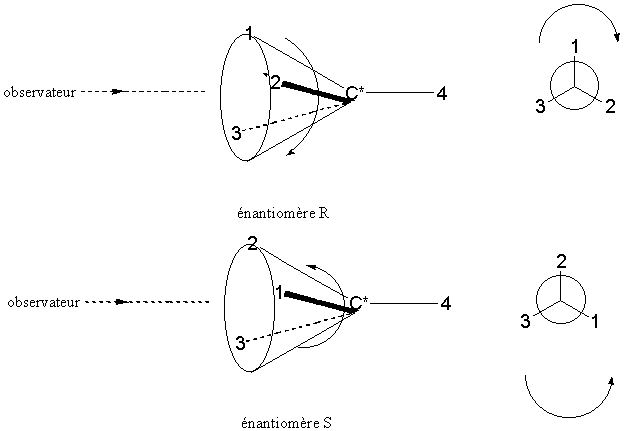
Dans
le cas contraire le stéréoisomère est S.
Remarque
1:En
représentation de Cram 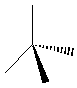 on a intérêt à placer le substituant 4 à l'arrière ce qui permet
de voir facilement dans l'espace dans quel sens il faut tourner pour aller de 1
vers 2 puis vers 3:
on a intérêt à placer le substituant 4 à l'arrière ce qui permet
de voir facilement dans l'espace dans quel sens il faut tourner pour aller de 1
vers 2 puis vers 3:
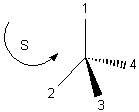
Remarque2: On rappelle qu'il n'y a aucune relation entre la configuration R ou S et le signe du pouvoir rotatoire de l'énantiomère, c'est-à-dire le fait qu'il soit dextrogyre ou lévogyre; autrement dit il existe des molécules R qui sont dextrogyres, et d'autres qui sont lévogyres.
3) Cas
d'une molécule ayant plus d'un carbone asymétrique:
Lorsqu'une molécule possède deux carbones asymétriques, chacun
d'eux peut se trouver dans la configuration R ou dans la configuration S; de
sorte que l'on peut trouver 4 stéréoisomères : R,R
R,S S,R S,S.
R,R
et S,S constituent un couple d'énantiomères; et de même pour les couples
R,S et S,R.
R,R
et R,S ou R,R et S,R ainsi que S,S et R,S ou S,S et S,Rsont des diastéréo-isomères.
Si
le nombre de carbones asymétriques augmente on devine que le nombre de
stéréo-isomères augmente rapidement (pour n stéréocentres on pourra avoir au
maximum 2n stéréo-isomères).
Les
énantiomères seront ceux qui auront une configuration opposée à chaque
stéréocentre.
On
appellera épimères
des diastéréo-isomères qui ne diffèrent qu'au niveau d'un seul stéréocentre.
4) Séparation des énantiomères:
Les
propriétés physiques des énantiomères sont identiques, ce qui rend leur
séparation dans un mélange par des techniques telles que la cristallisation
fractionnée ou la distillation très difficile. La seule différence qu'ils
présentent est le signe de leur pouvoir rotatoire, c'est à dire leur action sur
la lumière polarisée. Toutes les méthodes de résolution sont donc basées sur
cette propriété.
Par
exemple, le mélange racémique de deux acides énantiomères ( R et S) est traité
par une base optiquement active (par exemple R). On obtient deux sels
diastéréo-isomères (R,R et S,R) qui n'ont pas exactement les mêmes propriétés
physiques et que l'on peut séparer par exemple par cristallisation fractionnée,
si ce sont des solides. Après séparation on peut régénérer les acides et
obtenir les énantiomères purs.
Le
schéma général est donc le suivant:
Les
bases organiques les plus fréquemment utilisées dans ces opérations de
séparation des énantiomères sont: La strychnine,
la quinine, la brucine.
ACTION DES STEREOISOMERES SUR LA LUMIERE
POLARISEE