CHROMATOGRAPHIE
1) Généralités
2) Les différentes méthodes chromatographiques
3) Réalisation
d'une CCM
4) Chromatographie
en Phase Gazeuse
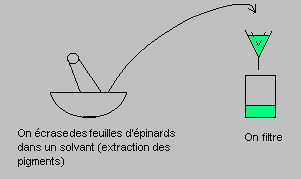
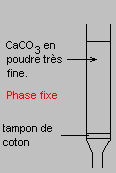
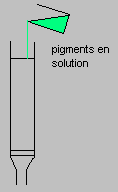
1-1) Expérience de base : TSWETT (1905) réalise une expérience, comparable à la suivante, qui a été le point de départ d'une technique d'analyse aujourd'hui très répandue:
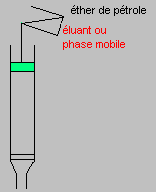

Interprétation
: les pigments verts sont en fait un mélange de pigments de plusieurs couleurs.
En se déplaçant
sélectivement sous l'effet du solvant (ou éluant) au travers
de la colonne, les différents pigments se séparent.
- 1-2) Définitions :
- la poudre, immobile lors de l'expérience, est
appelée phase fixe ou stationnaire.
- le solvant qui en se déplaçant entraîne le mélange
et participe à sa séparation est appelé phase mobile ou éluant.
- 1-3) Généralisation : Dans toute chromatographie (en grec chromato couleur et graphie écriture par référence à l'expérience de TSWETT où l'on détectait les composants grâce à leur couleur) on distinguera :
- une phase fixe,
- une phase mobile.
2)Les différentes méthodes chromatographiques :
- 2-1) Les deux groupes principaux : basés sur la nature de la phase mobile :
- si l'éluant est un gaz: Chromatographie en Phase
Gazeuse (CPG).
- si l'éluant est un liquide: Chromatographie en
Phase Liquide (CPL).
- 2-2) Les sous-groupes : en CPG ou en CPL on pourra distinguer des sous-groupes basés sur la nature de la phase stationnaire :
a)
phase stationnaire: solide doué de propriétés adsorbantes (comme dans
l'expérience de Tswett), on parle de Chromatographie d'adsorption.
b) phase stationnaire: liquide (non miscible à
l'éluant) fixé sur un solide qui sert de support inerte; on parle de
Chromatographie de partage.
c) phase stationnaire: gel constituant un tamis :
Chromatographie par perméation de gel ou d'exclusion.
d) phase stationnaire: résine échangeuse d'ions:
Chromatographie par échange d'ions.
Remarque :
Polarité des phases
On peut faire de la chromatographie :
- à polarité de phase normale : la phase stationnaire
est plus polaire que la phase mobile.
- à polarité de phase inverse : la phase stationnaire
est moins polaire que la phase mobile. La phase stationnaire apolaire est
souvent de la silice greffée avec des alcanes : SiOR avec R souvent une chaîne
alkyle en C18.
Dans la très grande majorité des cas, on fait de la
chromatographie en phase normale.
- 2-3) Quelques détails pratiques :
a) Chromatographie d'adsorption :
La phase fixe est souvent de la silice (en gel), de
l'alumine, des adsorbants organiques copolymères
(vinylbenzène/divinylbenzène), charbon
actif....
b) Chromatographie de
partage :
*Le support peut-être du gel de silice, de la poudre
de cellulose, ou du "papier" (cellulose très pure), ou des polymères synthétiques.
*La phase stationnaire, un solvant polaire ( eau,
solutions acides ou alcalines...)
c) Mode de migration du solvant :
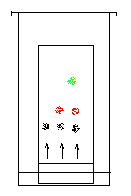 *
le solvant monte : chromatographie ascendante (exemple: Chromatographie en
couche mince) :
*
le solvant monte : chromatographie ascendante (exemple: Chromatographie en
couche mince) :
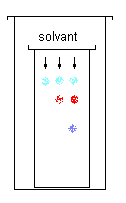 *
le solvant descend : chromatographie descendante (colonne ou papier).
*
le solvant descend : chromatographie descendante (colonne ou papier).
* le solvant migre tour à tour dans 2 directions perpendiculaires avec changement d'éluant : chromatographie bidimensionnelle.
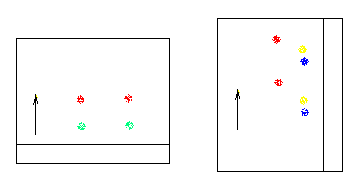 On
fait tourner la feuille de 90°
On
fait tourner la feuille de 90°
d) Révélation des constituants du mélange après séparation:
Rarement les composés sont colorés. Pour les détecter il faut souvent :
- pulvériser un réactif qui colore les taches (ninhydrine pour les amino-acides)
- opérer en lumière U.V. (voir
CCM avec indicateur de fluorescence).
- opérer un comptage de
radioactivité si les composés contiennent des éléments radioactifs.
e) HPLC ou CLHP : Chromatographie Liquide Haute Performance :
C'est une CPL sur
mini-colonnes avec un solide si fin (micronisé) qu'il faut travailler sous
pression (10 à 200 bars) pour que l'éluant puisse les traverser.
3) Réalisation d'une CCM (Chromatographie en couche mince) :
3-1) But: par exemple, vérifier la pureté d'un composé obtenu par
synthèse : le 4-nitroacétanilide obtenu par nitration de l'acétanilide.
Cette
opération conduit à un mélange de 4-nitroacétanilide
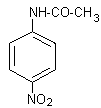
et de 2-nitroacétanilide
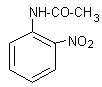 .
.
Par recristallisation dans l' éthanol, on élimine le 2-nitroacétanilide.
On souhaite vérifier l'efficacité de la purification en procédant à une CCM sur
le produit brut et le produit pur.
3-2) Type de
chromatographie utilisée :
Il s'agit d'une chromatographie d'adsorption (la
phase fixe est une mince couche d'alumine déposée sur une plaque d'aluminium)
en phase liquide (l'éluant est un liquide) ascendante (l'éluant se déplace de
bas en haut).
Remarque 1
:La plaque doit être mise dans une cuve à fond plat (un bécher pourra à la
rigueur convenir).
Remarque 2
:L'éluant ne doit pas réagir avec les constituants du mélange. Il est choisi en
fonction de son aptitude à entraîner les substances à séparer : plus
celles-ci sont polaires, plus l'éluant doit lui-même être polaire.
On peut classer différents liquides suivant un ordre croissant de leur
polarité, on définit ainsi une série éluotropique : Ether de pétrole,
cyclohexane, tétrachlorométhane, trichloroéthylène , toluène, dichlorométhane,
éthoxyéthane, trichlorométhane, éthanoate d'éthyle, pyridine, propanone, propan-1-ol,
éthanol, méthanol, eau, acide éthanoïque.
Remarque 3 :
Plus la substance à entraîner est soluble dans la phase mobile plus elle
migrera avec cette phase par capillarité le long du support fixe. On peut
aussi classer par ordre croissant de polarité les groupes fonctionnels : RH,
RX, RNO2, (ROR, RCOOR, RCOR, RCHO), RCONHR, (RNH2, R2NH,
R3N), H2O, ArOH, RCOOH.
3-3) Réalisation :
- On place l'éluant dans un bécher de 250mL (2 à 3 mm en hauteur suffisent) et l'on recouvre le bécher d'un couvercle (de boîte de Pétri par exemple) pour que l'atmosphère se sature en éluant.
Remarque :
composition de l'éluant: éthanoate d'éthyle/méthanol/diéthylamine
(80/10/10).
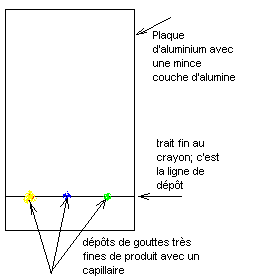
- On prépare la plaque de chromatographie : en aucun cas il ne faut toucher la couche d'alumine. On dispose une feuille de papier filtre sur un coin propre et sec de la paillasse. On place la plaque, couche d'alumine vers le papier filtre.Avec un crayon, on trace sur la face d'aluminium un trait horizontal à 1 cm du bord inférieur de la plaque (sans trop appuyer). Puis avec la pointe du crayon on appuie à 3 endroits sur ce trait (points de dépôt.) pour faire apparaître 3 empreintes de l'autre côté (face alumine).
- Préparation des échantillons : Dans des tubes à hémolyse, dissoudre quelques cristaux des échantillons à tester, dans le solvant. Les concentrations doivent être trés faibles et si possible identiques.
- Le dépôt : On retourne alors la plaque pour que la couche d'alumine soit face à nous ; on plonge un capillaire dans la solution de produit brut dans l'acétone; on vide le capillaire sur le papier filtre pour qu'il ne reste qu'un millimètre de hauteur de liquide; puis on touche un des points de la plaque que l'on avait repéré par une empreinte. La tache faite par le liquide doit avoir au maximum 1 à 2 mm de diamètre; on laisse sécher et on recommence 3 à 4 fois le même dépôt. On procède de même ensuite avec un autre capillaire pour le produit pur dans l'acétone, sur la 2ème empreinte.On recommence de même enfin avec un autre capillaire pour le produit de référence dans l'acétone,sur la 3ème empreinte.
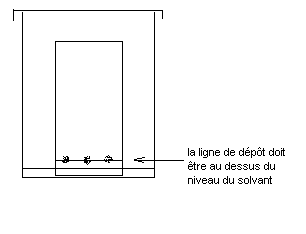
- L'élution : On sèche les 3 dépôts avec un sèche-cheveux, puis on plonge bien verticalement la plaque dans le bécher contenant l'éluant. Lorsque l'éluant est arrivé à 1 cm du bord supérieur de la plaque on repère le front du solvant par un trait de crayon. On sort la plaque et on la sèche très soigneusement.
§ La révélation se fait sous la lampe UV ; la plaque à utiliser doit alors contenir un indicateur de fluorescence ; on utilise couramment deux indicateurs :
- Du
silicate de zinc activé au manganèse dont la fluorescence se produit à 254 nm ;
elle est verte.
- Un autre
pigment minéral dont la fluorescence se produit à 366 nm ; elle est dans le
bleu.
Pour produire ces UV on utilise une lampe à vapeur de mercure et on élimine les radiations inutiles par des filtres.
3-4) Calcul
des Rf :
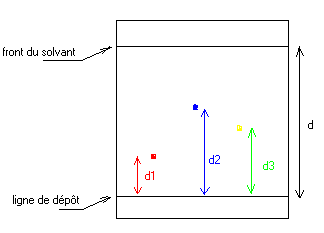
Rf1= d1/d
Rf2 = d2/d
Rf3 = d3/d
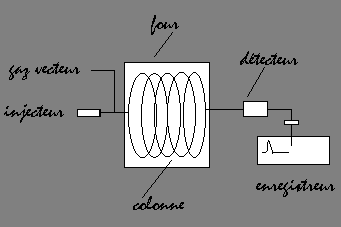
4) Chromatographie en Phase Gazeuse (ou Vapeur) : CPG ou CPV
4-1) Les différents éléments d' un chromatographe :
|
|
|
|
SCHEMA DE PRINCIPE |
UN CHROMATOGRAPHE DE DEMONSTRATION |
- La colonne peut être capillaire (fraction de mm d' épaisseur) ; elle est
remplie d' une phase fixe qui dépend du type de chromatographie que l'on
souhaite réaliser ( d'adsorption ou de partage).
- Le gaz vecteur peut être de
l'hélium, de l'azote, de l'hydrogène .......
- Le four permet de porter la
colonne à une température fixe ou variable (gradient de température programmé)
- L 'injecteur, dans lequel on
envoie le mélange à analyser au moyen d'une microseringue (volumes injectés de
l'ordre de la fraction de mL) est porté à une température supérieure à celle du four.
- Le détecteur peut être, soit de
type cataromètre (2 résistances trés sensibles montées en pont de
wheatstone, avec 2 autres résistances ; l'une est balayée uniquement par le gaz
vecteur, l'autre par le gaz vecteur plus le constituant lorsqu' il lui parvient
; du déséquilibre qui s'ensuit naît le pic observé), détecteur à ionisation
de flamme(FID), .......
- L'enregistreur permet
l'observation des pics et l'édition de l'analyse (traduction en % de la surface
des pics détectés, ainsi que temps de rétention).
- Un intégrateur couplé à
l'appareil permet de calculer la surface des pics détectés.
4-2) Les résultats obtenus
:
Après préparation du
2-méthylbut-2-ène par déshydratation par l'acide phosphorique, on obtient
le chromatogramme ci-dessous qui révèle deux pics, l'un dû au produit préparé
(produit majoritaire) l'autre dû à un isomère formé au cours de la
déshydratation (2-méthylbut-1-ène, produit minoritaire).
- Le temps de rétention
est caractéristique du constituant (dans des conditions données de
température du four et de pression , débit, nature, du gaz vecteur), que
celui-ci soit pur ou mélangé.
- La surface sous le pic
est proportionnelle à la quantité de constituant.
4-3) Un chromatographe de laboratoire :
|
|