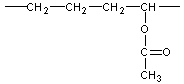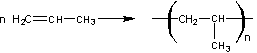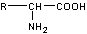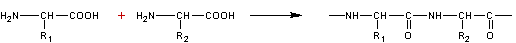POLYMERES
Jacques BARON
avec la collaboration de Gérard GOMEZ
Plan général de cette étude :
A)
Polymérisation par addition ou par condensation :
B) Propriétés générales des substances obtenues :
C) Polymérisations par addition :
D) Polymérisations par condensation :
E) Macromolécules naturelles :
F) Substances macromoléculaires
artificielles,dérivées de macromolécules naturelles :
G) Des polymères dégradables :
H)
Des abréviations :
I) Transfert de chaîne
– Polymérisation vivante
Plan détaillé:
Le XXème siècle fut à bien des égards, le siècle du développement des synthèses
organiques : médicaments, colorants, matières
plastiques.
La
fabrication de ces dernières prit naissance de la nécessité de remplacer les
matières premières et matériaux divers d'origine naturelle dont l'usage allait
sans cesse croissant. Et peu à peu on fabriqua des substances artificielles
ayant certaines propriétés dépassant celles des produits naturels.
Au XIXème
siècle déjà on synthétise des macromolécules artificielles dérivant de
substances naturelles :
- L'ébonite (1839 (Good Year))
obtenue à partir du caoutchouc naturel vulcanisé avec un taux de soufre de 20 à
40%. On obtient un solide dur et cassant de couleur noire rappelant l'ébène
(d'où son nom) qui peut être tourné et poli (fabrication de pipes, disques 78
tours avant les "vinyles", boules de bowling).
- Le celluloïd (1846 Schönbein)
: le nitrate de cellulose (estérification de la cellulose par l'acide nitrique)
dissous dans un mélange alcool-éther en présence de camphre donne une pâte qui
en séchant produit un solide (balles de ping-pong, anciennes poupées).
- La galalithe et le lanital
dérivant de la caséine du lait de vache traitée par le formol ; la galalithe
découverte en 1889 et fabriquée au début du XXème siècle (1905) servait à
fabriquer des montures de lunettes, des peignes, des bijoux, des manches de
couteaux, des boutons, des aiguilles à tricoter… Bien que ce soit une matière
noble, écologique, antistatique, sa fabrication a été abandonnée à partir de
1981.Le lanital permettait de fabriquer des fibres qu'on pouvait tisser et dont
les propriétés se rapprochaient de celles de la laine.
- La viscose ou rayonne inventée
par Chardonnet en 1890,
brevetée en 1892 et fabriquée dès 1924 à partir de cellulose traitée par le
disulfure de carbone en présence de soude concentrée et qui une fois filée se
rapproche des fils de soie ; sa fabrication se poursuit aujourd'hui . La
viscose a servi aussi à fabriquer les feuilles de cellophane (1908).
Parallèlement
se développent les synthèses de polymères indépendants des substances
naturelles :
- La bakélite un phénoplaste
thermodurcissable, mis en œuvre pour fabriquer des objets moulés en 1909 et
breveté en 1935 après sa découverte par L.H. Baekeland, un chimiste américain
d'origine belge.
- Le polystyrène découvert en
1839 mais produit industriellement à partir de 1933 et sous sa forme expansée à
partir de 1944.
- Les caoutchoucs : le Buna en
1936 qui surpasse le caoutchouc naturel par sa solidité et ses possibilités
d'utilisation.
- Les nylons, polyamides obtenus
par condensation, commercialisés en 1938.
- Le PVC découvert par H.V.
Regnault en 1835 et produit aux USA en 1933, en Allemagne en 1935, en France en
1939.
- Le polyéthylène préparé en
1898 par Hans Von Pechmann qui l'obtint par chauffage du diazométhane mais qui n'a été produit industriellement à
partir de l'éthylène qu'en 1939.
- Le Téflon découvert en 1938
aux laboratoires Du Pont de Nemours (New Jersey) qui résiste pratiquement à
tous les agents chimiques, avec un point de fusion élevé ; il est commercialisé
en 1945 et se démocratise dans les années 1960.
- Les silicones : Ils ont été
découverts par Friedel, Crafts et Ladenburg et préparés à
partir de 1904 par Frederic Stanley Kipping (1863-1949) Professeur à Nothingham
(Angleterre) et Walther Dilthey Professeur à Bonn (Allemagne). En France c'est
à partir de 1940 que l'on commence à s'intéresser à la chimie des silicones
(vernis pour l'isolement des bobinages de moteurs électriques) ; mais c'est à
partir des années 1950 que démarrent les productions significatives (graisses
résines, hydrofugeants..).
Puis le
besoin se fait sentir d'inventer des polymères respectueux de l'environnement,
c'est-à-dire biorésorbables et biocompatibles et on a fabriqué les polylactides
(PLA) 1930 ; mais leurs applications notamment en médecine datent des années
1960.
Aujourd'hui
les polymères sont omniprésents : médecine, travaux publics, industries
diverses (automobiles, aérospatiale), emballages, décoration ….. Ce sont des
matériaux de haute technologie pouvant répondre aux cahiers des charges les
plus divers, même les plus contraignants.
Ce rapide
historique, non exhaustif, permet de faire ressortir les étapes décisives qui
ont marqué ces très grands développements tant dans le domaine chimique que
technologique.
L'étude
des principaux procédés de fabrication de polymères ainsi que des familles de
matières plastiques va permettre d'entrer dans cet univers très varié.
A) Polymérisation par addition
ou par condensation:
Polymérisation
par addition
Réaction
d’addition d’un grand nombre de molécules identiques pour donner un composé à
masse molaire élevée.
Exemple 1 : Le poly(chlorure de vinyle)
Le chlorure de vinyle
![]()
ou
![]()
appelé poly(chlorure de vinyle) ; n est l'indice de polymérisation. La
partie entre parenthèses dans la formule étant le motif du polymère.
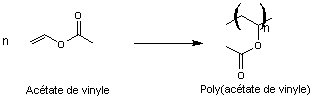
Exemple 2 : Le poly(acétate de vinyle)
Remarque :
S’il y a 2 monomères (très exceptionnellement 3), c’est une copolymérisation :
Exemple :
L' éthylène
CH2=CH2
et l'acétate de
vinyle
![]()
conduisent au polyéthylène vinylacétate
(films étirables).
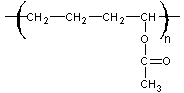
Polymérisation
par condensation
Réaction entre 2 molécules, avec élimination d’une petite molécule
(H2O, HCl,....) qui se répète un grand nombre de fois pour donner un
composé de masse molaire élevée.
Exemple :
Le nylon
![]()
ou
![]()
![]()
ou
![]()
donnent
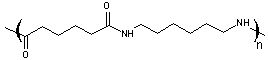
Dans une polymérisation par addition, il y a addition grâce à des
liaisons multiples (composés insaturés).
Dans une polycondensation, il y
a réaction entre 2 groupements fonctionnels (ou 2 atomes) : OH, NH2,
-COOH, Cl.
N.B : Les substances obtenues portent le nom de polymères. Ce
sont des substances macromoléculaires.
B) Propriétés générales des
substances obtenues :
- substances transparentes, translucides, ou blanches.
Remarque : appellation résine, pour certaines
d’entre elles, à cause de leur aspect, mais on peut leur incorporer :
des colorants (au sens strict : teinture par réaction
chimique avec le polymère : azoïques, anthraquinoniques,........Pigments :
solides en dispersion, oxydes minéraux, phtalocyanines,.....)
des plastifiants (pour
assouplir certaines matières dures) : acétates amyliques (les alcools amyliques
sont en C5) ; phtalates amyliques ; " polybenzyle " ;
phosphate de triphényle.
des charges (pour améliorer les propriétés physiques et
mécaniques ou électriques, on disperse des solides : craie, alumine, noir de
carbone, ....)
des stabilisants :
résistance à l’environnement (anti-oxydants : on les trouve surtout dans
les caoutchoucs (C=C) mais aussi dans le polyéthylène, .... ex: phénols,
amines, ....noir de carbone, complexants d’ions métalliques.
des anti-UV, .... souvent C=O conjugué à un cycle
benzénique, mais aussi certains pigments colorés : TiO2, noir de
carbone,...
des ignifugeants : composés organiques chlorés,
phosphates, borates, comme par exemple le phosphate de triorthocrésyle
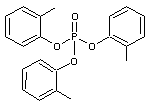
des antistatiques : contre l’accumulation
d’électricité (NH4+ quaternaires, esters de polyols,
poudres métalliques....
des fongicides : thiocarbamates, NH4+
quaternaires...).
des odoriférants.
- Surface lisse
- " légères ": la majorité a une densité
comprise entre 1 et 1,6.
- Inaltérables par de nombreux agents chimiques
- Ce sont souvent de bons isolants électriques.
- Elles se prêtent facilement à des opérations
telles que :
moulage
calandrage (= laminage,cylindres chauffés)
filage et tissage
extrusion (analogue au filage mais avec une filière
plus compliquée qu’un trou circulaire ; on obtient des profilés ex : tuyau)
soudage par pression, à chaud.
- Quelques unes peuvent être expansées, c’est à dire
acquérir une structure alvéolaire, qui en font d’excellents isolants thermiques
et qui sont utilisées aussi pour la protection contre les chocs.
Pour obtenir le produit expansé on fait la polymérisation dans un
solvant très volatil (son départ à l’état gazeux provoque les alvéoles) ou bien
on superpose à la polymérisation une réaction chimique qui produit un
dégagement gazeux CO2, N2).
- Enfin, certaines, par leur consistance ou mises en
solutions dans des solvants appropriés peuvent être le constituant principal de
colles, peintures ou vernis.
Ce sont des matières plastiques:
On peut donner comme définition des matières plastiques :
matériaux artificiels qui, au moins au moment de leur mise en oeuvre, sont
suffisamment modelables sous l’effet de contraintes extérieures (température,
pression,....) relativement faibles, pour être mis en forme avant de se
solidifier.
On distingue :
a) les thermoplastiques, déformables à chaud ; se
solidifient au refroidissement en conservant la forme qui leur a été imposée ;
la déformation ultérieure est possible sous l’influence d’une force ou d’une
élévation de température. La plasticité à chaud correspond à l’existence de
macromolécules linéaires. Lors de la formation, les molécules s’accrochent pour donner un composé n’ayant plus aucune
fonction pour réagir avec les molécules voisines : ex : polyéthylène -CH2-CH2-CH2-CH2-
b) les thermodurcissables : La mise en forme se fait à
chaud par pulvérisation dans un moule et c’est alors que les liaisons avec les
molécules voisines s’établissent. La matière se durcit et toute modification
ultérieure devient impossible. La rigidité à chaud correspond à un édifice
tridimensionnel dans lequel les chaînes sont enchevêtrées.
Ex : résine glycérophtalique (polycondensation glycérol + acide
o.phtalique)
Les thermodurcissables ne sont donc plus plastiques dès l’instant
où ils sont constitués. Mais l’addition de plastifiant supprime leur rigidité.
D’une façon générale la plasticité peut être augmentée par adjonction de
plastifiant; ex : le PVC dur et cassant (canalisations pour l’eau, le
téléphone,....) par adjonction de plastifiant, devient souple (tuyau
d’arrosage).
Les plastifiants agissent :
* dans les thermoplastiques, par simple insertion.
* dans les thermodurcissables, en écartant les groupements
fonctionnels susceptibles de provoquer des liaisons en différents points des
chaînes.
Dans les deux cas, les forces de
cohésion entre les chaînes sont diminuées ce qui explique la souplesse de
l’édifice.
Exemple de plastifiant :
Le phosphate de triorthocrésyle
(TOCP)

Il relie les chaînes
macromoléculaires du polymère par des liaisons moins rigides que celles
initialement présentes.
C) Polymérisations
par addition :
Mécanisme général de ces polymérisations :
Ce sont des réactions en chaîne qui comportent plusieurs étapes:
- initiation
- propagation
- arrêt
Il y a plusieurs types de mécanismes :
**radicalaire :
La première étape s'appelle l'initiation, elle
nécessite un radical A. que l'on obtient grâce à un initiateur (par
exemple le peroxyde de benzoyle)
:
![]()
La deuxième étape s'appelle la propagation.
![]()
La troisième étape est l'arrêt.
![]()
** cationique :
L'initiation nécessite soit un acide fort (acide sulfurique) ou un
acide de Lewis en présence d'eau. C'est H+ qui se forme :
![]()
L'étape suivante est la
propagation :
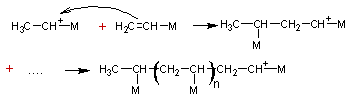
L'arrêt enfin :
![]()
ou
![]()
** anionique :
L'initiation nécessite une base : ion hydroxyde HO-, ion alcoolate RO-,
ion amidure NH2- : on le désignera par M-
Initiation :
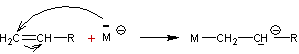
Propagation :
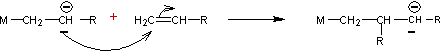
![]()
Arrêt :
![]()
I)Polyoléfines :
1) Polyéthylène
:
Inertie chimique remarquable (structure d’alcane) ; application: flacons
pour produits très divers.
Facilité de mise en forme : feuilles d’emballage, cuvettes moulées
Excellent isolant électrique ; application : gaines pour lignes
électriques.
En fait il existe deux variétés :
polyéthylène " basse densité ", souple, à
chaînes ramifiées, dit "haute pression" (1000 atm, 200°C)
polyéthylène " haute densité ", dur, peu ramifié,
dit "basse pression" (10 atm, 100°C)
Elles sont couramment désignées par les sigles PEbd et PEhd.
2) Polypropylène
(= polypropène)
Ressemble au polyéthylène haute densité ; tissu (Méraklon), cuves
d’accumulateurs, rubans pour cercler les colis.
3) Téflon :
C’est le polytétrafluoroéthylène (PTFE)
Résistance chimique remarquable ; peut supporter 200°C ;
anti-adhérent.
Applications:
- Revêtement
de poêle à frire, de cuves de réacteurs dans l’industrie chimique.
- En
chirurgie, clips vasculaires ; utilisé aussi en orthopédie.
- On peut aussi
citer un tissu à base de PTFE, le Gore-Tex® :
Bill et Bob GORE
père et fils, chimistes américains déposent un brevet en 1969
La membrane imperméable est
"respirante" ; c’est là que réside le principal progrès par
rapport aux tissus synthétiques étanches.
La technologie de la membrane Gore-Tex®
Rappelons deux définitions essentielles :
-
Imperméable : étanche aux liquides, mais laisse filtrer l’air et la vapeur
d’eau plus particulièrement celle produite par les mouvements du corps. On
parle alors de « respirabilité ».
-
Etanche : la membrane ne laisse pas passer la vapeur d’eau produite par
les mouvements du corps ; cette vapeur d’eau vient se condenser au niveau
de la membrane et l’humidité reste au contact du corps.
La membrane de téflon étiré comporte une multitude
de très petits pores.
Un milliard quatre cents millions de pores au
centimètre carré d’un diamètre de 0,2 micromètre. Selon les techniques de mise
en œuvre le nombre et la dimension des pores sont variables.
Les pores sont 20000 fois plus petits qu’une goutte
d’eau ; mais 700 fois plus grands qu’une molécule d’eau à l’état gazeux.
Cette structure microporeuse permet de laisser
passer la vapeur d’eau produite par le corps d’où la
« respirabilité » mais d’arrêter l’eau à l’état liquide venant de
l’extérieur d’où l’imperméabilité. La dimension des pores permet de favoriser
la « respirabilité » ou l’imperméabilité.
On mesure l’imperméabilité d’un tissu en Schmerber,
cela correspond à la pression à partir de laquelle le tissu se laisse traverser
par l’eau. L’ordre de grandeur de l’imperméabilité d’une membrane Gore-Tex® est
1500 Schmerber
1Schmerber =1 mm de colonne d’eau= 10 Pa=0,1mbar
On mesure la « respirabilité » d’un tissu
donc sa capacité à évacuer la vapeur d’eau
par son indice RET. (Resistance Evaporative Transfert)
Plus l’indice est faible plus le vêtement est
respirant ; un vêtement d'indice inférieur à 12 est respirant, au-delà de 20 il
est non respirant. L'indice RET du Gore-Tex® varie entre 2,5 et 6 RET.
II)Caoutchoucs artificiels :
Les élastomères : Ce sont
des substances qui sous l'effet de la traction subissent un allongement
important (seules sont intéressantes celles dont les dimensions peuvent
tripler) qui cesse quand l'action mécanique cesse.
Le caoutchouc naturel extrait du latex de l'hévéa est le
polyisoprène, l’isoprène étant le 2-méthylbutadiène
![]()
Le motif du caoutchouc naturel :
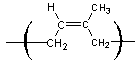
correspond à un enchaînement (Z) 1,4 de
l'isoprène.
La polymérisation du 2-méthylbutadiène peut aussi se faire par
enchaînement (Z) 1,4 en utilisant du lithium métal finement divisé ou des
catalyseurs de type Ziegler (tétrachlorure de titane et trialkylaluminium).
Le (E) 1,4-polyisoprène appelé gutta-percha a des propriétés
différentes du caoutchouc naturel (plus dur et cassant). Contrairement à
celui-ci qui a une structure amorphe, le gutta-percha, du fait de son
enchaînement (E), a une structure semi-cristalline.
1) A
partir du butadiène :
* copolymérisation avec le styrène :
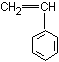
donne le SBR (Styrène Butadiène Rubber) utilisé pour la
fabrication des pneus de tourisme.
Gomme styrène-butadiène (SBR)
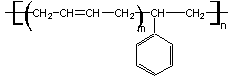
Suivant le nombre d'unités
butadiène et styrène on aura un caractère élastomère plus marqué (avec une
grande majorité de butadiènes) ou thermoplastique plus marqué (avec une grande
majorité de styrènes).
* copolymérisation avec
l’acrylonitrile :
![]()
donne le caoutchouc nitrile particulièrement résistant à l’essence
et à l’huile ; application : tuyaux de distribution d’essence.
* seul, le polybutadiène n’est pas
très intéressant, mais mélangé à du caoutchouc naturel, à du polyisoprène de
synthèse ou à du SBR, il sert à faire des pneus très résistants pour gros
engins.
2) A
partir de l’isobutène :
copolymérisé avec quelques % d’isoprène
![]()
donne le Butyl, particulièrement imperméable aux gaz ; application
: chambres à air.
3) A partir du chloroprène :
On obtient le Néoprène....

résistant aux frottements, au soleil,aux solvants ; ne propage pas
la flamme.
Application: gaines électriques, courroies, combinaisons
de plongée, pâtes élastiques pour l’étanchéïté, colle (colle au néoprène).
A cause de ces nombreuses doubles liaisons, la qualité des
caoutchoucs se perd au fil du temps.
III) Polymères vinyliques :
Le groupement vinylique est CH2=CH-
1) Polychlorure de vinyle : (ou
chlorure de polyvinyle ou PVC)
Le chlorure de vinyle est un gaz qui se polymérise spontanément
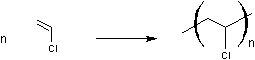
Rigide mais facile à plastifier, ses applications sont nombreuses:
on utilise surtout son aptitude à donner des profilés : fils
(tissu Rhovyl), tuyaux pour l’écoulement des eaux.Utilisé aussi en médecine
(poches de sang, cathéters).
C’est un bon isolant électrique (gaines de fils électriques) ; on
l’utilise aussi pour des revêtements de sol (gerflex), pour imiter le cuir
(skaï), en peinture (peinture vinylique).
2)
Poly(acétate de vinyle) :
Le
poly(acétate de vinyle) s'obtient par
polymérisation d'un monomère, l'acétate de vinyle.
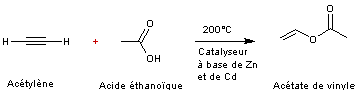
L'acétate de
vinyle s'obtient, lui, industriellement de deux façons :
* soit par action de l'acétylène
en excès sur l'acide acétique à 200°C avec des catalyseurs à base de zinc ou de
cadmium
*Soit par acétoxydation catalytique de l'éthylène en présence d'acide
acétique et d'oxygène ; le catalyseur est du palladium (Pd) déposé sur de
l'alumine et dopé par l'acétate de potassium.
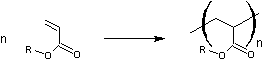
La
polymérisation de l'acétate de vinyle :
Application : colle
blanche ; spécialement efficace sur les matériaux poreux.
Remarque : L’hydrolyse du polyacétate de vinyle fournit le poly(alcool vinylique)
ou alcool polyvinylique (PVA), intermédiaire dans la fabrication d’autres matières plastiques :
les polyacétals.
![]()
Ce polymère n'est pas obtenu par polymérisation
d'un monomère insaturé, mais par hydrolyse d'un autre polymère, le poly
(acétate de vinyle) :
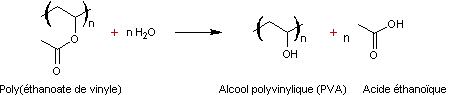
Ceci tient au fait que l'alcool
vinylique n'est pas stable ; c'est sa forme tautomère l'éthanal qui l'est :
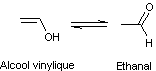
IV) Polymères styréniques :
1) Polystyrène
: ou PS
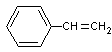
encore appelé styrène. Sa polymérisation
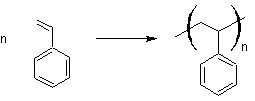
Il se prête très bien au moulage ; on en fait de nombreux objets
moulés, généralement blancs (pots de yaourt).
Il se prête bien à l’expansion, on obtient le polystyrène expansé,
aux qualités isolantes (thermiques) remarquables (glacières portatives) et est
très utilisé également pour la protection contre les chocs (emballage
d’appareils fragiles).
Remarque : On expanse les polymères par dégagement
d'un gaz au sein de la matière, ce qui forme des bulles ou cellules :
* par
vaporisation d'un liquide dissous( par exemple du pentane dissous dans le
polystyrène et dégagé par chauffage).
* par
injection d'un gaz inerte au sein d'un polymère fondu, par exemple dans une
extrudeuse (mousse de polyéthylène).
* par
décomposition d'un composé chimique dispersé dans la masse, comme
l'hydrogénocarbonate de sodium qui en se décomposant par la chaleur donne des
bulles de CO2 (principe de la levure chimique dans un gâteau).
* par
réaction chimique comme celle d'un isocyanate sur l'eau dans la fabrication de
certains polyuréthanes :
![]()
On trouve dans le commerce :
- le PS "cristal" qui est un homopolymère amorphe,
dur et cassant. Il est thermoplastique ce qui est un avantage et transparent (boîtes,
corps de stylos à bille, pipettes incassables).
- le PS "choc" qui est constitué d'une phase
polystyrène dans laquelle sont noyés des nodules de polybutadiène qui sont
capables d'absorber une partie de l'énergie d'un choc éventuel. On l'utilise
pour fabriquer le corps de certains appareils électroménagers.
2) Poly(styrène,acrylonitrile)
: ou SAN
Transparent comme le polystyrène mais plus résistant aux chocs.
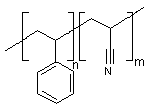
3) Poly(acrylonitrile,
Butadiène, Styrène) : ou ABS
Il est constitué de poly(styrène,acrylonitrile) greffé sur du
polybutadiène. Comparable au SAN mais plus résistant au choc et plus souple.
Utilisé dans l’industrie automobile (calandre, tableau de bord),
dans l’équipement ménager (corps d’aspirateurs), pour faire des jeux de
construction (Lego).
C'est un produit de choix pour les imprimantes 3D.
V) Polymères acryliques :
Ce sont des polymères dérivant de l’acide acrylique CH2=CH-COOH
1) Polyméthacrylates :
- de méthyle : ou PMMA
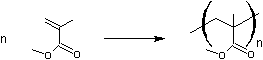
On obtient facilement un produit très transparent.
C’est un verre organique (plexiglas); pour cette raison, on l’utilise
en optique (verre de lunettes, lentilles de contact rigides, cristallins
artificiels).
On
obtient le PMMA par polymérisation radicalaire
du méthacrylate
de méthyle
ou MMA. Le procédé de
polymérisation a été découvert dès 1877 par les chimistes allemands Fittig
et Paul. Un autre chimiste allemand Otto Röhm a breveté en 1993 la marque
Plexiglas.
- de 2-hydroxyéthyle :
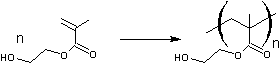
Utilisé pour faire des lentilles de contact souples.
2) Polyacrylates
:
Application : peinture acrylique
Le polyacrylate de sodium :
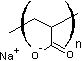
absorbe 800 fois sa masse en eau distillée, 300 fois sa masse en
eau du robinet et 60 fois sa masse en sérum physiologique (0,9% NaCl) ; c'est
ce qu'on appelle un polymère super absorbant et qu'on désigne par le sigle SAP
(Super Absorbent Polymer).
|
|
|
|
Avant absorption de l'eau |
Après absorption de l'eau |
Il est utilisé comme absorbant dans les couches jetables qui en
contiennent environ 15g (soit un pouvoir absorbant de 900g d'urine environ).
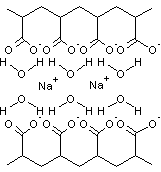
Le polyacrylate de sodium enserre les molécules d'eau qui sont
retenues par attraction électrostatique comme indiqué ci-dessous et forme un
gel :
Applications :
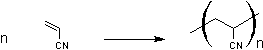
Fibres textiles (Crylor...).
Fibres de carbone :
Le polyacrylonitrile est un précurseur
pour l'obtention de fibres de carbone (annexe 1)
Les utilisations soit directement sous forme de fibres soit sous
forme de matériau composite fibre de carbone-carbone sont nombreuses :
raquettes de tennis, cannes à pêche, bâtons de ski, clubs de golf, vélos, pales
d'éoliennes, renforcement du béton, pièces d'avions (freins, empennages,
volets), pièces de voitures (freins de voitures de formule 1) ; on l'utilise en
chirurgie (prothèse de hanche par exemple)....
4) Adhésifs cyano-acryliques :
Le
cyanoacrylate de méthyle
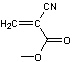
est un
monomère qui se polymérise très rapidement en présence d'un nucléophile
(souvent HO-) pour donner une colle très résistante :
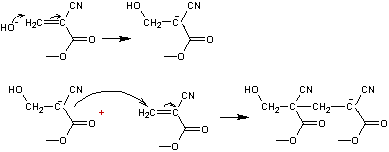
- Utilisation de ces adhésifs :
Superglue
® est une dénomination très connue de ce type d'adhésif. Ils sont très résistants
et à prise très rapide ; ils ont des usages industriels et domestiques.
Les
colles cyanoacryliques sont susceptibles de convenir à tous les matériaux sauf
le téflon. Dans les cas difficiles, polyéthylène par exemple, il faut ajouter
un activateur spécifique.
Le
cyanoacrylate de 2-octyle (Indermil®, Dermabond®, etc.) a trouvé des
applications médicales, il permet dans certains cas d'éviter l’usage de fils ou
d’agrafes pour suturer les plaies.
D) Polymérisations
par condensation :
I) Polyamides :
Caractérisés par la répétition du groupement peptidique -CO-NH-
qui résulte de la condensation, d’un acide carboxylique et d’une amine :
-COOH + H2N- ![]() -CO-NH- +
H2O
-CO-NH- +
H2O
1) Nylon
:
1-1) Le nylon
6-6
L' acide adipique
HOOC-(CH2)4-COOH
et l' hexaméthylènediamine
H2N-(CH2)6-NH2
condensés à 270°C et 10 atm donnent un polymère :
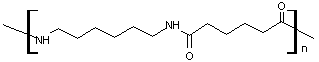
dont le motif (entre crochets dans la formule ci-dessus) est :
- HN-(CH2)6-NH-OC-(CH2)4-CO-
Cette structure rappelle celle de la kératine des poils (laine) et celle
de la fibroïne de la soie. On peut
faire des fils de nylon remarquablement tenaces (~ acier), résistants à
l’usure, au froissement et qui prennent la teinture----> tissus.
On les utilise aussi en chirurgie ; Les fils de
suture en polyamides sont des monofils non résorbables, mais une hydrolyse
progressive peut se produire qui diminue leur résistance dans le temps.
Ils
sont utilisés pour des fermetures cutanées mais aussi en neurochirurgie en
microchirurgie et en ophtalmologie.
La résistance au frottement et au choc du nylon 6-6 permet d’en
faire des pièces mécaniques (engrenages).
NB: ce nylon est le polyamide 6-6 (amine à 6C et acide à 6C); le
mot " nylon " qui est une marque, remplace souvent polyamide.
1-2)
Le nylon 6
On
fabrique couramment un autre nylon, le polyamide 6 dont le motif est -(CH2)5-CO-NH-
Le
caprolactame est un lactame (amide cyclique) à 7 atomes dans le cycle
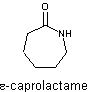 Il est
utilisé aussi
Il est
utilisé aussi
Il
peut se polymériser par ouverture de cycle (POC) et conduit à un polymère le
nylon 6
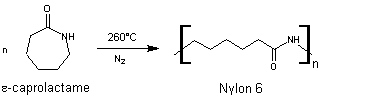
Très utilisé à la sortie de la guerre comme fibre
synthétique (Perlon ®) pour fabriquer notamment des bas, le nylon 6 est aussi
utilisé en chirurgie pour des fils de suture en association avec le nylon 6-6
ou seul ; les domaines d'application étant les mêmes que ceux du nylon 6-6.
2) Rilsan
:
Par polymérisation de l'acide 11-amino-undécanoïque,
H2N-(CH2)10-COOH
![]()
provenant de l’huile de ricin, on fabrique le polyundécanamide 11
(ou polyamide11)
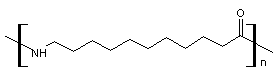
dont le point de fusion est aux environs de 184°C et dont on fait
un textile, le Rilsan ®.
3) Polyaramides :
Couramment appelés "aramides" ; ce
sont des polyamides comportant des noyaux aromatiques.
L’aramide le plus connu est le Kevlar ® obtenu en 1973 en condensant
l'acide téréphtalique
![]()
et le p.phénylènediamine
![]()
on obtient
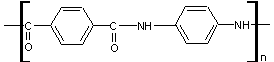
Sa résistance mécanique et à la chaleur est supérieure à celle du
nylon ; la résistance mécanique est même supérieure à celle de l'acier, mais
inférieure tout de même à celle des fibres de carbone. Cela est dû au fait
qu'il possède une structure cristalline ; en effet, il existe de nombreuses
liaisons hydrogène entre les chaînes polymères, elles sont bien alignées,
régulières et orientées.
C'est aussi un très bon isolant électrique.
On en fait des amarres de navires, des gilets pare-balles…..
Les aramides comme le Kévlar sont des para-aramides.
On connaît aussi des méta- aramides ; par exemple avec l'acide
adipique
![]()
et le m-xylènediamine :
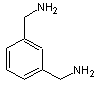
On obtient:
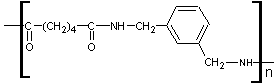
Elles constituent des fibres textiles légères et résistantes.
II) Polyesters :
Ils comportent la répétition de la fonction ester.
1) Polytéréphtalate
d’éthylène glycol : ou PET
L' acide téréphtalique et le glycol conduisent à un polymère, le
poly(téréphtalate d'éthylène glycol).
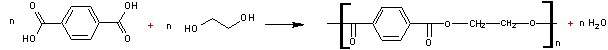
Les applications de ce polymère sont nombreuses : textile
(Tergal®) ; ruban support d’enregistrement audio et vidéo (cassettes), feuilles
d’emballage conservant l’arôme (café), bouteilles de boissons gazeuses.
Il est aussi
utilisé en chirurgie sous forme de fils enduits de silicone ou de téflon pour
certaines sutures.
2) Résines glycérophtaliques :
Exemple :
L'acide orthophtalique
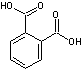
et le glycérol
![]()
ou
HO-CH2-CHOH-CH2-OH
donnent:
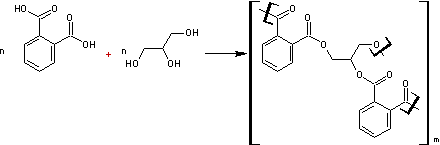
On obtient un réseau réticulé tridimensionnel.
L'état de ces substances les rend particulièrement aptes à être
utilisées dans des vernis et des peintures.
Remarque :
On a donné à de telles macromolécules le nom de glyptals (glycérophtalique)
et plus généralement, avec d'autres alcools (alkohol en allemand)
et d'autres acides (acid) le nom d'alkydes.
3) Polyesters insaturés :
Exemple:
![]()
et l'acide
o.phtalique

avec le glycol
HOCH2-CH2OH
donnent :

le polymaléophtalate d’éthylèneglycol.
Le plus souvent on leur incorpore de la fibre de verre.
Application : éléments de carrosserie, coque de bateaux.
III) Polycarbonates : ou PC
Le chlorure de carbonyle (COCl2) avec un diphénol (le bisphénol A) conduit
à un polymère transparent, résistant aux chocs. Applications: panneaux de
balcons, luminaires :
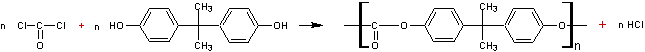
Ce même polymère (le poly(carbonate de bisphénol A)) peut
aussi s'obtenir en faisant réagir le bisphénol A sur le carbonate de diphényle
selon l'équation :
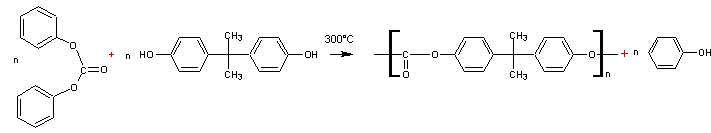
Voir différentes
synthèses des polycarbonates
IV) Phénoplastes :
Ils résultent de la polycondensation d’un phénol et d’un aldéhyde.
Leur élaboration comporte trois stades A, B, C. Ils sont
fluides dans l'état A, pâteux à chaud dans l'état B, durs et infusibles dans
l'état C après que les résines aient été mélangées à des charges (poudre de
bois) à des plastifiants et des pigments puis aient été chauffées et
comprimées.
Exemple : résine Phénol-Formol (méthanal) = bakélite ; ce nom
vient de son inventeur : L.H.Baekeland
(1863-1944), chimiste belge puis américain qui l'a obtenu en 1909.
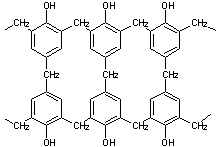
On obtient des matières dures (plastiques thermodurcissables), de
couleur sombre, à propriétés isolantes avec lesquelles on fait des objets
moulés (queues de casseroles), des supports de circuits imprimés, des résines
échangeuses de cations (type phénoplaste sulfoné).
Globalement on peut considérer qu'il s'agit d'une élimination
d'eau entre deux cycles benzéniques et une molécule d'aldéhyde ; l'existence de
trois endroits réactifs sur la molécule de phénol (en ortho et en para par
rapport au OH) permet la formation d'un réseau complexe tridimensionnel
(résine) dont la représentation ci-dessus n'est que partielle.
Le mécanisme implique tout d'abord, la formation d'un alcool
hydroxybenzylique :
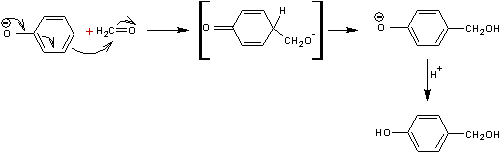
La seconde étape est la condensation de cet alcool avec une molécule
de phénol, en para ou en ortho du OH phénolique :
![]()
par le mécanisme suivant :
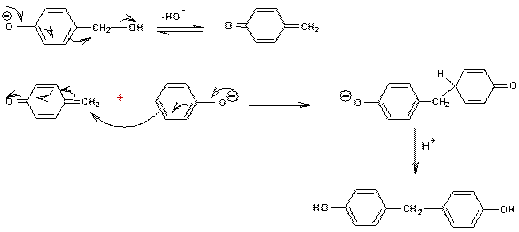
et ainsi de suite...
V)Aminoplastes :
Ils résultent de la polycondensation du méthanal (formol) H2C=O
avec des composés à groupement -NH2. Mêmes propriétés que les
phénoplastes mais teintes très claires, faciles à colorer.
Remarque : à l’origine on a fabriqué la galalithe
(boutons), par action du formol sur la caséine du lait
(la caséine comporte des fonctions amine)
1) Résine urée-formol :
l’urée a pour formule CO(NH2)2 ; condensée
avec le méthanal on obtient en première étape :
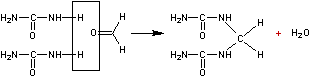
puis progressivement un réseau tridimensionnel serré :
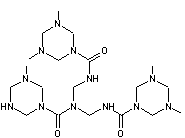
Applications : colle à bois, panneaux de particules
agglomérées.
2) Résine mélamine-formol :
L’amine est la mélamine :
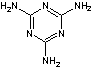
On obtient :
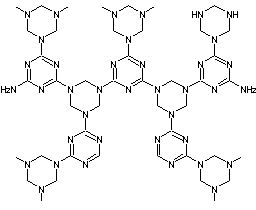
Applications : revêtements stratifiés (formica), résines
échangeuses d’anions (type hydroxyde d’ammonium quaternaire), colles avec
durcisseur.
VI)
Polyéthers :
1) Polyéthers "simples"
-R-O-R-O-
Ils résultent de la polycondensation de diols
ou de la polymérisation d’aldéhydes
Exemples :
- le
polyoxyméthylène -CH2-O-CH2-O-
….
Sigle POM
C'est un des plus importants.
Il est obtenu par polymérisation du formol (méthanal).
C'est un auto-lubrifiant ; il atténue les bruits. Application : galets
anti-bruit.
Il est résistant au dépôt de microorganismes. Application :
hachoirs à viandes, raccords d’adoucisseurs d’eau.
- le polyéthylèneglycol -CH2-CH2-O-CH2-CH2-O-
…
Sigle PEG
En théorie HO-CH2-CH2-OH HO-CH2-CH2-OH à -(O-CH2-CH2-)n-O-
En pratique, on réalise l'addition de l'oxyde d'éthylène en
utilisant de l'éthylène glycol pour la réaction d'initiation
![]()
puis chaque addition d'une molécule d'oxyde d'éthylène allonge la
chaîne :
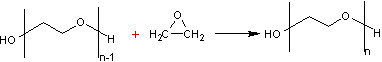
Applications diverses :
Le PEG est utilisé comme gélifiant, mais aussi comme hydratant
dans les produits cosmétiques (crèmes, shampooings..).
En pharmacologie, on rend les liposomes furtifs dans les nanomédicaments en les
entourant de "filaments de PEG".
On peut donner comme exemple les polysulfones (PSU)
Ce sont des polymères thermoplastiques.
Exemple : L'Udel ®

Ce sont des polymères connus pour leur dureté et leur stabilité à
haute température.
On en fait des membranes poreuses semi-perméables utilisées dans les
applications basées sur le phénomène d'osmose.
On les utilise notamment pour fabriquer les membranes
d'hémodialyse.
VII)
Polymères époxydes :
Résines dont l’obtention est basée sur la chimie des époxydes.
Rappelons qu'un époxyde (ou oxirane) est une molécule contenant un
"pont oxygène" entre deux carbones adjacents d'une molécule :
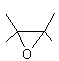
La première étape est la
formation d'un prépolymère par condensation polymérisation du sel de sodium du
bisphénol A avec l'épichlorhydrine en présence de soude :

Le degré de polymérisation de ce prépolymère est faible (n compris
entre 5 et 12 unités).
La résine (polymère tridimensionnel) s'obtient ensuite par
réaction des oxiranes avec une triamine comme par exemple la diéthylène
triamine (NH2-CH2-CH2-NH-CH2-CH2-NH2).
La réticulation se fait de la manière suivante :
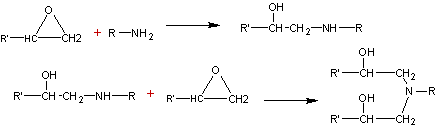
On obtient aussi :
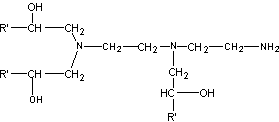
Avec R' qui représente :
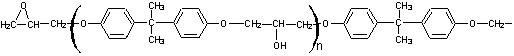
L’appellation " polyépoxyde " n’est pas heureuse, car il
n’y a pas répétition d’un motif issu d’époxyde seulement. L’appellation "
époxyde " entraîne la confusion avec l’un des monomères.
Applications : revêtement intérieur de boîtes de
conserves.
On peut aussi utiliser cette synthèse en deux parties pour réaliser
des colles aux propriétés adhésives remarquables : la colle "époxyde" ,
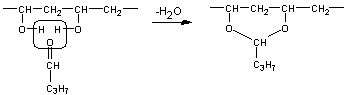
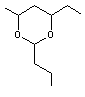
VIII) Polyacétals :
Un acétal :
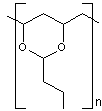
Les polyacétals sont des acétals de polyvinylalcool et d’aldéhydes ; les
aldéhydes utilisés sont l’aldéhyde formique (méthanal), l’aldéhyde acétique
(éthanal), l’aldéhyde butyrique (butanal).
Ex: polyvinylbutyral
Il est transparent et
adhère très bien au verre. Application : pare-brise feuilleté.
ou
Le polymère s'écrivant alors :
IX) Polyuréthanes :
Résultent de l’action d’un di-isocyanate sur un diol
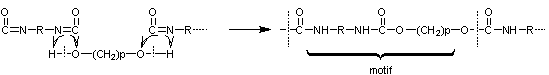
Remarque : c’est une polycondensation sans élimination.
On fabrique couramment le polyuréthane pour lequel p=4 et R est le
toluène :
![]()
Le 4,4'-diphénylméthane diisocyanate (ou 4,4'-MDI)
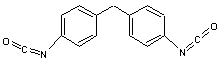
est aussi très utilisé.
Applications :
En médecine : cathéters, pompes cardiaques.
Sous la forme expansée : matelas mousse.
Une application très connue est l'élasthanne
® :
![]()
Mis au point par le scientifique Joseph C. Shivers
de la firme américaine DuPont dans les années 1960 l'élasthanne a été un
évènement dans l'industrie textile. Thermoplastique, très élastique, cette
fibre a été introduite d'abord dans les vêtements de sport (maillots,
justaucorps, collants….), puis dans l'ensemble des vêtements dès les années
1980.
La surface des vêtements en élasthanne est très lisse et
résiste au développement des champignons ; cette fibre ne perd pas son
élasticité aux basses températures et n'entraîne pas d'allergie contrairement
au latex.
Elle
se teint très facilement.
X) Polyimides :
Rappel de la
fonction imide :
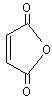
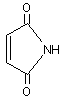
A l'anhydride
d'un diacide, par exemple l'anhydride maléique :
correspond
l'imide :
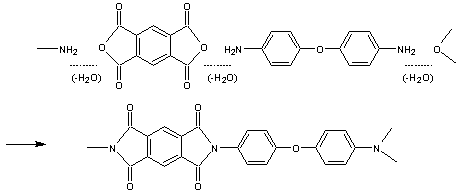
Les polyimides
résultent de la polycondensation d'un dianhydride de tétracide avec une
diamine.
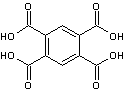
En prenant
l'acide benzène 1,2,4,5- tétracarboxylique
et la
4,4'-oxydianiline
on obtient :
Ces matières plastiques ont la propriété de résister au frottement
et à l’échauffement (400°C) pendant un temps très long.
Remarque :
La présence d'une fonction éther donne de la
flexibilité, ce qui facilite la mise en œuvre .
En pratique, il s’agit de polyétherimides (PEI).
Applications: pièces d’amortisseur de wagons, supports
des connexions de circuits électroniques (échauffement lors de soudures).
Le Kapton
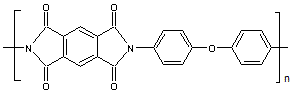
est couramment utilisé en impression 3D car il adhère facilement
aux polymères utilisés dans ce domaine.
XI) Silicones :
Les
silicones découverts par Friedel, Crafts et Ladenburg, furent préparés à partir de 1904 par Frederic Stanley
Kipping (1863-1949) Professeur à Nothingham (Angleterre) et Walther Dilthey
Professeur à Bonn (Allemagne) ; ils utilisèrent le procédé de Grignard. L’ importance des silicones fut reconnue aux Etats-Unis
pendant la seconde guerre mondiale ; James Franklin Hyde Ingénieur et Eugene
George Rochow Professeur à Cambridge (Massachusetts) mirent au point, la
fabrication industrielle. Rochow trouva pratiquement en même temps que Richard
Müller Professeur à la faculté technique de Dresde un procédé de synthèse des
monomères conduisant aux silicones. La synthèse de Rochow et Müller est
toujours d’actualité.
- Le Silicium, tétravalent comme
C, peut remplacer celui-ci dans la constitution d’édifices organiques; il
existe, en particulier, des silanediols :
![]()
- Les
silicones sont des polymères (polysiloxanes) obtenus par déshydratations
intermoléculaires du diméthylsilanediol (ou dihydroxydiméthylsilane)
![]()
cette molécule dérivant elle-même du dichlorodiméthylsilane :
![]()
Le schéma de synthèse des silicones peut se résumer par la
suite de réactions ci-dessous :
![]()
![]()
![]()
Si l’on veut isoler le diméthylsilanediol il faut opérer en
milieu neutre et en forte dilution.
La dernière étape est une polymérisation par déshydratation
en milieu acide ou basique du diméthylsilanediol :
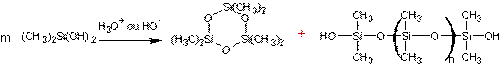
Le silicone étant
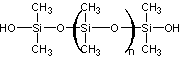
Ces synthèses ne sont pas aisées à mener et les rendements de
la deuxième et de la quatrième étape sont assez faibles. Les polymères ainsi
obtenus sont dits linéaires.
Les polymères linéaires sont liquides et ont une viscosité
qui dépend de la longueur des chaînes. Ils restent fluides à basses
températures et sont très stables à la chaleur.
Ils ont une remarquable inertie chimique, la liaison Si-O
leur conférant une excellente résistance à l’oxydation et à l’hydrolyse.
Ils sont également résistants aux radiations, aux agents
atmosphériques.
Ils sont étonnamment stables thermiquement et utilisables de
-50°C à +250°C sans modification de leurs propriétés ; ils
diffèrent, en cela, de la plupart des autres matières plastiques.
Les silicones sont d’excellents isolants électriques,
insensibles à la chaleur et à l’humidité.
Les caoutchoucs aux silicones restent élastiques entre -80°C et
+320°C; on en équipe des avions de haute altitude.
On les utilise comme fluides hydrauliques.
Ils sont hydrofuges et servent à enduire tissus,
papier, ....... pour les rendre non mouillables (imperméabilisation
des textiles) et rebelles aux tâches
Ils sont visqueux et servent à la lubrification (huiles ou
graisses et notamment graisse à rodages
Rhodorsil®) ; ils sont résistants aux moisissures et aux bactéries et servent
de base aux agents anti-mousses.
Ils ne sont pas toxiques et trouvent des applications dans de
nombreux domaines :
-
médecine et chirurgie (prothèses mammaires, tubes de transfusion, tubes
oxygénateurs, membranes souples, tétines de biberons),
-
cosmétologie,
-
secteur dentaire,
-
secteur alimentaire (moules pour la pâtisserie),
-
secteur des encres, peintures, vernis, cirages….
E) Macromolécules
naturelles :
I)Cellulose
:
Résulte de la polycondensation de glucose (C6H12O6)
CH2OH-CHOH-CHOH-CHOH-CHOH-C(H)=O sous forme de
β-D-glucopyranose
On obtient des chaînes dîtes "linéaires".
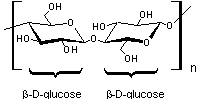
Les différentes chaînes placées côte à côte sont liées par de
nombreuses liaisons hydrogène ce qui donne à ce matériau une très grande
rigidité et qui explique qu'elle est la substance de soutien (parois) des
cellules jeunes des végétaux :
Liaisons intramoléculaires :
|
|
|
|
Selon
Liang et Marchessault - 1959 |
Selon
Blackwell et al. -
1977 |
Liaisons
intermoléculaires :
|
|
|
Klemm et al - 1998 |
La cellulose pratiquement pure est tirée du fruit du cotonnier; il
contient des graines recouvertes d’un duvet formé de fibres de 2 à 7 cm de
long; débarrassées des impuretés, ces fibres constituent le coton hydrophile.
La cellulose s’obtient également à partir du bois; le bois est essentiellement
constitué de cellulose et de lignine; un traitement à l’hydrogénosulfite de
calcium détruit la lignine; il reste la pâte de bois; on en fait le papier, le
carton, ....
Elle n'est pas attaquable par les sucs digestifs de l'homme. C'est
une matière première de tout premier ordre dans l'industrie chimique.
Elle est insoluble dans l'eau et la plupart des solvants
organiques et n'est solubilisée que par une solution ammoniacale d'hydroxyde de
cuivre(II) : la liqueur de Schweitzer. Son hydrolyse acide conduit au
glucose.
II) Caoutchouc naturel :
Provient de la coagulation du suc laiteux (latex) de l’hévéa; la
coagulation s’obtient par action de l'acide éthanoïque CH3COOH.
C’est un polymère de l’isoprène (2-méthylbutadiène) :
![]()
dont le motif est :

Il correspond à un enchaînement
(Z)1,4 de l'isoprène.
A l’état pur, c’est un solide blanc, un peu moins dense que l’eau,
soluble dans le benzène (C6H6), le tétrachlorométhane
(CCl4 ).
Il se soude à lui-même, à froid, par simple pression (pour
5<t<35°C). A t<5°C, il est cassant; à t> 35°C, il se ramollit. Pour
lui conserver son élasticité à froid et à chaud, on lui incorpore environ 3% de
soufre et diverses charges (magnésie,craie,....) ; on obtient alors du
caoutchouc vulcanisé.
En incorporant davantage de soufre (30%), on obtient un produit
dur et cassant: l’ébonite. C’est un bon isolant électrique.
III) Protéines :
Résultent de la polycondensation d’un grand nombre d’acides a-aminés :
![]()
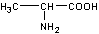
Exemple : l'alanine
![]()
La polycondensation donne une succession de liaisons
peptidiques :
![]()
Les acides a-aminés et les protéines sont des constituants essentiels de la matière vivante. La chair des animaux est essentiellement constituée de protéines. L’albumine des oeufs, les globulines du plasma, la kératine des poils, etc.... sont des protéines. La nature, le nombre et l’ordre d’enchaînement des divers acides aminés obéissent à des lois rigoureuses pour former chaque protéine.
F) Substances
macromoléculaires artificielles,dérivées de macromolécules naturelles :
Il s’agit pratiquement de substances dérivées de la cellulose.
I) Viscose :
Cellulose avec NaOH
concentré -------> alcali-cellulose qui, avec CS2 ---->
xanthate de cellulose.
Le xanthate de cellulose se dissout dans la soude en donnant un
liquide sirupeux, la viscose, qui se coagule au contact des acides en donnant
une substance transparente et brillante. On obtient ainsi les feuilles de cellophane
et les fils de rayonne. Les tissus de rayonne ressemblent à ceux en
soie.
II) Nitrate de cellulose :
HNO3 peut estérifier les -OH de la cellulose
-----------> " nitrocelluloses "
Le nitrate de cellulose à 12% d’azote (2 NO2 par motif
- attaque des OH secondaires) dissous dans un mélange alcool-éther, donne un
liquide sirupeux (collodion) ; ce produit, mélangé à du camphre en solution
dans l’alcool donne une pâte qui, après évaporation de l’alcool, devient le
celluloïd ; utilisation : balles de ping-pong.
Une nitration plus poussée de la cellulose (~ 13% d’azote) fournit
le coton-poudre, explosif sans fumée.
Le coton, après traitement par le mélange sulfo-nitrique, a à peu
près l’aspect d’origine, mais il est plus rugueux; on en fait une pâte par
dissolution partielle dans un mélange alcool+éther; cette pâte est ensuite
filée, séchée et réduite en granulés. C’est le chimiste Christian
Friedrich Schönbein qui
prépara le premier ce nitrate de cellulose en 1846.
III) Acétate de cellulose :
Une ou plusieurs molécules de CH3COOH peuvent
estérifier les -OH du motif de la cellulose.
La cellulose moyennement acétylée, soluble dans l’acétone, peut
donner une pâte qui, filée et séchée conduit aux fils d’acétate; les tissus
d’acétate ressemblent à la soie; avec l’acétate de cellulose on fait encore les
pellicules, support d’émulsions photographiques, des montures de lunettes, des
stylos, des manches d’outils, du vernis,.......
IV) Autres composés cellulosiques :
La famille des cellulosiques comporte un grand nombre de matières
qui sont des dérivés de substitution des fonctions alcools.
- Avec R =
CO-CH2-CH3 (propionate), CO-CH3 et CO-CH2-CH2-CH3
(acéto butyrate) on fait des articles de bureau, des boîtiers de protection, ….
- Avec R = CH3
méthylcellulose, C2H5 éthylcellulose, CH2-CH2OH
hydroxyéthylcellulose, CH2COOH carboxyméthylcellulose on obtient
surtout des émulsifiants, des gélifiants, des cosmétiques, …..
Certains de ces produits sont des additifs alimentaires.
G) Des polymères dégradables :
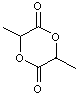
I) Polylactide (PLA)
Le monomère est le lactide (ou
2,5-diméthyl-3,6-dioxo-1,4-dioxanne) :
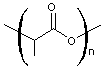
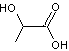
obtenu par condensation de l'acide lactique
lui-même obtenu par fermentation du D-glucose issu de
l'amidon de maïs.
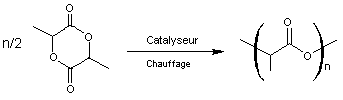
La polymérisation du lactide a lieu par ouverture
du cycle (POC).

Le polymère
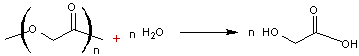
qui se déforme dès 50°C, est thermoplastique et dégradable
sous l'effet d'enzymes excrétées par des microorganismes (bactéries,
champignons, algues).
La biodégradation du PLA a lieu en deux étapes :
·
La première est une
hydrolyse des liaisons esters autocatalysée par les acides libérés conduisant à
la réduction du poids moléculaire et à la formation de fragments à bas poids
moléculaire (oligomères).
·
La deuxième étape
correspond à l'assimilation par les microorganismes de ces fragments pour une
minéralisation complète en formant CO2 et H2O.
C'est un polyester entièrement biocompatible et
biorésorbable, qui a permis dans les années 1980 de créer une fibre qui a tout
de suite intéressé le domaine médical ; Les chirurgiens l'utilisent (sutures,
implants).
Il sert également, de nos jours, à confectionner de nouveaux
tissus (en ameublement par exemple) et en association avec de la soie, pour des
vêtements.
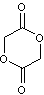
II) Poly(acide glycolique) ou polyglycolide (PGA) et copolymères
Poly(lactide-co-glycolide) (PLGA)
- PGA
Le monomère est le glycolide (ou p.dioxanne-2,5-dione) :
![]()
La polymérisation a lieu par ouverture du cycle (POC),

on obtient un polymère thermoplastique, le plus simple des
polyesters aliphatiques linéaires, le premier polymère biodégradable qui a été
utilisé pour des fils de suture.
Le PGA est plus hydrophile que le PLA.
Le polymère est dégradable dans l'organisme par hydrolyse des
fonctions esters qui conduit d'abord à des oligomères puis à l'acide
glycolique ; on peut traduire cette dégradation globale par
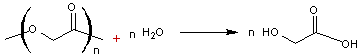
Celui-ci entre dans le processus métabolique, le terme ultime
de la dégradation étant CO2 et H2O.
Le PGA est hautement cristallin ; il a un point de fusion
élevé et une faible solubilité dans les solvants organiques.
- PLGA
On fabrique des copolymères (PLGA) lactide-co-glycolide. En
modifiant ainsi ses propriétés physiques on permet au composé obtenu de
s'adapter aux exigences demandées notamment en chirurgie (pour les implants par
exemple).
Poly(lactide-co-glycolide)
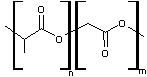
Le PLGA peut résulter de la polycondensation d'acide lactique

et d'acide glycolique
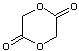
Par estérifications successives, en proportions équimolaires
et avec alternance régulière on obtiendrait :
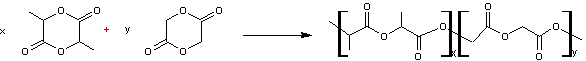
Mais la synthèse se fait généralement par ouverture des
cycles lactide
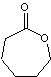
et glycolide
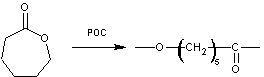
On peut écrire schématiquement :
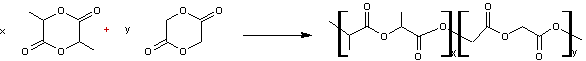
III) (Poly(ϵ-caprolactone))
ou Polycaprolactone (PCL).
Le monomère est la ϵ-caprolactone :
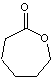
La polymérisation a lieu par ouverture du cycle (POC)
C'est un polymère biodégradable.
Il est un hydrophobe comme le PLA ; sa densité est de 1,1 et
son point de fusion aux alentours de 60°C ; sa qualité principale est sa
flexibilité (sa déformation à la rupture peut atteindre 1100%).
On l'utilise comme plastifiant mais aussi dans le domaine de
l'emballage et des adhésifs. Dans le domaine de la pharmacie, on l'utilise dans
le processus de libération contrôlée des principes actifs.
Par copolymérisation on peut obtenir un copolymère
polyuréthane thermoplastique (TPU)/PCL servant de charpente lors de la
régénération de tissus de la peau.
Par mélange de polyuréthane thermoplastique (TPU) (25%) et de
PCL (75%) on obtient un produit ayant une mémoire de forme et permettant de
fabriquer des fils de suture se nouant seuls.
IV) Pullulane
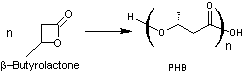
Le motif de répétition est le maltotriose (3 résidus
glucopyrannose liés en α-1,4). Les maltotrioses sont liés entre eux par
des liaisons glycosidiques en α-1,6.
Matériau soluble dans l'eau mais pas dans le méthanol,
l'éthanol ou l'acétone.
C'est une production polysaccharidique extracellulaire de l'hypomycète
Aureobasidium pullulans (une levure), de plus en plus l'objet
d'applications commerciales et industrielles.
Les usages pharmaceutiques:
Il sert à fabriquer des gélules transparentes, solubles dans l'eau et étanches
à l'air servant d'enrobage à des médicaments ou destinées à contenir des huiles
ou des poudres à usage diététique.
Les usages alimentaires:
Il permet d'obtenir des emballages, des contenants, des épaississants pour
confitures et sauces en remplacement de la gélatine ou de l'amidon.
Applications industrielles:
Colles et adhésifs, couches pour bébés.
V) PBS et PBSA
L'acide succinique
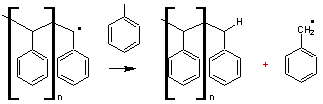
est un synthon
(building block) à quatre carbones, servant de point de départ à de multiples
synthèses.
Une des méthodes pour l'obtenir utilise des molécules issues du pétrole.
Par des technologies propres "biotechnologies
blanches" on peut le produire à partir du glucose (provenant de
l'amidon de blé, de maïs ou de résidus ligno-cellulosiques ou provenant des
sucres de la canne à sucre ou de la betterave) par métabolisme bactérien
(fermentation) ; Actinobacillus succinogenes, Mannheimia succiniproducens
mais aussi Escherichia Coli sont les principales bactéries utilisées.
L'acide succinique est utilisé par exemple pour la production de polyesters,
polymères biodégradables : PBS (PolyButylène Succinate
: Acide succinique et butanediol) et PBSA ( PolyButylène
Succinate Adipate : Acide succinique, acide adipique et butanediol
).
VI) Sorona ®
Le propane-1,3-diol (ou PDO)
![]()
est un synthon
(building block) à 3 carbones servant de point de départ à de multiples
synthèses.
Par des technologies propres "biotechnologies blanches"
on peut le produire à partir du glucose (obtenu souvent à partir de l'amidon de
maïs) fermenté par une bactérie (non pathogène) génétiquement modifiée. On peut
aussi l'obtenir par fermentation du glycérol industriel non raffiné
(sous-produit de la production industrielle de biodiesel) suivie d'une étape de
purification.
Avec lui, on prépare en particulier des polymères thermoplastiques ; par
exemple, le sorona ®, polyester obtenu par polymérisation du propane-1,3-diol
avec l'acide téréphtalique (ou TPA), est utilisé pour fabriquer des pièces
d'automobiles ou des textiles de hautes performances.
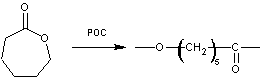
VII) PHB
ou poly(3-hydroxybutyrate)
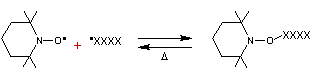
Le poly(3-hydroxybutyrate) est
un polymère biodégradable, qui est
produit naturellement par des micro-organismes (Bacillus megaterium par
exemple) mais qui peut être synthétisé à partir de la β-butyrolactone ; il
trouve des applications dans le médical lorsqu'on a besoin d'un matériau
biodégradable.
H) Des abréviations :
ABS Terpolymère acrylonitrile-butadiène-styrène
CA Acétate
de cellulose
CAB
Acétobutyrate de cellulose
EP Polyépoxydes
EVA
Copolymère éthylène-acétate de vinyle
MF
Mélamine-formaldéhyde
NR Caoutchouc naturel
PA
polyamides 6,6-6,6-10,11,12
PBSA Polybutylène succinate adipate
PBT
Polybutylène téréphtalate
PC
Polycarbonates
PCL Polycaprolactone
PE Polyéthylène
PEBD Polyéthylène basse densité
PEBDL Polyéthylène basse densité linéaire
PEG Polyéthylèneglycol
PEHD Polyéthylène haute densité
PESU
polyéthersulfone
PET
Polyéthylène téréphtalate
PF
Phénol-formaldéhyde
PGA Polyglycolide
PI
Polyimides
PLA Polylactide
PLGA Copolymères lactide-co-glycolide
PMMA
polyméthacrylate de méthyle
POM Polyoxyméthylène
PP Polypropylène
PPO
polyphénylène oxyde
PPS polyphénylène sulfure
PS Polystyrène standard
et choc
PSE
Polystyrène expansible
PSU
polysulfone
PTFCE
polytrifluorchloréthylène
PUR
Polyuréthanes
PVDC
Polychlorure de vinylidène
PVDF Polyfluorure de vinylidène
PVC Polychlorure de
vinyle
SAN Copolymère styrène-acrylonitrile
SI Silicones
UF Urée-formaldéhyde
UP Polyesters insaturés
I) Transfert de chaîne – Polymérisation
vivante
I)
Tranferts de chaîne
Un transfert de chaîne est un stade réactionnel se produisant
généralement au cours de réactions en chaîne et dans lequel le site réactif est
transféré de la macromolécule en cours de croissance à une autre molécule, ou à
une autre partie de la même molécule.
Exemple :
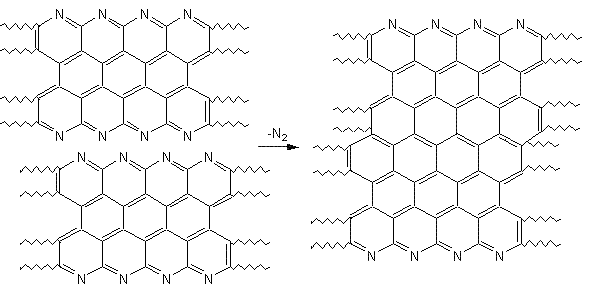
II)
Polymérisation vivante
La définition donnée par l'IUPAC (Union internationale de
chimie pure et appliquée) de la polymérisation vivante est la suivante :
"C'est une polymérisation en chaîne dont le transfert et la
terminaison de chaîne sont absents. Dans de nombreux cas la vitesse
d'initiation de la chaîne est rapide par rapport à la vitesse de propagation de
la chaîne, de sorte que le nombre de porteurs de chaînes cinétiques est
essentiellement constant tout au long de la polymérisation."
La polymérisation se termine quand le monomère est épuisé, mais
l'extrémité de la chaîne demeure activée. On obtient des chaînes de longueur
sensiblement égales.
Rappelons que la longueur de chaîne, directement liée au degré de
polymérisation, influence diverses propriétés physiques du polymère obtenu
comme la viscosité, la température de transition vitreuse ou le module
d'élasticité.
On comprend alors que l'utilisation de polymérisations vivantes
permet d'obtenir des polymères à propriétés physiques définies.
On voit aussi que cette méthode se prête particulièrement bien à
l'obtention de copolymères en blocs de type XXXXYYYYZZZZ ; en effet il suffit
d'attendre que le monomère X soit épuisé pour mettre le monomère Y puis Z.
Ces réactions sont très voisines des polymérisations contrôlées ;
dans celles-ci la terminaison est supprimée mais pas éliminée ce qui veut dire
qu'on peut placer le polymère dans un "état dormant" et lui permettre
de recommencer à s'allonger en modifiant par exemple la température, ce qui
réactive l'extrémité de la chaîne qu'un réactif P° était venu provisoirement
bloquer.
XXXX° + P° …….. XXXX-P En chauffant légèrement XXXX-P ……… XXXX° +
P°.
Un radical très utilisé pour bloquer provisoirement la chaîne est
le 2,2,6,6-tétraméthyl-1-pipéridinyloxy
dont le nom est abrégé en TEMPO :
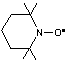
Le blocage de la chaîne se fait par réaction des deux radicaux :
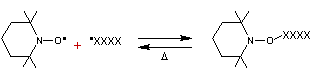
Un léger chauffage libère l'extrémité de la chaîne.
Annexe 1
Les fibres de carbone
Elles sont fabriquées à partir de polyacrylonitrile P.A.N. (appelé précurseur) . Une première étape consiste à oxyder des fibres de PAN à l'air vers 200 ou 300°C pendant 1 à 2 heures. La deuxième étape est la carbonisation , obtenue en chauffant le produit précédent entre 700 et 1500°C pendant 2 à 10 minutes sous atmosphère de diazote ; cette étape comme son nom l'indique conduit à éliminer la plupart des atomes autres que ceux de carbone (H et N : voir ci-dessous). On obtient une fibre contenant environ 90% de carbone, 8% d'azote, 1% d'oxygène et 1% d'hydrogène, qui a une résistance élevée mais une faible élasticité et qu'on peut utiliser après traitement de surface.
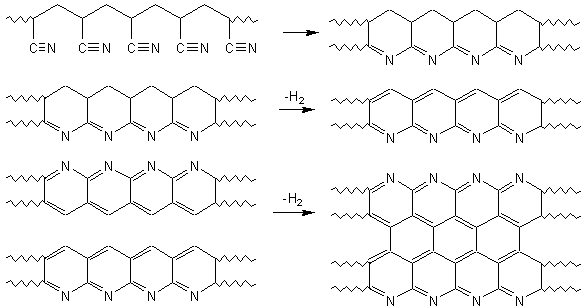
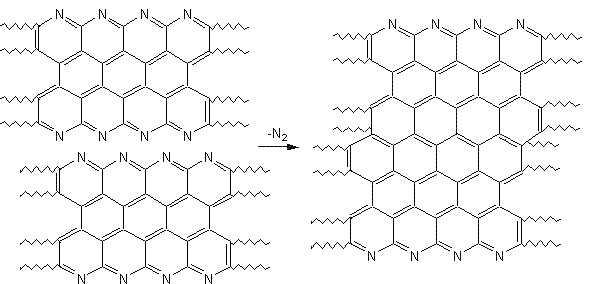
On peut aussi après la carbonisation, procéder à la graphitisation
en chauffant la fibre précédente entre 2000 et 3000°C pendant une minute. On
obtient un produit à 99% de carbone possédant la structure en feuillets du
graphite (voir ci-dessous), une élasticité élevée mais une moindre résistance ;
elle nécessite un traitement de surface (en principe une oxydation
électrolytique de surface) qui augmentera son adhérence sur une matrice en
polymère .

Les diamètres des fibres de carbone se situent entre 5 et 8 µm.
Les avantages des fibres de carbone sont :
- Faible densité.
- Grande souplesse.
- Un faible coefficient de dilatation thermique
- Une très bonne tenue à la compression (en comparaison de la fibre de verre ou
du kevlar).
- Une très bonne tenue à haute température (2000°C) en atmosphère non oxydante.
- Une excellente rigidité (surtout les fibres graphitisées).
- Bonnes conductions électrique et thermique (Elles peuvent encore être
augmentées par métallisation (dépôt de nickel ou de cuivre) des fibres).
- Complète inertie aux agents chimiques non oxydants.
Quelques inconvénients :
- Sensibilité au choc mécanique et à l'abrasion.
- Leur raideur rend difficile le bobinage des filaments.
Les fibres de carbone peuvent être utilisées seules ou sous
forme de matériaux composites (on appelle matériaux composites
des matériaux composés d'un renfort, fibres résistantes noyées dans une matrice
moins résistante mécaniquement :résines thermoplastiques ou thermodurcissables
(polyesters, polyuréthanes, silicones) ou alliages d'aluminium ou de titane, ou
encore de nature minérale : graphite carbure de silicium) ; dans le composite
fibre de carbone-carbone, la fibre de carbone constitue le renfort, la matrice
étant le graphite.