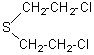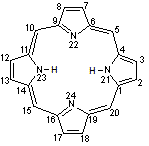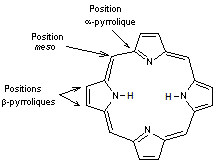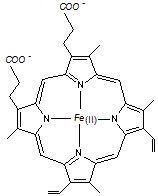MEDICAMENTS ET MOLECULES
PARTICULIERES (2)
|
ou Oxyde de N,N-diméthylméthanamine Aspect physique : Aiguilles hygroscopiques Masse molaire : 256°C Solubilité : Très soluble dans
l'eau et l'éthanol. N° CAS : 1184-78-7 |
|
C'est un composé inodore qui se
forme normalement dans le foie par oxydation de la triméthylamine (malodorante)
provenant du métabolisme de certaines substances ingérées (poissons, oeuf,
foie, reins...)
|
||
|
|
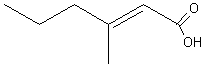
Cette molécule est la
principale responsable de l'odeur de transpiration chez les êtres humains. |
|||
|
|
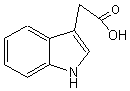
Produit naturel
d'origine végétale qui a le même effet qu'une hormone sur la croissance de
plusieurs insectes. Il pourrait être utilisé pour protéger les cultures en
limitant le flux des insectes prédateurs. |
|||
|
ou Méthylmercaptan CH4S Aspect physique : Gaz incolore Masse molaire : -123°C Ebullition : Solubilité : Très
soluble dans l’éthanol et l’éther ; légèrement
soluble dans l’eau et le chloroforme. |
CH3-SH Le méthylmercaptan ou méthanethiol est
obtenu industriellement par réaction entre le sulfure de dihydrogène et le
méthanol. |
Le méthanethiol est principalement
utilisé comme intermédiaire de
synthèse de la méthionine (acide
aminé utilisé dans l'alimentation animale). C’est une substance à
odeur caractéristique que l'on excrète dans les urines après avoir mangé des
asperges. C’est un métabolite de
l’acide asparagusique. |
||
|
|
Hormone végétale |
|||
|
|
Test à la ninhydrine: permet de détecter les a-aminoacides par une réaction conduisant à une couleur
dans le bleu-violet.
|
|||
|
|
Poison violent utilisé
comme arme de guerre chimique notamment pendant la première guerre mondiale. |
|||
|
|
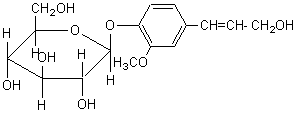
Hétéroside présent dans la sève des conifères |
|||
|
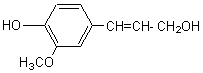
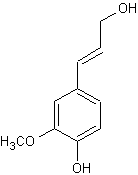
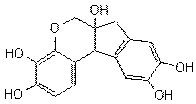
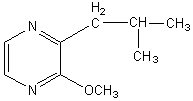
ou 4-(3-hydroxyprop-1-ènyl)-2-méthoxyphénol
Masse molaire : 74°C Ebullition : 458-35-5 Solubilité : Très soluble dans
l'éther ; soluble dans l'éthanol ; insoluble dans l'eau. |
ou
|
Partie aglycone d'un hétéroside présent dans la sève des conifères. Il dérive tout comme
l'acide férulique du métabolisme de la phénylalanine
et de la tyrosine et peut être obtenu
à partir de l'acide férulique par réduction. |
||
|
Amygdaline (du grec amugdalê:
amande) ou Amygdaloside Mandelonitrile-b-gentiobioside |
|
Hétéroside végétal présent dans les amandes amères
et les noyaux de certains fruits (les drupes: cerises, abricots, prunes). Il a été mis en
évidence en 1830 par Robiquet dans les amandes amères (Prunus dulcis). |
||
|
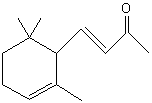
a-Ionone |
|
Composé à odeur de
violette. Il est utilisé dans de nombreuses synthèses, notamment celle du
phytol et de la vitamine A. |
||
|
b-Ionone |
|
Composé à odeur de
violette. |
||
|
|
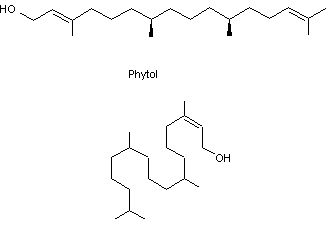
Diterpène oxygéné que l'on trouve sous forme
estérifiée dans la structure de la chlorophylle,
on le retrouve donc comme produit de dégradation de celle-ci. Sa synthèse fut menée
pour la première fois par Franz Gottwald Fischer, en 1928. |
|||
|
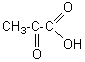
Acide pyruvique
|
|
Le glucose libéré du glycogène se transforme en acide pyruvique
par une voie réactionnelle complexe appelée glycolyse où interviennent
diverses enzymes. |
||
|
ou ou Malonylurée Aspect : Cristaux en prismes orthorhombiques
(si recristallisé dans l'eau) Masse molaire : 248°C Ebullition : N° CAS : 67-52-7 Solubilité : Soluble dans l'eau et
dans l'éther ; légèrement soluble dans l'éthanol. |
On l'obtient par condensation avec
l'urée du dimalonate d'éthyle en présence d'éthylate de sodium.
|
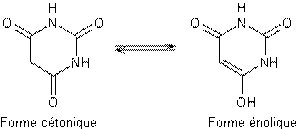
L'acide barbiturique,
un uréide peu soluble dans l'eau, est un monoacide plus fort que l'acide
éthanoïque. La forme énolique fait mieux apparaître ce caractère que la forme
cétonique. Nombre de ses dérivés,
appelés barbituriques, sont des hypnotiques et des sédatifs du système
nerveux (gardénal, véronal...). On appelle
barbituriques, des dérivés dialcoylés ou arylés au carbone de l'acide
barbiturique ; Ils ont été utilisés comme calmants somnifères et hypnotiques. |
||
|
|
Pigment de lichen à
propriétés antibiotiques. |
|||
|
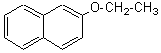
Néroline(II)
ou |
|
Utilisé en parfumerie
comme substitut de l'essence de fleur d'oranger. |
||
|
|
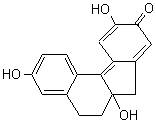
Molécule qui se forme
par oxydation spontanée à l'air, des substances majeures des "bois
solubles" : bois du Brésil et notamment de Pernambouc, bois de Campêche (la
plus vieille ville espagnole connue du Yucatan au Mexique). Les molécules
extraites sont incolores et en quelques heures se transforment en braziléine
ou en hématoxyline, qui sont de couleur rouge. Elles servaient autrefois à
fabriquer les laques rouges utilisées par les artistes peintres. |
|||
|
Aspect : Cristaux jaunes. Masse molaire : Soluble dans l’éthanol
; légèrement soluble dans l’eau, l’éther. N° CAS : 517-28-2 |
|
Molécule qui se forme,
comme la braziléïne, à partir des substances
majeures des "bois solubles". Par oxydation la couleur est jaune
puis rouge puis rouge foncé puis noire (voir hématéine). |
||
|
C16H12O6 Aspect : Cristaux rouge sombre,
marrons. Masse molaire : Légèrement soluble
dans l’éthanol et le méthanol ; insoluble dans l’eau, l’éther, le
benzène, le chloroforme. N° CAS : 475-25-2 |
|
Par oxydation de l’hématoxyline, on obtient l’hématéine de couleur
noire |
||
|
Cantharidine
|
|
Monoterpène bicyclique constituant le principe
irritant de la substance injectée lors de la piqûre de la cantharide (Mouche
d'Espagne ou Spanish fly en anglais, insecte coléoptère vert doré de longueur
2cm environ fréquent sur les frênes). C'est un produit toxique et vésicant
utilisé comme insecticide et qui entrait autrefois dans la préparation
d'aphrodisiaques.
|
||
|
|
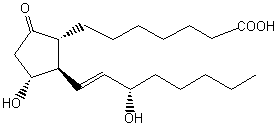
PGE1 |
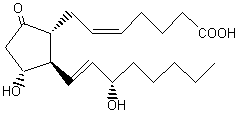
Famille de molécules
agissant comme des hormones et qui permettent de contrôler de nombreuses
fonctions physiologiques (diminution de la tension sanguine, induction des
contractions en vue de l'accouchement, menstruation, inhibition de
l'agrégation plaquettaire, exaltation des réactions inflammatoires par
exemple...). John Vane (Prix Nobel
de médecine en 1982) découvre le rôle des prostaglandines dans les phénomènes
inflammatoires. |
||
|
|
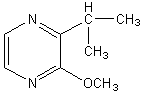
Molécule donnant leur
odeur aux pommes de terre crues. |
|||
|
|
Molécule donnant leur
odeur aux poivrons verts. |
|||
|
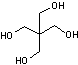
C5H12 O4
Masse molaire : Ebullition : Sesublime Indice de réfraction : 1,548 115-77-5 |
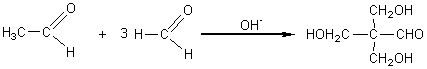
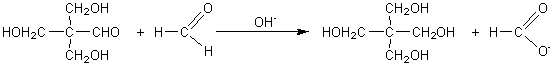
Sa
synthèse
: |
Polyol servant à
fabriquer des revêtements de surface et le PETN,
un explosif puissant. |
||
|
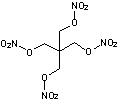
Tétranitrate de pentaérythritol C5H8 N4O12 Masse molaire : Ebullition : 180°C (se décompose au
dessus de 150°C) Densité : 1,773 (20°C) 78-11-5 |
|
Explosif dont la
structure rappelle celle de la nitroglycérine. C'est un solide
blanc cristallisé qui a été préparé en laboratoire en 1894 à Cologne
(Allemagne) puis fabriqué à partir de 1912 ; il a été utilisé pendant la
première guerre mondiale puis lors de la seconde pour la fabrication de
mines. Il peut être
obtenu pat nitration (action de l'acide nitrique concentré) sur le
pentaérythritol
C'est un explosif
moyennement sensible aux chocs et aux frottements. Sa vitesse de
détonation est 8400 m.s-1 pour une densité de 1,77. Explosif très puissant
appelé aussi penthrite (ou pentrite). Plus stable que la dynamite il entre
dans la composition du plastic
(Semtex). |
||
|
Mélamine
ou C3H6N6 Aspect : Cristaux en prismes monocliniques
si recristallisés dans l'eau. Masse molaire : 126,120 g.mol-1 Fusion : 345°C (se décompose) Ebullition : Se sublime Densité : 1,573 (à 16°C) Indice de réfraction : 1,872 à 20°C Solubilité : Soluble dans l'eau et l'éthanol ;
insoluble dans l'éther. N° CAS : 108-78-1 |
|
C'est le trimère du
cyanamide (HN=C=NH ou NC-NH2). |
||
|
Camomille allemande ou matricaria
chamomilla |
Molécule présente dans
la camomille ordinaire (camomille allemande ou matricaria chamomilla).
L'un de ses stéréoisomères (E,Z) présente des propriétés fongicides et
insecticides. |
|||
|
Acide phytique
|
|
Existe sous forme de
sels de calcium et de magnésium dans les graines de nombreuses
céréales.
|
||
|
C12H8O Masse molaire 168,191 g.mol-1 Fusion 83°C Numéro CAS 495-74-9 |
|
Cétone
polyacétylénique (Ethynylcétone) naturelle (Elle a été isolée la première
fois d'Artemisia capillaris en 1956) ayant une activité fongicide;
c'est un antifongique. |
||
|
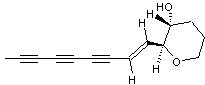
Ichthyothéréol
C14H14O2 Masse molaire 214,260 g.mol-1 Numéro CAS 20110-23-0 |
|
Poison présent dans
les feuilles de plantes d'Amérique du sud et d'Amérique centrale, très
violent et mortel pour les poissons et provoquant des convulsions chez les mammifères.
Il est utilisé par les indiens d'Amazonie pour enduire la pointe de leurs
flèches. |
||
|
|
Alcaloïde ayant montré
une activité contre les tumeurs (il bloque l’activité de la topoisomérase I)
et la leucémie mais dont la toxicité a empêché l’utilisation directe à des fins
thérapeutiques. Des dérivés de cette molécule constituent des médicaments
utilisés en chimiothérapie : l’irinotecan (cancer du colon) et le
topotecan (cancer de l’ovaire). La Camptothecine a été
isolée la première fois de Camptotheca
acuminata, un arbre ornemental courant en Chine centrale. |
|||
|
|
Triterpène, principal constituant du liège. |
|||
|
|
Phéromones sexuelles
d'une variété de hannetons (hanneton du sapin Douglas). |
|||
|
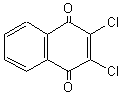
|
Fongicide |
|||
|
|
||||
|
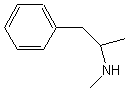
Métamphétamine |
|
Molécule voisine de l'amphétamine
et de l'éphédrine. Elle peut être
synthétisée à partir de l'éphédrine. |
||
|
Germanicol
|
|
Triterpène naturel que l'on trouve par exemple
dans: |
||
|
Si l'on substitue les hydrogènes des carbones b de la porphine (carbones des noyaux pyrrole non liés à l'azote) par des chaînes carbonées on obtient une porphyrine. |
|
Structure composée de
4 noyaux pyrrole liés les uns aux
autres à partir de leurs positions 2- et 5- par 4 ponts méthine (=CH-). |
||
|
|
L'hème est constitué
d'un noyau porphyrine (structure plane) et d'un
atome de fer (II); ce complexe est rouge et donne sa couleur au sang. Du
point de vue biologique l'hème est une porphyrine très importante puisqu'elle
assure la fixation de l'oxygène. |
|||
|
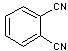
Phtalocyanine de cuivre (II) C32H16CuN8 Masse
molaire : 576.08
g.mol-1 Fusion : 600°C N° CAS : 147-14-8 |
|
|
||
|
Succinylcholine ou Suxaméthonium Anectine ® nom systématique: C14H30N2O42+ Masse molaire : 290,399 g.mol-1 N° CAS : 306-40-1 |
|
Médicament aux
propriétés curarisantes, utilisé en anesthésie pour provoquer un relâchement
musculaire (curare dépolarisant). C'est une poudre blanche sans odeur, légèrement
amère et très soluble dans l'eau. Remarque:Le curare est un mélange de substances extraites de lianes d'Amazonie et provoquant une paralysie des muscles. Il est utilisé par les Amérindiens qui en enduisent l'extrémité de leurs flèches . |