DEUX
MATERIAUX VISCOELASTIQUES
Silly Putty® et Slime®
Gérard GOMEZ
Plan de l'étude
1) Propriétés remarquables des matières viscoélastiques
2) Le Slime
®
3) Le Silly Putty ®
3-1)
PBS
3-2)
Autres PBS
3-3)
Relation entre propriétés et structure dans les PBS
4) L'oobleck
Annexe 1 Silly
Putty®
Annexe 2 Fluide newtonien
Annexe 3
Alcool polyvinylique, Borax, réticulation
Annexe 4 Le
poly(diméthylsiloxane) ou (PDMS)
1) Propriétés
remarquables des matières viscoélastiques :
Les matériaux
viscoélastiques peuvent, selon les contraintes qui leur sont imposées, être
élastiques ou visqueux.
Ainsi :
- le Silly Putty ® (voir annexe 1)
x Si on jette une boule de ce matériau qui ressemble à de la pâte
malléable, sur le sol, elle rebondit comme le fait une balle de ping-pong.
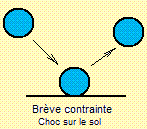
x Si on laisse cette boule sur le sol elle finit par s'étaler comme le
fait un liquide.

x Placée sur un anneau la boule forme au bout d'un certain temps une
goutte qui finit par se détacher et tomber.
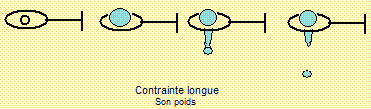
x Si on sépare en les arrachant deux morceaux de ce matériau puis qu'on
les remet en contact bord à bord, ils se "ressoudent" spontanément
montrant des propriétés d'autoréparation certaines et intéressantes.
- le Slime
®
x Sans contrainte, il coule et on peut si on le manipule avec précautions
obtenir un film mince.
x Si on le manipule sans ménagement il forme un bloc et se casse.
x En penchant le contenant dans lequel il se trouve, puis en redressant
celui-ci, et même en l'abandonnant sur une table, il continue à couler.

x Une boule de Slime projetée au sol rebondit
très peu comparativement à une boule de Silly Putty.
On le voit, le
comportement de ces matériaux sous la contrainte n'est pas le comportement d'un
fluide comme l'eau que l'on qualifie de fluide newtonien (voir annexe 2).
Ces matériaux à la
viscosité particulière sont classés comme fluides non newtoniens ; leur
viscosité dépend de la vitesse à laquelle ils se déplacent.
Parmi ceux-ci on
distingue :
* Les fluides non newtoniens
rhéoépaississants (c'est le cas du Silly Putty et du Slime) ; leur viscosité dynamique augmente quand leur
vitesse d'écoulement augmente ; dit autrement ils deviennent plus visqueux
quand on augmente l'agitation.
* Les fluides non newtoniens
rhéofluidifiants (exemple le sang) ; leur viscosité dynamique diminue quand
leur vitesse d'écoulement augmente ; ils deviennent moins visqueux quand on
augmente l'agitation.
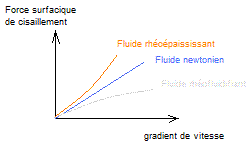
On peut traduire cela
par des courbes :
On porte (voir les
définitions dans l'annexe 2) la force surfacique de
cisaillement en ordonnée et le gradient de vitesse en abscisse ; La viscosité
en chaque point correspond au coefficient directeur de la tangente à la courbe
en ce point.
Les fluides non
newtoniens les plus abondants sont rhéofluidifiants.
2) Le Slime ®
Il s'agit d'un gel
résultant de la réticulation par le borax (Na2B4O7,
10 H2O) de l'alcool polyvinylique PVA de masse molaire 100 000 Da au
minimum et qui correspond à une hydrolyse du poly (acétate de vinyle) d'au
moins 95% (voir annexe 3).
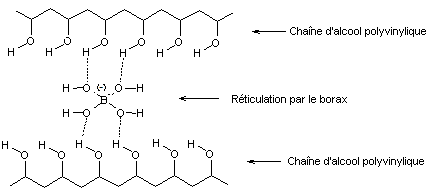
Des liaisons hydrogène
s'établissent entre les doublets d'électrons des atomes d'oxygène du borax
placé entre les chaînes de polymère et les atomes d'hydrogène des groupes
alcool des chaînes de PVA de part et d'autre.
En fonction des
contraintes mécaniques que subit le Slime®, ces
liaisons se rompent ou s'établissent modifiant sa viscosité.
|
|
Sa préparation en
laboratoire : - Dissoudre 4g de
PVA (Masse molaire Supérieure à 100 000g/mol) dans 100mL d'eau à 80°C et
agiter jusqu'à obtenir une solution homogène. - Préparer une
solution saturée de borax (400mg de borax dans 10 mL
d'eau). Ajouter un colorant alimentaire. - Quand les deux
solutions sont à température ordinaire verser lentement la solution de borax dans
celle de PVA en agitant avec un agitateur. Il y a une prise en masse.
Continuer à agiter en écrasant sur les bords du bécher puis mélanger
vigoureusement jusqu'à obtention d'une pâte gluante mais non collante. Recette provenant du
site de ressources en chimie pour les enseignants de l'Ecole Normale
Supérieure
http://culturesciences.chimie.ens.fr/content/synth%C3%A8se-de-mat%C3%A9riaux%C2%A0-le-slime |
3) Le Silly Putty ®
Il s'agit de polyborosiloxane (PBS) dont la structure est
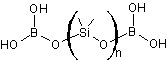
s'il a été obtenu par réaction du poly(diméthylsiloxane)
(PDMS) (voir annexe 4)
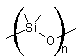
avec de l'acide borique B(OH)3 ou H3BO3 à
200°C.
Au cours de cette
réaction les chaînes de PDMS sont coupées et des fragments issus de l'acide
borique deviennent les groupes terminaux des molécules de polyborosiloxane.
Des liaisons hydrogène
se forment entre les groupements terminaux des chaînes faisant de ces polymères
des composés supramoléculaires.
Remarque :
Il se forme aussi lors
de cette réaction des produits de structure
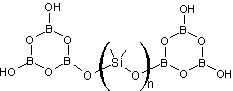
En les dissolvant dans
l'hexane et en les soumettant à l'air humide ils sont hydrolysés pour donner du
PBS qui reste en solution dans l'hexane et de l'acide borique sous forme de
poudre blanche
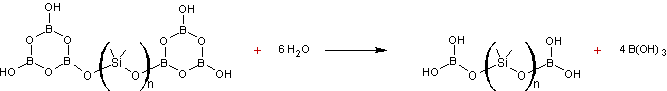
On peut aussi préparer des polyborosiloxanes
par polymérisation directe à 90°C entre le dichlorodiméthylsilane
Si(CH3)2Cl2
![]()
et l'acide borique B(OH)3
![]()
Le polymère résultant
peut être décrit par la formule brute (BO3)2(Si(CH3)2)3
3-3) Relation
entre propriétés et structure dans les PBS
Les propriétés des PBS
qui ont été données plus haut, et notamment le fait qu'ils peuvent s'auto-réparer sont dues aux liaisons hydrogène (qui font
d'eux des supramolécules) liaisons qui se font et se défont au gré des
contraintes que le matériau subit.
4) L'oobleck
On peut également
citer une autre substance non newtonienne rhéoépaississante, l'oobleck, obtenue en mélangeant de l'eau avec de l'amidon de
maïs. Elle peut se comporter comme un liquide lorsqu'elle est manipulée
lentement, mais devient soudainement plus visqueuse et même solide lorsqu'elle
est soumise à une pression ou une agitation rapide.
Elle est souvent
utilisée à des fins ludiques ou éducatives pour illustrer par exemple le
principe d'un fluide viscoélastiques.
Remarque :
Cette substance tire
son nom d'un terme provenant d'un livre pour enfants du Dr. Theodor Seuss Geisel intitulé
"Bartholomew and the Oobleck". Il a été
publié en 1949. L'histoire met en scène le personnage Bartholomew Cubbins et raconte comment le roi Azaz,
souverain du Royaume de Didd, demande une nouvelle
sorte de précipitation atmosphérique, différente de la pluie, de la neige, du
brouillard et de la grêle. Cela conduit à la création de l'"oobleck", une substance visqueuse et magique qui crée
des problèmes pour le royaume. Le livre est connu pour sa créativité
linguistique et ses illustrations distinctives, caractéristiques du style du
Dr. Seuss.
Silly Putty®
L'apparente extravagance du comportement de ce matériau est
à la base du nom qui lui a été donné : littéralement "mastic stupide"
Fluide newtonien
On dit qu'un fluide est newtonien (l'eau par exemple) s'il y
a proportionnalité entre une force élémentaire surfacique tangentielle
appliquée (force de cisaillement par unité de surface) et le gradient de la
vitesse qui en résulte, gradient (dans la direction perpendiculaire au
déplacement) de la vitesse tangentielle.
![]()
Le premier membre correspond à la contrainte subie par
l'élément de fluide considéré (force surfacique de cisaillement), le deuxième
membre au gradient de vitesse résultant ; le coefficient de proportionnalité
η étant la viscosité dynamique du fluide exprimée en Poiseuille (Pl).
|
|
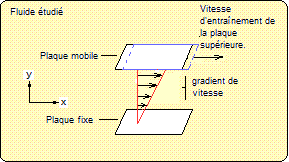
Envisageons deux plaques
métalliques parallèles plongées dans un fluide. On tire sur la plaque supérieure
parallèlement à sa surface
ce qui induit une certaine vitesse de déplacement. La
lame de fluide en contact immédiat de la plaque va à son tour se mettre en
mouvement et prendre la vitesse de la plaque (on suppose qu'elle adhère à
celle-ci). Des frottements vont avoir lieu entre la lame de fluide et une autre
lame située en dessous à son contact. La vitesse qu'elle va prendre sera
légèrement inférieure ….De proche en proche la
vitesse des lames va décroître jusqu'à arriver à 0 pour celle qui sera en
contact avec la plaque fixe inférieure. On dit qu'il s'établit un gradient de
vitesse que l'on note
La contrainte subie par un élément de
fluide et qui provoque son déplacement, encore appelée force surfacique de
cisaillement correspond à
Ces deux
grandeurs sont proportionnelles, le coefficient proportionnalité η étant
la viscosité dynamique du fluide exprimée en Poiseuille. Plus la
viscosité est grande et plus la force à appliquer pour un gradient de vitesse
donné sera grande. |
Alcool polyvinylique, Borax, réticulation
1) Alcool
polyvinylique ou PVA
![]()
Ce polymère n'est pas obtenu par polymérisation d'un
monomère insaturé, mais par hydrolyse d'un autre polymère, le poly (acétate de
vinyle) ou poly (éthanoate de vinyle) :
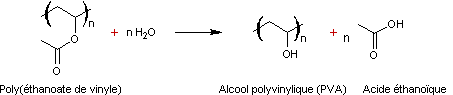
Ceci tient au fait que l'alcool vinylique n'est pas stable ;
c'est sa forme tautomère l'éthanal qui l'est :
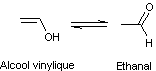
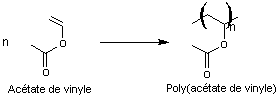
Remarque : Le poly(acétate de vinyle) s'obtient par polymérisation d'un monomère,
l'acétate de vinyle.
L'acétate de vinyle s'obtient, lui, industriellement de deux
façons :
- soit
par action de l'acétylène en excès sur l'acide acétique à 200°C avec des
catalyseurs à base de zinc ou de cadmium
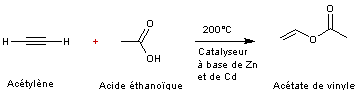
- Soit
par acétoxydation catalytique de l'éthylène en
présence d'acide acétique et d'oxygène ; le catalyseur est du palladium (Pd)
déposé sur de l'alumine et dopé par l'acétate de potassium.

La polymérisation de l'acétate de vinyle :
2) Le borax
Le borax ou borate de sodium se trouve dans le commerce à
l'état pur sous forme de cristaux blancs très fins, Na2B4O7,
10H2O. Il est couramment utilisé comme antiseptique, insecticide ou
retardateur de flamme.
Il peut aussi avoir d'autres degrés d'hydratation : 4 ou 5
molécules d'eau pour une molécule Na2B4O7.
En solution le borax s'hydrolyse:
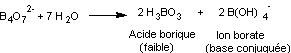
3) Réticulation
Lorsqu' on verse une solution de borax dans de l'alcool
polyvinylique on obtient un polymère réticulé ; des liaisons hydrogène s'établissent entre les doublets d'électrons
des atomes d'oxygène du borax placé entre les chaînes de polymère et les atomes
d'hydrogène des groupes alcool des chaînes de PVA de part et d'autre.
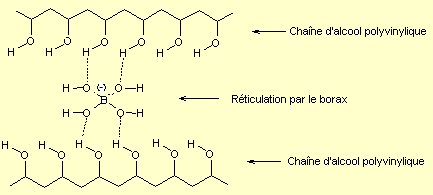
Cette réticulation rigidifie le
polymère car les chaînes d'alcool polyvinylique ont moins de liberté de
mouvement dans le milieu, et ce d'autant plus que les liaisons hydrogène sont
nombreuses
En fonction des contraintes
mécaniques que subit le Slime®, ces liaisons
hydrogène, moins solides que les liaisons covalentes, se rompent ou
s'établissent modifiant sa viscosité.
Le poly(diméthylsiloxane)
ou (PDMS)
Ce polymère encore appelé diméthicone
est un polysiloxane, structure de base des silicones
(huiles et caoutchoucs).
- Utilisé comme additif
alimentaire E900 (antimoussant des sodas et des huiles de friture).
- Utilisé en cosmétique
(shampooing pour augmenter le volume des cheveux).
- produit anti-poux.
- présent dans les huiles dites
aux silicones.
Il se présente comme
un liquide visqueux.
La formule du polydiméthylsiloxane est
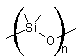
ou, en développant la chaîne
![]()
Ce polymère peut être obtenu de la
manière suivante :
-
On fait réagir le dichlorodiméthylsilane sur l'eau
![]()
-
On fait réagir le corps obtenu sur le dichlorodiméthylsilane
![]()
-
Le composé obtenu peut remplacer le dichlorodiméthylsilane
dans la réaction précédente
![]()
On voit que de proche en proche se
forme le PDMS.
Le mélange dichlorodiméthylsilane
et eau peut donc conduire au poly(diméthylsiloxane).