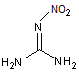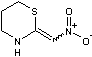Les
nÉonicotinoïdes
Gérard Gomez
avec la collaboration de
Jacques Baron
Plan de l'étude
1) La nicotine
2) Formules des néonicotinoïdes
3) Dénomination des néonicotinoïdes
4) Quelques propriétés des 5 composés principaux
5) Quelques autres néonicotinoïdes
6) Mode d'action des néonicotinoïdes
7) Synthèse de quelques néonicotinoïdes
7-1) Imidaclopride
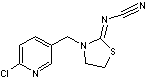
7-2) Thiaclopride
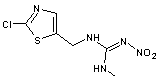
7-3) Acétamipride
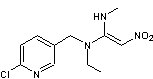
7-4) Nitenpyrame
Annexe 1 : Récepteurs – neurotransmetteurs
– Récepteurs nicotiniques
1) La nicotine
Comme leur nom de
famille l'indique les néonicotinoïdes sont de "nouvelles" (préfixe néo)
molécules "ressemblant à, s'apparentant à" (suffixe oïde)
la nicotine.
La nicotine est un alcaloïde présent dans les
feuilles de tabac (2 à 8 % dans les feuilles séchées) :
|
|
|
L-Nicotine |
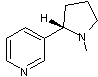
Cette molécule comporte les noyaux de la pyridine
![]()
et de la pyrrolidine
![]()
des molécules à propriétés basiques.
Elle a été découverte en 1809 par Louis-Nicolas Vauquelin.
Elle a été isolée pour la première fois par les chimistes
allemands Posselt et Reimann.
Sa structure a été élucidée par Pinner et Wolffenstein en 1895.
Aimé Pictet (Professeur à Genève) joua un rôle décisif dans sa
synthèse en 1903.
La L-nicotine se fixe sur les mêmes récepteurs que l'acétylcholine
et produit les mêmes effets, du moins en partie.
Stimulante à faible dose, elle provoque nausées et vomissements à
forte dose ; la dose létale se situerait entre 50 et 60 mg environ pour les
humains.
La nicotine bien que possédant un faible pouvoir insecticide a été
utilisée en agriculture, ainsi qu'un groupe de molécules similaires en
structure chimique appelées nicotinoïdes. C'est par référence à ce groupe qu'a
été ajouté le préfixe néo pour désigner les composés qui font l'objet de cette
étude ; ils ressemblent aux nicotinoïdes car ils partagent le même site de
fixation et possèdent un cycle pyridine similaire.
2) Formules des néonicotinoïdes
¾ On trouve très souvent le noyau pyridyle o.chloré,
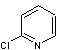
le plus souvent
pyridyl méthyl amine o.chloré,
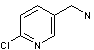
On peut y voir associé :
·
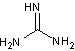
Un groupe
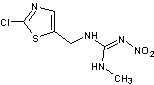
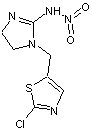
nitroguanidine c'est-à-dire un groupe –NO2
fixé sur un azote d'une guanidine substituée
|
|
|
|
Guanidine |
Nitroguanidine |
Exemple
|
|
|
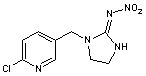
Imidaclopride |
·
Un groupe
cyanoamidine c'est-à-dire un groupe cyano,![]() fixé sur un azote d'une
amidine substituée
fixé sur un azote d'une
amidine substituée
|
|
|
|
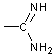
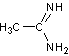
Groupe amidino |
Acétamidine |
Exemples
|
|
|
|
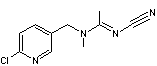
Acétamipride |
Thiaclopride |
·
Un groupe nitrométhylène =CH-NO2
Exemple
|
|
|
Nitenpyrame |
¾ Mais le groupe pyridyle n'est pas toujours présent.
On a cependant, le plus souvent, un groupement nitroguanidine
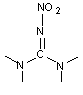
Exemples
|
|
|
|
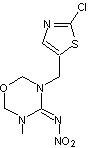
Clothianidine |
Thiamétoxame |
Remarque :
Le tableau ci-dessous fait apparaître une classification de
l'ensemble des molécules qui sont citées au paragraphe 3), et indique les groupes
que chacune de ces molécules possède.
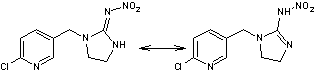
On peut remarquer que certaines d'entre elles possèdent deux
groupes, la molécule d'imidaclopride, par exemple, contient tant la partie
nitroguanidine que la partie pyridylméthylamine ; elles sont alors classées
dans deux catégories en fonction des groupes qu'elles ont.
Les flèches font apparaître les néonicotinoïdes appartenant à deux
catégories.
|
Classement |
Pyridyl méthyl amine (Pyr) |
Nitroguanidine (G) |
Nitrométhylène (M) |
Cyano amidine ( |
|
Néonicotinoïdes
nitroguanidines : |
Pyr |
G G G G G |
|
|
|
Néonicotinoïdes
nitrométhylène : |
Pyr |
|
M M |
|
|
Néonicotinoïdes
pyridilméthylamine : |
Pyr Pyr Pyr Pyr Pyr Pyr |
G |
M M M |
|
3) Dénomination des néonicotinoïdes
Cette famille est constituée essentiellement de 5 composés tous
obtenus par synthèse :
- L'acétamipride
- La clothianidine
- L'imidaclopride
- Le thiaclopride
- Le thiamétoxane
Ils ont
des propriétés insecticides et ont été utilisés comme tels (insecticides
systémiques) en traitement des semences, en granulés ou en pulvérisation.
Ils
sont interdits dans l'Union Européenne depuis septembre 2018 à cause d'effets
destructeurs notamment sur les abeilles.
En 2022
et pour 120 jours, l'emploi de semences de betteraves sucrières traitées avec
le thiamétoxane a été autorisé.
On en
connaît d'autres, également synthétiques, qui ont trouvé moins d'applications
que les 5 précédemment cités ; ce sont :
- Le
nitenpyrame
- Le
nithiazine
- Le
dinotéfurane
-
L'imidaclothiz
- Le
cycloxapride
- Le
paichongding
Nous
étudierons essentiellement les 5 composés principaux et nous dirons un mot des
autres.
4) Quelques propriétés des
5 composés principaux
Acétamipride – Clothianidine – Imidaclopride – Thiaclopride - Thiamétoxame
|
C10H11ClN4 Aspect : Poudre
blanche inodore Masse
molaire
: 222,674
g.mol-1 Fusion : 98,9°C Solubilité : Eau :
4,25 g/L à 25°C N°
CAS
: 135410-20-7
Isomère E 160430-64-8
Mélange Z/E Risques :
|
|
Composé
synthétique, utilisé comme insecticide (vigne, coton, agrumes, cerise,
feuillus, crucifères) et apparu sur le marché en 1995 sous la formulation Suprême
®. C'est
un neurotoxique pour les insectes ; il est actif sur les récepteurs de
l'acétylcholine de type nicotinique des neurones. L'utilisation
de cet insecticide fait courir un risque aigu aux abeilles (Efsa janvier
2013). Il
est interdit d'utilisation dans l'Union Européenne depuis septembre 2018. |
|
C6H8ClN5O2S Aspect : Poudre
incolore Masse
molaire
: 249,678
g.mol-1 Fusion : 176,8°C Solubilité : - Eau
: 340 mg/L à 20°C -
Acétone : 15,2 g/L à 20°C Densité : 1,61 N°
CAS
: 210880-92-5 Risques :
|
|
Insecticide
synthétique, systémique (racines) utilisé pour les cultures de riz, de maïs,
de fruits. C'est
un agoniste des récepteurs de l'acétylcholine ; c'est un métabolite du thiamétoxane. Il
est apparu sur le marché en 2001 sous la formulation Poncho ® L'utilisation
de cet insecticide fait courir un risque aigu aux abeilles (Efsa janvier
2013). Il
est interdit d'utilisation dans l'Union Européenne depuis septembre 2018. |
|
C9H10
ClN5O2 Masse
molaire
: 255,66
g.mol-1 Fusion : 144°C Ebullition : 442,3°C Densité : 1,54 N°
CAS
: 138261-41-3 Solubilité : 0,061
g pour 100mL à 20°C Risques :
|
|
Insecticide commercialisé en 1991 sous le nom de Gaucho
® par Bayer. C'est un neurotoxique systémique utilisé pour le traitement des
semences avant semis ou sur les feuilles des plantes (tournesol, riz, maïs,
céréales, légumes). C'est un perturbateur des synapses cholinergiques. Il est mis en cause dans la surmortalité des
abeilles. Des restrictions d'usage ont eu lieu dans l'UE dès
2004. Il est interdit d'utilisation dans l'Union
Européenne depuis septembre 2018. |
|
C10H9
ClN4S Masse
molaire
: 252,723
g.mol-1 N°
CAS
: 111988-49-9 Risques :
|
|
Propriétés insecticides : il agit sur les récepteurs de l'acétylcholine de type
nicotinique des neurones des insectes. Insecticide systémique utilisé contre les
pucerons, les aleurodes (mouches blanches), la mouche de l'olive ; il est
apparu sur le marché en 2000 sous la formulation Calypso ® et Exemptor ®. Il est mis en cause dans la surmortalité des
abeilles. Il est interdit d'utilisation dans l'Union
Européenne depuis septembre 2018. |
|
C8H10ClN5O3S Masse
molaire
: 291,715
g.mol-1 N°
CAS
: 153,719-23-4 Risques :
|
|
Insecticide systémique utilisé en agriculture
depuis son apparition en 1998 sous le nom de Cruiser ®, qui cible les
insectes suceurs de sève et ceux qui consomment les plantes cultivées. Son principal métabolite est le clothianidine. Il est mis en cause dans la surmortalité des
abeilles. Il est interdit d'utilisation dans l'Union
Européenne depuis septembre 2018. |
5) Quelques autres néonicotinoïdes
Leur mode
d'action est le même. Ils agissent sur le système nerveux central des insectes
entraînant la paralysie et la mort comme nous l'expliquerons au paragraphe
suivant..
Cependant
leur utilisation n'a pas été interdite dans l'Union Européenne en septembre 2018.
|
C11H15ClN4O2 Masse
molaire
: 270,716
g.mol-1 N°
CAS
: 150824-47-8 Risques :
|
|
Insecticide
utilisé en agriculture et en médecine vétérinaire pour éliminer les parasites
du bétail et des animaux de compagnie (en particulier chez les chiens et les
chats). Il
est classé comme néonicotinoïde nitrométhylène. |
|
Nithiazine (E/Z) ou (E/Z)-2-Nitrométhylène-1,3-thiazinane. C5H8N2O2S Masse
molaire
: 160,194
g.mol-1 Aspect Solide
cristallisé ou poudre brune Densité : 1,388 N°
CAS
: 58842-20-9 Risques :
|
|
Insecticide
utilisé principalement pour la lutte contre les mouches domestiques dans les
installations d'élevage d'animaux. Ce
n'est pas un inhibiteur d'acétylcholinestérase. Il
est classé comme néonicotinoïde nitrométhylène. |
|
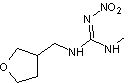
C7H14N4O3 Masse
molaire
202,211
g.mol-1 Fusion 107,5°C Solubilité 39,83
g.L-1 dans l'eau N°
CAS
: 165252-70-0 Risques
|
|
Néonicotinoïde
utilisé comme insecticide en agriculture et en médecine vétérinaire pour
éliminer les parasites du bétail et des animaux de compagnie (en particulier
chez les chiens et les chats). Il
peut être classé chimiquement dans les nitroguanidines. |
|
C7H8ClN5O2S Masse
molaire
261,69
g.mol-1 N°
CAS
: 105843-36-5 Risques
|
|
Insecticide
utilisé en agriculture (riz, tomates, citrons..) contre les ravageurs que
sont les pucerons, la cicadelle, la mouche blanche, la cicadelle du thé. Il
agit sur le système nerveux central des insectes entraînant la paralysie et
la mort. Il
peut être classé chimiquement dans les néonicotinoïdes nitroguanidines. |
|
C14H15ClN4O3 Masse
molaire
322,75
g.mol-1 N°
CAS
: 1203791-41-6 Risques
|
|
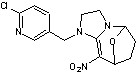
Néonicotinoïde
classé dans la catégorie nitrométhylène. Insecticide
efficace dans la lutte contre les parasites hémiptères (Aleurodes, cicadelles
…). |
|
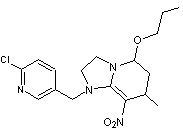
ou 1-[(6-chloropyridin-3-yl)méthyl]-7-méthyl-8-nitro-5-propoxy-3,5,6,7-tétrahydro-2H-imidazo[1,2-a]pyridine C17H23ClN4O3 Aspect Solide
jaune pâle Masse
molaire
366,842
g.mol-1 Solubilité
Soluble
dans le méthanol, légèrement soluble dans le chloroforme. N°
CAS 948994-16-9 Risques
|
|
Néonicotinoïde
classé chimiquement dans la catégorie pyridylméthylamine ; il agit sur le
système nerveux central des insectes entraînant la paralysie et la mort. Utilisé
en agriculture comme insecticide. |
6) Mode d'action des néonicotinoïdes
L'acétylcholine
![]()
est le
plus important neurotransmetteur (voir
annexe 1)
excitateur au sein du système nerveux central des insectes ; il joue un rôle
essentiel dans la transmission synaptique neuronale.
3 types
de récepteurs à l'acétylcholine (voir annexe 1) ont été identifiés
:
- de type muscarinique
- de type nicotinique
- de type "mixte"
(pharmacologie à la fois muscarinique et nicotinique).
Les
néonicotinoïdes ont pour cible les récepteurs à l'acétylcholine de type
nicotinique du système nerveux central. Ce sont,du fait de leur structure chimique,
des agonistes de ces récepteurs.
Ces
insecticides ne peuvent être dégradés par l'acétylcholinestérase de la fente
synaptique ; leur action se prolonge donc et conduit à une dépolarisation
permanente de la membrane, ce qui provoque chez l'insecte la paralysie, puis la
mort.
Remarque
1 :
La
présence d'un atome de chlore en position 2 dans le groupe pyridyle des
néonicotinoïdes qui le possèdent modifie l'hydrophobicité de ces molécules.
L'hydrophobicité joue un rôle important dans la pénétration de ces substances
dans le système nerveux central des insectes. On comprend alors le rôle de cet
atome de chlore dans l'activité insecticide des néonicotinoïdes.
Remarque
2 :
Les abeilles ne sont pas des espèces ciblées lors de l'utilisation des
néonicotinoïdes.
Des
études ont cependant permis de constater que l'ingestion involontaire de
thiamétoxame en quantité sublétale par des abeilles butineuses affecte de façon
significative leur capacité à s'orienter pour revenir à la ruche ; elles se
perdent et meurent. C'est en partie cette surmortalité qui est à l'origine de
l'interdiction qui a été prise dans l'Union Européenne de l'utilisation de ces
insecticides depuis septembre 2018.
7) Synthèse de quelques néonicotinoïdes
|
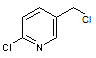
Il
est très souvent fait usage de 2-chloro-5chlorométhyl pyridine |
|
7-1) Imidaclopride
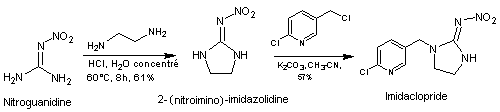
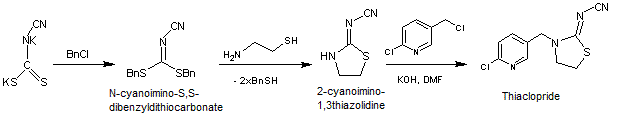
7-2) Thiaclopride
7-3) Acétamipride

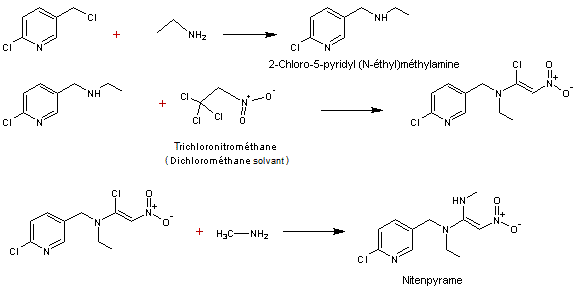
7-4) Nitenpyrame
Récepteurs – neurotransmetteurs –
Récepteurs nicotiniques
-
Récepteur :
Un récepteur est une structure située à la
surface d'une cellule et qui permet à des molécules appropriées (messagers chimiques)
de se fixer, ce qui déclenche une action spécifique sur la cellule. Ce sont en
général des protéines membranaires. Plus la concentration du messager est
grande plus la réponse est grande ; lorsque tous les récepteurs sont liés au
messager on dit qu'ils sont saturés.
- Neurotransmetteur
Molécule qui est libérée par un
neurone lors d'une stimulation et qui se fixe sur un récepteur d'une cellule
cible, déclenchant une action spécifique. Un exemple de neurotransmetteur :
l'acétylcholine.
-
Récepteur à l'acétylcholine de type nicotinique
Le récepteur de type nicotinique
est une protéine membranaire que l'on trouve au niveau de tous les
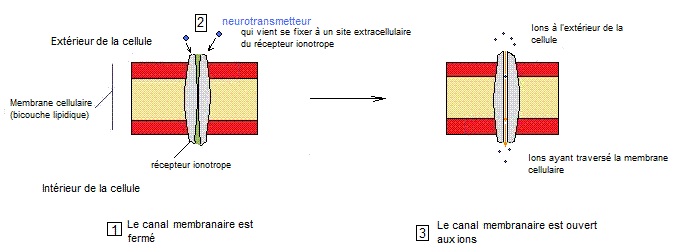
compartiments d'un neurone. C'est un récepteur canal ionotrope (il ouvre un
canal ionique lorsqu'un neurotransmetteur adapté se lie à lui). Il est peu
sélectif et perméable aux ions Na+, Ca2+ mais
aussi K+, Mg2+.
Son agoniste endogène est
l'acétylcholine, mais la nicotine est également un agoniste important.
Principe de fonctionnement d'un
récepteur canal ionotrope