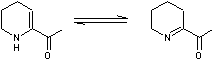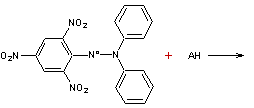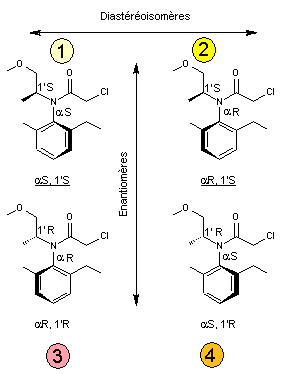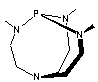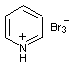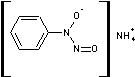MEDICAMENTS ET MOLECULES PARTICULIERES
(42)
|
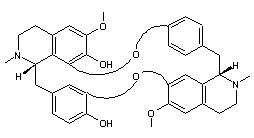
C36H38N2O6 Masse molaire 594,70 g.mol-1 Aspect Cristaux lorsque
recristallisé dans le benzène ou l'éthanol ou le mélange
chloroforme-méthanol. Fusion 221°C Solubilité Très soluble dans
l'acétone et le chloroforme ; soluble dans l'éthanol, le méthanol et l'éther. N° CAS 436-05-5 |
|
Alcaloïde naturel,
cyclique que l'on trouve dans l'écorce de Chlorocardium
rodiée utilisée en médecine comme substitut à
la quinine. |
||
|
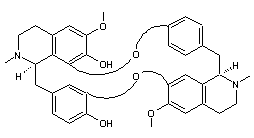
C36H38N2O6 Masse molaire 594,696 g.mol-1 Aspect Cristaux prismatiques
ou en aiguilles lorsque recristallisé dans le mélange chloroforme-méthanol. Fusion 221°C Solubilité Très soluble dans
l'acétone, le benzène ou la pyridine. N° CAS 436-05-5 |
|
La curine est un isomère de la bebeerine. La curine induit l’arrêt du cycle cellulaire et la mort
cellulaire dans les cellules de carcinome hépatocellulaire. |
||
|
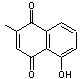
ou 5-hydroxy-2-méthyl-1,4-naphtoquinone. C11H8O3 Masse molaire 188,180 g.mol-1 Aspect Cristaux prismatiques
or ou aiguilles jaune-orange si recristallisé dans l'éthanol dilué. Fusion 78,5°C Solubilité Très soluble dans
l'acétone, le benzène, l'éther ou l'éthanol. N° CAS 481-42-5 |
|
Molécule existant
naturellement dans les racines de Plumbago zeylanica,
une plante médicinale et présentant une remarquable activité
anticancéreuse dans divers cancers humains. Elle induit un arrêt
du cycle cellulaire et une apoptose dans les cellules du carcinome
épidermoïde de l'œsophage. En outre elle possède
une activité antimicrobienne, anti-inflammatoire, hypolipidémique
et neuroprotectrice. |
||
|
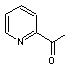
ou 1-(2-Pyridinyl) éthanone C7H7NO Masse molaire 121,1366 g.mol-1 Aspect Liquide incolore à
jaune clair dans l'air. Fusion 9,0°C Ebullition 192°C Indice de réfraction 1,5203 (20°C) Solubilité Soluble dans
l'éthanol, l'éther. N° CAS 1122-62-9 |
|
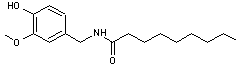
Odeur douce de
noisette, de popcorns, d'amande, de pain cuit. Cette molécule se forme dans
ces aliments cuits, par réaction de Maillard. |
||
|
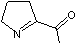
C7H11NO Masse molaire 125,168 g.mol-1 N° CAS 27300-27-2 |
|
Odeur de pain cuit,
de popcorns comme la 2-acétylpyridine dont elle
dérive. Cette substance se
forme dans ces aliments cuits, par réaction de Maillard. |
||
|
C6H9NO Masse molaire 111,1418 g.mol-1 N° CAS 85213-22-5 |
|
Cette molécule à une
odeur de pain cuit, donne son odeur à certaines variétés de riz (Basmati par
exemple) … Cette molécule se forme dans ces aliments cuits, par réaction de
Maillard. |
||
|
C9H16O Masse molaire 140,2227 g.mol-1 Aspect Liquide Densité 0,904 Indice de réfraction 1,447 Solubilité dans l'eau 1,64g/L N° CAS 2408-37-9 |
|
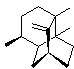
C'est une cétone
cyclique Molécule présente
dans Cistus ladaniferus.On
la trouve aussi dans différents fruits et différentes boissons dont le thé. |
||
|
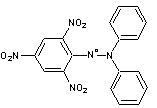
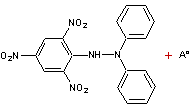
2,2-Diphényl-1-picrylhydrazyle ou DPPHO
radical C18H12N5O6 Aspect Poudre cristalline de
couleur foncée. Masse molaire 394,3178 g.mol-1 N° CAS 1898-66-4 |
Test DPPHO
On peut apprécier la réduction du DPPH° par
spectrométrie à 515 nm. |
Radical relativement
stable, de couleur violette qui devient jaune par réduction (il devient du
DPPH-H). Le test DPPHO
permet de mesurer l'aptitude d'un antioxydant comme par exemple un composé
phénolique à réduire le DPPHO et mesure donc le pouvoir
antiradicalaire de molécules ou d'extraits végétaux dans un système donné. |
||
|
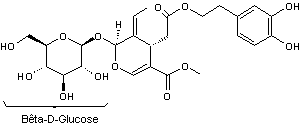
C25H32O13 Masse molaire 540,514 g.mol-1 N° CAS 32619-42-4 |
|
Diphénol présent dans
les olives et responsable de leur amertume. Pour rendre
mangeables les olives brutes, il faut les rincer avec une solution de soude
très diluée puis après rinçage à l'eau, les tremper dans de la saumure. |
||
|
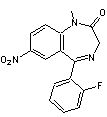
ou Flunitrazépam C16H12
FN3O3 Masse molaire 313,283 g.mol-1 N° CAS 1622-62-4 |
|
Benzodiazépine
prescrite autrefois dans les cas d'insomnies sévères. N'est plus prescrite en
France. |
||
|
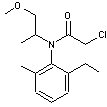
ou (α
R, 1'S) -N- (1'méthyl -2'- méthoxyéthyl) -N- (chloroacétyl) -2- éthyl -6- méthylaniline C15H22
ClNO2 Masse molaire 283,794 g.mol-1 Aspect Liquide huileux
blanchâtre à légèrement coloré. Fusion -62,1°C Solubilité dans l'eau : 490 mg/L (25°C) Densité 1,12 à 20°C N° CAS 51218-45-2 |
Deux éléments de chiralité : - Un atome de carbone asymétrique (1') et un axe chiral
entre le cycle aromatique et l'atome d'azote (a) qui empêche la rotation autour de la liaison ; cela
conduit à 4 stéréoisomères.
Les stéréoisomères 1 et 2 sont "S". Ce sont
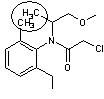
eux qui ont un caractère herbicide. Remarque : Le schéma ci-dessous permet de visualiser l'empêchement
stérique à la libre-rotation autour de la liaison cycle aromatique – atome
d'azote qui explique le deuxième élément de chiralité :
|
Herbicide agissant
sur les graminées (maïs en particulier). Seuls les stéréoisomères S du
carbone asymétrique sont actifs. C'est un
micropolluant des eaux usées. |
||
|
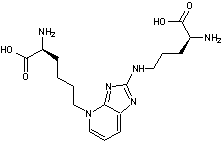
C17H26
N6O4 Masse molaire 378,433 g.mol-1 Densité 1,47 à 20°C N° CAS 124505-87-9 |
|
Résulte de la
réaction du ribose (un pentose) avec les protéines (réaction de Maillard). C'est un AGE (produit
terminal de glycation) marqueur du stress oxydant et de l'hyperglycémie. Il
est facilement détectable car fluorescent. |
||
|
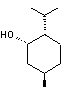
ou (1S,2S,5R)-(+)-Néomenthol ou (1S,2S,5R)-2-Isopropyl-5-méthylcyclohexanol C10H20O Masse molaire 156,265 g.mol-1 Aspect Huile Densité 0,897 à 22°C Fusion -22°C Ebullition 211,7 Indice de réfraction nD20 = 1,4600 N° CAS 2216-52-6 |
|
C'est un
monoterpénoïde que l'on trouve dans Mentha
piperita L. Cet isomère du
menthol est en général utilisé comme additif dans des produits d'hygiène
bucco-dentaire et comme agent de saveur dans des boissons ou de la
nourriture. |
||
|
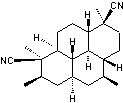
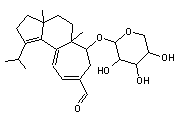
7,20-Diisocyanoadociane |
|
Le
7,20-diisocyanoadociane est un métabolite marin rare avec une activité
antipaludique significative notamment contre les stades hépatiques du
parasite Plasmodium. C’est un diterpène
polycyclique possédant deux groupes isocyanate. |
||
|
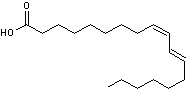
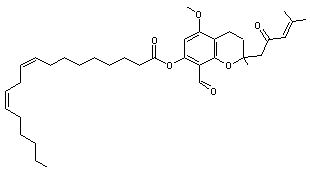
C18H32O2 Masse molaire 280,445 g.mol-1 N° CAS 1839-11-8 |
|
Acide gras en C18,
di-insaturé, cis en C9 et trans en C11 qu'on peut désigner par 18:2 D9c,11t. Les deux doubles
liaisons sont conjuguées. On le trouve dans les
graisses des ruminants et les produits laitiers, car il se forme dans la
panse des animaux lors de la rumination. |
||
|
C18H34O2 Masse molaire 282,461 g.mol-1 N° CAS 693-72-1 |
|
Acide gras mono-insaturé, trans, qu'on peut désigner par 18:1 D11t. On le trouve dans les
graisses des ruminants et les produits laitiers, car il se forme dans la
panse des animaux lors de la rumination. On en trouve dans le lait humain ;
il est probablement dû à l'alimentation. |
||
|
ou Acide heptanoïque C7H14O2 Masse molaire 130,185 g.mol-1 Aspect Liquide Densité 0,9124 à 25°C Fusion -7,17°C Ebullition 222,2°C Indice de réfraction nD20 = 1,4170 Solubilité Soluble dans
l'éthanol, l'éther et l'acétone ; légèrement soluble dans l'eau. N° CAS 111-14-8 |
|
Acide utilisé dans
l'industrie des arômes pour la synthèse d'esters. Il contribue à
l'odeur de rance de certaines huiles. On le désigne par C7:0. |
||
|
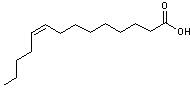
Acide myristoléique ou Acide 9-tétradécènoïque C14H26O2 Masse molaire 226,355 g.mol-1 Aspect Liquide Fusion -4,0°C Ebullition 144°C N° CAS 13147-06-3 |
|
Acide gras mono-insaturé cis qu'on peut désigner par 14:1 D9c. Peu présent dans le
milieu naturel ; les graines de muscadier par exemple en contiennent 30%
environ. Le muscadier est un arbre tropical originaire des îles Moluques
produisant la noix muscade. |
||
|
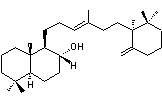
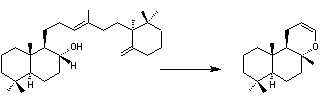
C30H52O Masse molaire 428,733 g.mol-1 N° CAS 8016-26-0 |
Ambréine
Dégradation
oxydante
|
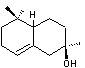
L'ambre gris est à
l'origine une sécrétion intestinale du cachalot qui est récoltée en mer ou
sur les rivages des îles de Sumatra, Madagascar et des côtes du Pacifique.
Cette substance, qui se présente sous forme d'un solide gris, est un mélange
de plusieurs constituants dont le principal est un terpénoïde,
l'ambréine. L'ambréine est un précurseur d'éthers polycycliques formés après
dégradation oxydante. |
||
|
C30H52O Masse molaire 428,733 g.mol-1 N° CAS 41199-19-3 |
|
Produit synthétique
utilisé en parfumerie pour reproduire l'odeur de l'ambre gris naturel. Cette molécule
entrait dans la composition de l'ambre gris naturel, une sécrétion
intestinale du cachalot. Son odeur est classée
par les parfumeurs comme "note animale et ambrée". |
||
|
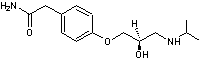
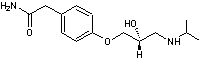
C14H22N2O3 Masse molaire 266,336 g.mol-1 Fusion 147°C N° CAS 29122-68-7 |
(R)
(S) |
C'est un
bêta-bloquant utilisé pour lutter contre l'hypertension artérielle,
l'infarctus du myocarde …. C'est un antagoniste
des récepteurs β1 responsables de l'augmentation de la
fréquence cardiaque. |
||
|
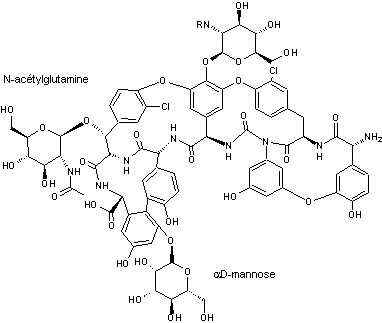
C58H42
Cl2N7O18 Masse molaire 1195,896 g.mol-1 N° CAS 61036-62-2 |
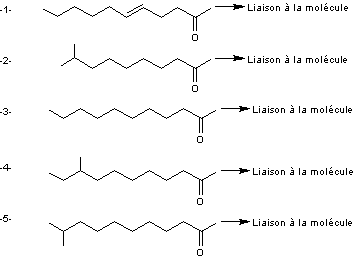
Différentes molécules suivant la nature de R-
|
Antibiotique de la
classe des glycopeptides ; en se fixant sur les peptides précurseurs de la
paroi bactérienne il bloque la transpeptidation (conversion d'un peptide en
un autre par une protéase). Son spectre
antibactérien est limité aux bactéries à Gram positif, aérobie ou anaérobies. |
||
|
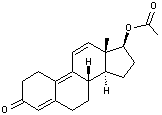
ou 17-acétate de
17β-hydroxyestra-4,9,11-trièn-3-one. C20H24
O3 Masse molaire 312,403 g.mol-1 N° CAS 10161-34-9 |
|
Stéroïde anabolisant
synthétique, fabriqué à l'origine pour accélérer la croissance de la masse
musculaire des bovins. Ce produit est interdit dans l'Union Européenne mais
autorisé aux USA et au Canada. C'est un agoniste des
récepteurs des androgènes. |
||
|
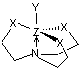
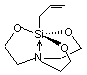
Exemples : - Allylsilatrane (Z = Si ; X = O ; Y = -CH2
–CH=CH2)
- Azaphosphatrane (Z = P ; X = N-R ;
Y = H)
|
On appelle ainsi
toute classe d'hétérocycle tricyclique ayant une liaison dative transannulaire entre un azote et un autre hétéroatome. Ce nom leur a été
donné par le chimiste russe Mikhail Grigorievitch Voronkov (Institut de chimie organique d'Irkoutsk en
1988). |
|||
|
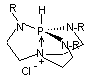
Base
de Verkade |
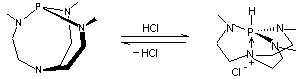
Proazophosphatrane
Equilibre entre les deux formes |
Superbase (Base extrêmement
forte, de basicité supérieure à celle que possède l'ion HO- dans
l'eau) non nucléophile, que l'on utilise en synthèse organique. Sa structure est de
type proazophosphatrane (c'est-à-dire un azaphosphatrane sans liaison
centrale entre le phosphore et l'azote). On remarque que c'est
le phosphore qui est protoné et non l'azote lorsque le chlorure d'hydrogène
réagit sur le proazophosphatrane. Cette base porte le
nom du chimiste qui l'a découverte. John G Verkade est un chimiste américain qui a enseigné
notamment à l'Université de l'état de l'Iowa. |
||
|
C9H10O3 Masse molaire 166,174 g.mol-1 Fusion 77°C Ebullition 285°C Densité 1,186 Solubilité Soluble dans l'eau,
l'éthanol, l'éther, le chloroforme. N° CAS 121-32-4 |
|
Molécule de synthèse
qui a un parfum proche de celui de la vanille ; elle est utilisée dans la
parfumerie et l'alimentation. |
||
|
ou Acide oxoacétique C2H2O3 Masse molaire 74,035 g.mol-1 Fusion 98°C Solubilité Très soluble dans
l'eau ; légèrement soluble dans l'éthanol, l'éther, le benzène. N° CAS 298-12-4 |
|
Un des acides
carboxyliques en C2, possédant aussi une fonction aldéhyde. Il peut être
synthétisé par oxydation nitrique de l'éthanedial
ou par ozonolyse de l'acide maléique. Possède un rôle
biologique important pour les plantes (cycle du glyoxylate)
notamment dans l'induction des mécanismes de défense des plantes en réponse
aux champignons. |
||
|
C7H9O Aspect Solide blanc (plaques
cristallisées dans le système orthorhombique) Masse molaire 123,152 g.mol-1 Fusion 57,2°C Ebullition 243°C Densité 1,071 à 57°C Indice de réfraction 1,5559 à 60°C (raie D du sodium) Solubilité Très soluble dans
l'éthanol, l'éther ; soluble dans l'eau, l'acétone, le benzène. N° CAS 104-94-9 |
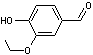
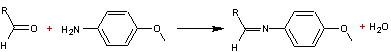
Condensation
de la p.anisidine avec un
aldéhyde en milieu acide
L'imine obtenue absorbe vers 350 nm. A cette longueur
d'onde, l'absorbance est proportionnelle à la concentration de l'imine (Loi
de Beer-Lambert), elle-même proportionnelle à la quantité d'aldéhyde ayant
réagi. On établit au préalable une courbe d'étalonnage avec des quantités
connues d'aldéhyde. |
Molécule utilisée
pour détecter et doser les aldéhydes non volatils dans les huiles et les
corps gras, qui se forment par évolution des peroxydes et qui donnent une
odeur et un goût de rance à ces matières grasses. Le principe du dosage
est la condensation de la para-anisidine avec les aldéhydes pour donner une
imine (base de Schiff) qui absorbe à 350 nm. La préparation de la p.anisidine se fait par
réduction du 4-nitroanisole. |
||
|
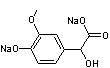
Acide 4-hydroxy-3-méthoxymandélique Sel disodique ou SDM C9H8 Na2O5 Masse molaire 242,136 g.mol-1 N° CAS 2394-20-9 (pour
l'acide correspondant). |
SDM
Obtention
du SDM
|
Molécule obtenue par
réaction de condensation entre le gaïacol et l'acide glyoxylique en présence
de soude, à 35°C. Après oxydation ce
composé conduit à la vanilline. |
||
|
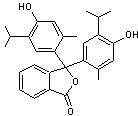
C28H30O4 Aspect Prismes ou aiguilles
lorsque recristallisé dans l'éthanol. Masse molaire 430,536 g.mol-1 Fusion 253°C pKa 10,1 Solubilité Soluble dans
l'éthanol, l'éther,l'acétone
; légèrement soluble dans le DMSO ; insoluble dans l'eau. N° CAS 125-20-2 |
|
Substance dont la
couleur dépend du pH ; utilisée comme indicateur coloré. Rouge en milieu très
acide, incolore en milieu acide ,bleue en milieu
basique. Sa zone de virage se
situe entre 9,3 et 10,5. |
||
|
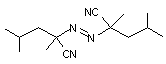
2,2'-Azobis(2,4-diméthyl)valéronitrile ou AMVN C14H24N4 Masse molaire 248,37 g.mol-1 Fusion 45-70°C Ebullition 330,6°C Densité 0,93 N° CAS 4419-11-8 |
|
Solide blanc, sans
odeur. Initiateur de
radicaux utilisé dans les polymérisations radicalaires au même titre que l'AIBN (azobisisobutyronitrile). |
||
|
Pyridinium
tribromure C14H24N4 Aspect Solide cristallisé
rouge Masse molaire 319,82 g.mol-1 N° CAS 39416-48-3 |
Il est composé du cation pyridinium et de l'anion
tribromure. Il peut être préparé en faisant réagir le bromure de
pyridinium sur le dibrome. |
C'est un composé
donneur de dibrome, l'ion tribromure
étant engagé dans l'équilibre : Br3+(aq) = Br2 (aq)
+ Br- (aq) Il permet la bromation des phénols, des cétones et des éthers
notamment. |
||
|
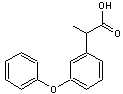
C15H14O3 Masse molaire 242,270 g.mol-1 N° CAS 29679-58-1 |
|
Anti-inflammatoire
non stéroïdien (AINS) notamment utilisé sous sa forme calcique pour soulager
la polyarthrite rhumatoïde et l'arthrose. Son nom commercial est Nalgésic. |
||
|
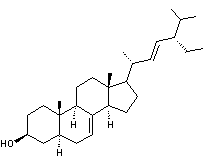
C29H48O Aspect Solide cristallisé Masse molaire 412,702 g.mol-1 Fusion 169°C N° CAS 481-18-5 |
|
Phytostérol que l'on
trouve dans différents végétaux dont les épinards d'où il tire son nom. On l'a trouvé dans Gordonia ceylanica de
la famille des Theaceae (Sri Lanka) ou dans Medicago
sativa (nom commun alfalfa ou luzerne). |
||
|
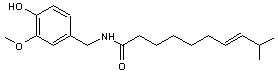
Famille d'Alcaloïdes
voisins de la capsaïcine. |
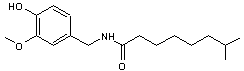
Dihydrocapsaïcine (C18H29NO3) Présent à 20% dans Capsicum
anuum
Nordihydrocapsaïcine (C17H27NO3) Présent à 7% dans Capsicum
anuum
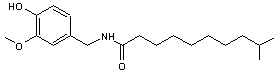
Homodihydrocapsaïcine (C19H31NO3) Présent à 1% dans Capsicum
anuum Homocapsaïcine (C19H29NO3) Présent à 1% dans Capsicum
anuum
|
Ces composés activent
les récepteurs vanilloïdes (nocirécepteurs) VR1 de
la peau, de la langue, de la vessie, par exemple, qui sont aussi activés par
la chaleur (45°C) et par l'acidité. Les capsaïcinoïdes
provoquent donc une douleur (sensation de piquant sur la langue, de brûlure
sur la peau) au début, mais par contact prolongé, ils désensibilisent ces
récepteurs entraînant un effet analgésique. |
||
|
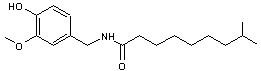
ou Pseudocapsaïcine ou Vanillylamide C17H27NO3 Aspect Poudre blanche à
blanc cassé à odeur piquante. Masse molaire 293,401 g.mol-1 Fusion -57°C Densité 1,1 (à 25°C) Solubilité Soluble dans le
méthanol (100g/L) ; insoluble dans l'eau N° CAS 2444-46-4 |
|
Composé très stable
thermiquement, semblable à la capsaïcine et utilisé en substitution à
celle-ci. Existe en quantité très faible dans le piment. La plupart du temps
le nonivamide est d'origine synthétique. |
||
|
C15H24 Masse molaire 204,351 g.mol-1 N° CAS 20085-93-2 |
|
Hydrocarbure
sesquiterpénique, composé minoritaire de l'huile essentielle de patchouli (Pogostemon cablin)
utilisé en parfumerie et en cosmétologie. Le patchouli est un
grand arbuste de la famille des lamiacées, que l'on trouve en Chine, en
Indonésie et aux Philippines, à larges feuilles duveteuses portées par une
tige velue, desquelles on extrait l'huile essentielle. |
||
|
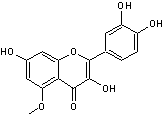
C16H12O7 Aspect Solide cristallisé en
aiguilles jaune clair. Masse molaire 316,262 g.mol-1 N° CAS 529-51-1 |
|
Flavonol présent dans de
nombreuses espèces de rhododendrons. |
||
|
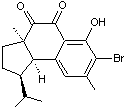
C18H21BrO3 Masse molaire 365,262 g.mol-1 |
|
Molécule que l'on
trouve dans les éponges marines Hamigera,
de la famille Hymedesmiidae vivant dans des
eaux peu profondes au large de la Nouvelle-Zélande. C'est un agent
antiviral puissant en raison de son activité inhibitrice prononcée contre la
polio et le virus de l'Herpès. |
||
|
C36H52O6 Masse molaire 580,794 g.mol-1 |
|
Molécule que l'on
trouve dans l'hydne hérisson (Hericium erinaceus), un champignon cultivé surtout en
Chine et au Japon où il porte le nom de yamabushi.
A l'état naturel (il est répandu dans l'hémisphère nord) c'est un parasite
des feuillus. Ce champignon est comestible lorsqu'il est jeune. Des études montrent
que l'héricénone favorise in vitro, la
synthèse du NGF (Neuronal Growth Factor) qui peut
permettre la régénération des cellules nerveuses. |
||
|
C25H36O6 Masse molaire 432,550 g.mol-1 |
|
Molécule que l'on
trouve dans l'hydne hérisson (Hericium erinaceus), un champignon cultivé surtout en
Chine et au Japon où il porte le nom de yamabushi.
A l'état naturel (il est répandu dans l'hémisphère nord) c'est un parasite
des feuillus. Ce champignon est comestible lorsqu'il est jeune. Des études montrent
que l'héricénone favorise in vitro, la
synthèse du NGF (Neuronal Growth Factor) qui peut
permettre la régénération des cellules nerveuses. |
||
|
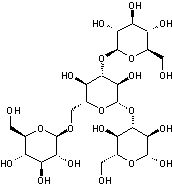
ou Schizophyllan C24H42O21 Masse molaire 666,578 g.mol-1 N° CAS 9050-67-3 |
|
Polysaccharide
extracellulaire produit par Schizophyllan
commune. C'est un β-1,3- beta-glucan avec des
ramifications β-1,6. |
||
|
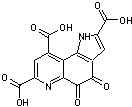
ou Méthoxatine ou PQQ C14H6N2O8 Masse molaire 330,206 g.mol-1 N° CAS 72909-34-3 |
|
Selon l'Académie de
médecine c'est une "quinone naturelle associée à certaines quinoprotéines ayant une activité enzymatique-oxydasique,
auprès desquelles elle joue le rôle de coenzyme". Dit autrement, c'est
un cofacteur utilisé par certaines enzymes d'oxydo-réduction comme par
exemple l'alcool déshydrogénase. Cette molécule peut
être isolée de cultures de bactéries méthylotropes,
de tissus de mammifères. Cette molécule a des
effets antioxydants et neuroprotecteurs. Elle a une très
grande stabilité moléculaire et neutralise une grande quantité de radicaux,
comme par exemple, O2.- et hydroxyle HO.. |
||
|
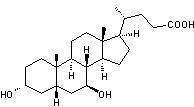
Acide
ursodéoxycholique ou Acide ursodésoxycholique ou Ursodiol C24H40O4 Masse molaire 392,572 g.mol-1 Fusion 203°C N° CAS 128-13-2 |
|
Acide biliaire
secondaire produit par les bactéries intestinales chez l'homme. Il tire son
nom du fait qu'il a été identifié la première fois dans la bile d'ours du
genre Ursus. C'est un épimère de l'acide chénodéoxycholique. Son administration
modifie la composition de la bile et peut dissoudre des calculs biliaires. Cette molécule est
employée comme cholagogue et cholérétique. |
||
|
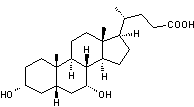
C24H40O4 Masse molaire 392,572 g.mol-1 N° CAS 474-25-9 |
|
Acide biliaire
primaire dont le précurseur est le cholestérol. C'est un épimère de
l'acide ursodéoxycholique
au niveau du OH sur le carbone n° 7. Cette molécule est
utilisée dans le traitement de la xanthomatose cérébrotendineuse
une maladie se caractérisant par une accumulation de cholestérol et de cholestanol dans l'organisme en particulier dans le
système nerveux central et les tendons. |
||
|
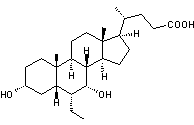
ou Acide 6-éthyl chénodéoxycholique C26H44O4 Masse molaire 420,625 g.mol-1 Fusion 109°C N° CAS 459789-99-2 |
|
Acide biliaire
synthétique voisin de l'acide chénodéoxycholique. C'est un stimulateur
du récepteur farnésoïde X, une protéine de la super
famille des récepteurs nucléaires (protéines actives dans le noyau des
cellules). |
||
|
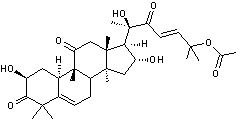
C32H46O8 Masse molaire 558,702 g.mol-1 Fusion 181°C N° CAS 6199-67-3 |
|
Composé de la famille
des cucurbitacines, substances présentes dans
certaines cucurbitacées auxquelles elles donnent un goût amer ; à structure
stéroïdique ces molécules rendent les plantes qui en contiennent cytotoxiques
et vénéneuses ; elles ne doivent pas être consommées. |
||
|
C32H48O8 Masse molaire 560,718 g.mol-1 Fusion 207,5°C N° CAS 5988-76-1 |
|
Composé de la famille
des cucurbitacines, substances présentes dans
certaines cucurbitacées auxquelles elles donnent un goût amer ; à structure
stéroïdique ces molécules rendent les plantes qui en contiennent cytotoxiques
et vénéneuses ; elles ne doivent pas être consommées. |
||
|
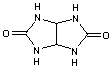
C4H6N4O2 Masse molaire 142,118 g.mol-1 N° CAS 496-46-8 |
Obtention
du glycolurile
|
Composé obtenu par
réaction de deux molécules d'urée sur une molécule de glyoxal. Les molécules de glycolurile servent à la synthèse des macrocycles cucurbituriles. |
||
|
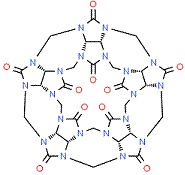
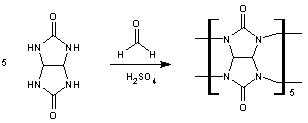
Cucurbit[5]urile obtention du CB[5]
|
Macrocycles ainsi
nommés car leurs molécules ressemblent à des citrouilles (cucurbitacées). Ce sont des unités glycoluriles séparées par des –CH2-. Ils sont couramment
désignés par CB[n], n indiquant le nombre d'unités glycoluriles. Ce sont des molécules
cages que l'on peut insèrer dans une matrice de
polymère pour constituer des canaux (membranes sélectives utilisées dans les
applications de l'osmose). |
|||
|
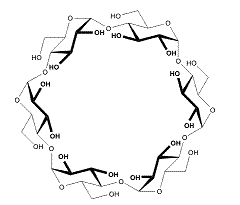
Elles sont formées par
dégradation enzymatique de l'amidon. Elles sont
consommables par l'homme et considérées comme des additifs alimentaires ;
leur utilisation est réglementée : α-CD : E 457 β-CD : E 459 γ-CD : E 458 De nombreux dérivés
peuvent être obtenus à partir des cyclodextrines naturelles ; ainsi les
groupements hydroxyles des glucopyranoses peuvent être aminés, estérifiés ou
éthérifiés dans le but d'augmenter la solubilité. |
α-CD C36H60O30 M = 972,8 g.mol-1 N° CAS : 10016-20-3 Solubilité : 145 g.L-1 (25°C) Forme des cyclodextrines : tronc-conique.
Remarque :
pour les β et γ cyclodextrines ces mêmes caractéristiques sont : β : H 0,79 nm
- Diamètres : 0,60 et 0,65
nm -
Volume : 0,262 nm3 γ : H 0,79
nm -
Diamètres : 0,75 et 0,83 nm
- Volume : 0,427 nm3
|
Oligomère ou polymère
cyclique constitué d'un enchaînement de n groupes glucopyranose (C6H10O5)n liés en (1-4), structure de l'amylose. Si n est petit (de 6 à
8) on a un oligomère qui a les propriétés des molécules-cages ; si n est
beaucoup plus grand (20, 30), on est en présence d'un polymère qui n'a plus
cette propriété. On désigne parfois les
cyclodextrines par CD. Celles à 6 chaînons par α-CD, celles à 7 chaînons
par β-CD et celles à 8 chaînons par γ-CD. Utilisations : Elles sont nombreuses
; en général elles permettent d'encapsuler diverses molécules. Dans le domaine des
cosmétiques elles permettent de stabiliser un produit en augmentant la
solubilité des composés dans une crème à base d'eau. Dans le domaine
pharmaceutique, elles constituent des excipients multifonctionnels,
biodégradables, non toxiques ; elles permettent la traversée des membranes
des cellules par des médicaments hydrophobes logées dans leur cavité. Des cyclodextrines
réticulées sont utilisées pour la réalisation de membranes permettant des
filtrations notamment dans le domaine des micropolluants ; elles permettent
de retenir des produits pharmaceutiques, des pesticides, des métaux lourds
des phénols, des phtalates des PCB notamment. |
||
|
ou sel d'ammonium du N-nitroso-N-phénylhydroxylamine C6H9N3O2 Aspect Cristaux jaune clair Masse molaire 155,155 g.mol-1 N° CAS 135-20-6 |
|
Utilisé comme
complexant d'ions métalliques en formant un chélate à 5 atomes. Il permet de séparer
le cuivre, le fer et le vanadium des autres métaux. Il a été découvert par
Baudisch (1881-1950 un biochimiste
Austro-Américain). Il donne avec le fer,
le titane, le cuivre, le zirconium, l'uranium des complexes insolubles en
milieu acide tandis que l'alumine, le manganèse, le zinc, le chrome ne
donnent pas de précipité. |