LE SUCRE
(Wolfgang WERNER – Münster)
Photosynthèse :
Les plantes vertes tirent l’énergie
dont elles ont besoin pour vivre et se développer de la lumière du soleil et
produisent des substances, à partir du dioxyde de carbone puisé dans l’air et à
partir de l’eau, selon l’équation suivante :
![]()
Parce que la formule brute de la
plupart de ces substances, fait apparaître hydrogène et oxygène dans les
mêmes proportions que dans l’eau K.Schmidt leur a donné en 1844 le nom d'hydrates
de carbone. A cause de la saveur particulière de quelques unes on les a
aussi appelées sucres ; on continue parfois à employer ce terme, mais on
utilise aujourd'hui en France l'appellation glucides.
Saccharose :
Le sucre
destiné à l’usage domestique se présente sous forme de petits cristaux, c’est
pourquoi on parle de sucre cristallisé. De plus gros cristaux, obtenus
par une lente cristallisation, sont connus sous le nom de sucre candi. Les
cristaux de sucre appartiennent au système de cristallisation
monoclinique.Le terme « candi » vient de l’arabe qandi (sucre
cristallisé). On parle encore de « sucre raffiné» : le sirop obtenu par
concentration du jus sucré provenant de la canne ou de la betterave à sucre
tire sa couleur brune des produits de la réaction de Maillard ; le sucre
cristallisé à partir de ce sirop est lui aussi de couleur brune, du fait des
restes de sirop qu’il contient – on parle alors de sucre brun – et ne
devient du sucre blanc qu’après avoir subi un traitement (notamment une recristallisation). L’ensemble des processus de traitement
est appelé raffinage. Le reste de sirop forme la mélasse. Celle–ci est utilisée
comme fourrage, une partie peut également être transformée par
fermentation en éthanol. Dans le vocabulaire scientifique, le sucre est
appelé saccharose (du latin saccharum et du grec saccheron).On
rencontre aussi parfois l’appellation « sucrose ». La terminaison – ose permet
de désigner certains glucides.
Le saccharose
est l’un des sucres formés au cours de la photosynthèse. Il est très aisément
soluble dans l’eau : 200g dans 100ml à 20°C (à 100°C : 400g dans 100ml) et, de
ce fait, il circule facilement dans les plantes afin de leur fournir l’énergie
qui leur est nécessaire. Toutefois, cette substance fixe de grandes quantités
d’eau et influe de ce fait sur l’équilibre osmotique. La teneur en saccharose
de la sève des plantes n’excède par conséquent guère plus de 15%.
Illustration
1
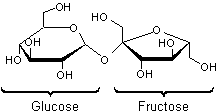
Le saccharose
|
|
|
α-D-glucopyrannosyl-β-D-fructofurannose |
La formule
de structure montre bien, que le saccharose est formé à partir de deux glucides
simples. C’est pourquoi on le considère comme un disaccharide.
Les deux oses
élémentaires sont chacun formés de six atomes de carbone (on les appelle par
conséquent « hexoses »). Lorsqu’on les rencontre individuellement (et non
groupés), on parle alors de monosaccharide.
Fructose :
L’un de ces
deux oses, appelé fructose (littéralement «
sucre de fruit »), est lui aussi aisément soluble dans l’eau (375g dans 100ml à
20°C) et peut, par voie enzymatique être transformé en l’autre ose élémentaire,
appelé glucose. La transformation inverse (du glucose en fructose) est elle
aussi possible.
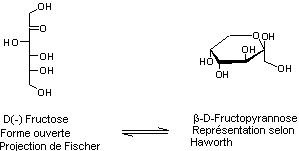
La forme
ouverte montre bien que le fructose contient un groupe cétone (d’où le nom
générique de « cétose »). A l’état solide, le groupe carbonyle forme avec le
groupe hydroxyle (en C5) un acétal cyclique
pentagonal.
Et comme le furanne
constitue le cycle de base du fructose, ce dernier s’avère le plus connu des
furannoses.
Illustration 2 : Le fructose
|
|
Glucose :
L’autre
monosaccharide, le « sucre de raisin » ou
glucose, a été découvert en 1792 par Lowitz sur des grappes de raisin.
L’appellation scientifique glucose a été forgée en 1838 par Jean–Baptiste Dumas
(1800-1884) à partir de la racine grecque glykos (« doux »). Friedrich
August Kekulé von
Stradonitz (1829-1896) trouva l’appellation dextrose (du latin dexter,
droit) plus appropriée, du fait qu’une solution de glucose possède la propriété
physique de faire tourner vers la droite le plan de la lumière polarisée linéairement.
Une solution de fructose quant à elle fait basculer le plan de la lumière
polarisée vers la gauche. C’est pourquoi on qualifie également le fructose de
lévulose (du latin laevus, gauche).
Le glucose se
dissout lui aussi aisément dans l’eau (82g dans 100 ml à 25°C).
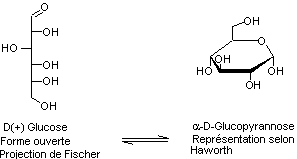
Illustration n° 3 : Le glucose.
|
|
Dans la représentation de Fischer, l’atome de carbone
ayant le plus grand degré d’oxydation est écrit en haut, et les autres en
dessous. La représentation d’Emil Fischer (1852–1919) est bien adaptée à la
forme ouverte.
Les initiales D
(dexter) ou L (laevus) indiquent la configuration
de la molécule. Les signes + ou - placés entre parenthèses, indiquent
eux, le sens de rotation qu'apporte la molécule au plan de la lumière
polarisée.
Tous les oses
qui comme le glucose ont un groupe aldéhyde (placé en haut de la molécule) sont
appelés "aldoses".
Illustration n° 4 : Les anomères du glucose
Le groupe carbonyle du glucose forme,
avec le groupe OH en C5 un hémiacétal
intramoléculaire. On appelle pyrannoses les oses dont le cycle de base est
celui du pyranne
.
Le groupe OH voisin de l'oxygène du cycle peut lors de la cyclisation se placer
de manière axiale (α) ou équatoriale (β), le cycle hexagonal étant en forme chaise. Dans la représentation de Haworth (1883-1950)
cela correspond à la position du OH du carbone C1 en trans par rapport au CH2OH (α) et en position cis pour (β).
La cyclisation a fait apparaître sur le carbone C1 un nouveau centre de
chiralité et donc des diastéréoisomères,
que l’on appelle encore anomères.
Le glucose solide se présente sous la forme α–D–glucopyrannose. Une solution de glucose lorsqu'elle vient d'être préparée, a un angle de rotation de +112°. Quelques instants après, l’angle de rotation est de +53°. On appelle « mutarotation » (du latin mutatio, changement) une telle modification de l’angle de rotation. Grâce à la forme ouverte, que l’on ne rencontre qu’en faible quantité, un équilibre s’est établi, entre les deux formes α et β dans le rapport suivant : α(36%) : β(64%). Le β–D–glucose a une valeur de l'angle de rotation de +19°. La valeur de l'angle rotation de la solution à l'équilibre résulte de l'addition des rotations qu'apporte chacune des substances présentes.
Illustration
n° 5
:La mutarotation
Si l’on ajoute
un peu d’acide (H+) à une solution de saccharose, on constate que le
signe de l’angle de rotation change : la rotation qui était initialement
de +66°, devient -20° . On appelle ce processus « inversion » (du latin inversio)
: le saccharose s’hydrolyse en ses composés, le glucose (+52°) et le fructose
(–92°). Le mélange est appelé « sucre inverti » ; les valeurs des angles de
rotation sont additives. Une scission par une enzyme peut
aussi s’opérer comme par exemple dans l’estomac des abeilles lors de la
fabrication du miel. Une crème composée de sucre inverti fut commercialisée
comme « miel artificiel » dans les années 1940.
Amidon :
L’amidon
(amylum) est insoluble et n’a de ce fait aucune influence sur la pression
osmotique d’une cellule. Il s’agit d’un glucide, qui permet le stockage de
l’énergie.
Illustration n° 6 : l’amidon, l’amylose.
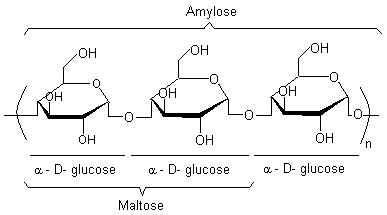
L’amidon se
compose d'enchaînements 1-4 de molécules de α–D–glucose. Il est stocké
(en réserve) dans les graines, les tubercules, les bulbes et les rhizomes.
Selon la variété de plantes concernée, les grains d’amidon ont une taille et
une forme variables, et leur agencement peut lui aussi différer d’une plante à
l’autre. On distingue deux sortes d’amidon :
a) l’amylose : l'amidon en contient de
10–30%. La macromolécule a une masse molaire de 100 000 à 300 000 Daltons. Les molécules de α–D–glucose sont linéaires, et liées du C1 de l'une au C4
d'une autre. La chaîne présente une structure hélicoïdale. L’inclusion de
molécules de diiode (plus exactement de polyiodures comme par exemple I3-, I5-) dans cette hélice
est connue sous le nom de réaction amido–iodée et se traduit par une forte
absorption de la lumière qui provoque l'apparition d'une couleur bleue intense.
b) La seconde sorte d’amidon est l’amylopectine ou iso-amylose ; l'amidon en contient de 70% à 90%. Les
chaînes de glucose sont fortement ramifiées ; On distingue des enchaînements
1-4 comme dans l'amylose avec fréquemment des enchaînements 1-6 qui constituent
les ramifications.
Illustration
n° 7
: l'amylopectine

Le
glycogène,synthétisé par l’organisme humain présente de grandes similitudes
avec l’amylopectine, mais il est encore plus ramifié.
Une plante, tout
comme un organisme animal, est en mesure de dissocier, au moyen d’enzymes, des
particules d’amidon solubles (et de ce fait aisément transportables). Le
meilleur exemple est sans doute celui de la formation du sucre de malt
(maltose) par germination de grains d’orge au cours de la fabrication de la
bière. L’amidon est le glucide le plus important pour l’alimentation.
La cellulose :
La cellulose
est une macromolécule linéaire et non–ramifiée, formée d'environ 500 à 5000
unités monomères de glucose reliées les unes aux autres par des liaisons β–glycosidiques.
Illustration n° 8 : la cellulose
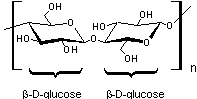
La cellulose est la substance de soutien (parois) des cellules des plantes (par exemple dans le cas du bois). Le glucose présent dans la cellulose ne peut cependant être utilisé en tant que tel, ni par les plantes ni par les animaux. Dans l’alimentation humaine, la cellulose est présente sous forme de fibres. Seuls les ruminants peuvent profiter de la cellulose, car durant leur digestion des microorganismes parviennent à diviser les macromolécules, qui deviennent alors assimilables par l’organisme. D’un point de vue chimique on peut, dans des conditions très particulières, parvenir à transformer du bois en sucres fermentescibles, comme le fait par exemple la Suède, afin de produire du bioéthanol utilisé ensuite comme carburant.
La « route du sucre » :
Il est assez
frappant de noter que l’appellation « sucre » présente des similitudes dans
bien des langues européennes : sugar en anglais, zucchero en italien, azucar en
espagnol, açùcar en portugais, cukier en polonais. Cela s’explique sans doute
en partie par l’influence du terme arabe sukkar au Moyen–Age, c’est–à–dire à
une époque où le monde arabe jouissait d’un grand rayonnement en matière
d’échanges commerciaux.
La canne à
sucre, originaire d’Asie de l’Est, est arrivée en Inde vers l’an 6000 avant
Jésus–Christ. On en tirait directement du sucre, en remplissant des tonneaux
d’argile ou de bois de forme conique de sirop de sucre épaissi ; grâce à une
ouverture pratiquée au sommet du cône, on pouvait filtrer le sirop, qui avait
entre temps perdu de sa teneur en sucre. Restait alors un cône de sucre solide,
le « pain de sucre », que l’on obtient aujourd’hui et depuis 1841 (tout comme
d’ailleurs le sucre en morceaux) en comprimant du sucre cristallisé humide.
Un amiral
qui accompagnait Alexandre le Grand lors de son expédition militaire en Inde a
parlé en 327 avant J. C. d’un roseau indien
qui produirait du miel sans abeilles. C’est probablement à ce récit que l’on
doit l’emprunt par le grec (saccharon) puis le latin (saccharum) du terme
sakara, issu du vieil indien. En sanscrit, sakara signifie aussi « grain de
sable », ce qui renvoyait à la forme cristalline du sucre.
Pline l’Ancien
(79-23 avant J.C.) écrit dans son historia
naturalis (livre II) : « L’Arabie produit certes du sucre, mais celui
venu d’Inde est plus célèbre encore. Il est blanc et craque sous la dent. Ses morceaux
peuvent atteindre la taille d’une noisette. On l’utilise à des fins médicales.»
Les Arabes ont appris des Perses comment produire le sucre et leur ont aussi emprunté leur vocabulaire, qui fut à l’origine des termes quandi et sukkar. Au VIIIè siècle, ils implantèrent en Mésopotamie des cultures de canne à sucre, à l’entretien desquelles ils employaient des esclaves. La canne à sucre fut tout d’abord implantée sur les rives du Nil et du Jourdain, puis sa culture s’étendit à la Méditerranée et à ses côtes et à ses îles, notamment aux Baléares.
Entre 1095 et 1291, les croisés découvrirent la canne à sucre et répandirent en Europe la nouvelle de la découverte d’un « sel indien ». Peu de temps après, le sucre, considéré comme une nouvelle épice, fut disponible dans les pharmacies à un prix qui était parfois supérieur à celui du poivre. Au XIIIè et au XIVè siècle, le sucre et la « douceur » qui le caractérise sont fréquemment utilisés comme métaphores dans la poésie amoureuse des troubadours tels que Oswald von Wolkenstein, Wolfram von Eschenbach ou Walther von der Vogelweide.
Outre Gênes,
c’est principalement Venise qui avait le monopole du commerce avec l’Orient et
contrôlait les importations de sucre vers l’Europe. Les états régissant le
commerce maritime établirent aussi des plantations de canne à sucre sur les
rives de la Mer Noire. Cette voie fut cependant fermée après la chute de
Constantinople en 1453.
Christophe
Colomb emporta avec lui en 1493 (lors de son deuxième voyage aux Amériques) des
plants de canne à sucre. La culture sur le sol américain connut un rapide
essor, dû notamment à une demande européenne croissante, et eu pour conséquence
la traite de nombreux Africains, massivement acheminés par bateaux.
L’importation
de sucre en provenance du « Nouveau Monde » cessa avec l’instauration, en 1806,
de la « barrière continentale ».
Le chimiste
et pharmacien Andreas
Sigismund Marggraf (1709–1782) examina la teneur en sucres de plantes
locales. Il découvrit en 1747 que la betterave fourragère produisait un sucre
identique à celui de la canne à sucre.
Son élève, le
physicien et chimiste Franz
Karl Achard (1753-1821) mena dans son domaine près de Berlin des
expériences en vue de sélectionner des betteraves particulièrement riches en
sucre et parvint ainsi à convaincre le roi Friedrich Wilhelm III de Prusse de
l’intérêt de produire du sucre à partir de ressources nationales. Avec le
soutien du roi, la première usine de fabrication du sucre put ouvrir ses portes
en Silésie dès 1802.
L’usage
du sucre
:
Dès
l’Antiquité, les médecins avaient observé que l’apport de glucose pouvait
améliorer les performances des sportifs lors des Jeux Olympiques. Le glucose
fut donc en quelque sorte le premier moyen de dopage connu. Il est aujourd’hui
prouvé que le glucose pénètre particulièrement rapidement dans le sang.
Le sucre
prodigue à l’organisme humain et animal de l’énergie grâce au cycle de
l'acide citrique ou cycle de Krebs (il a auparavant été fractionné
par voie enzymatique). L' insuline régule le taux de glucose dans le sang. Le
glucose devient du glycogène, un amidon de structure semblable à celle de
l’amylopectine.
Le glycogène
est stocké dans le foie et les muscles. L’absorption de grandes quantités de
glucose peut aussi favoriser la formation de graisses.
C'est pour des
raisons esthétiques (minceur) mais aussi médicales que la quantité de sucre se
trouve souvent réduite lors de régimes.
Quoi qu’il en
soit, l’apport d’énergie procuré par le sucre ne suffit pas au maintien des
fonctions vitales. Les vitamines et les oligo–éléments sont dans ce domaine
essentiels.
Le sucre a
également mauvaise presse du fait de son effet cariogène.
D’un point de
vue quantitatif, l’utilisation du sucre ne joue pas un grand rôle dans la
fabrication du sucre couleur ou caramel (additif alimentaire E
150).
Les propriétés
de conservation du sucre proviennent de sa capacité à fixer l’eau et à la
préserver par osmose, de microorganismes néfastes. Dans le cas des fruits
confits, le jus est remplacé par du sirop de sucre. Les confitures contenant
une quantité élevée de sucre se conservent mieux indépendamment de tout
traitement.
La
transformation, par fermentation, de solutions contenant du sucre (comme par
exemple la mélasse) en éthanol joue aujourd’hui un rôle croissant. On utilise
cet éthanol depuis des années déjà au Brésil comme carburant pour automobiles.
La transformation du bois en sucres fermentescibles fournit aussi en Suède de
l’éthanol que l’on mélange à l’essence.
Le
sucre comme denrée :
La consommation
du sucre obéit moins à un impératif alimentaire qu’à un plaisir gustatif. Le
plaisir procuré par le goût sucré d’un aliment et la gourmandise que celui–ci
suscite n’ont guère varié à travers les âges.
Le pouvoir
sucrant des différentes sortes de sucre est différent. A titre de comparaison,
on attribue au saccharose un pouvoir sucrant relatif de 1.
Tableau
1 : le
pouvoir sucrant relatif de différents types de sucres
|
Sucre |
Douceur relative |
|
Saccharose |
1 |
|
Fructose |
1,1– 1,7 |
|
Glucose |
0,5 – 0,8 |
|
Sucre
inverti |
0,95 |
|
Sorbitol |
0,4 – 0,5 |
|
Maltose* |
0,4 |
|
Lactose** |
0,3 |
* "Sucre
de malt"
** "Sucre
de lait"
Les substituts du sucre :
Il est
difficile de renoncer à la douceur du sucre. Mais les raisons de restreindre sa
consommation sont cependant nombreuses. Un moyen d’y parvenir réside dans la
substitution au sucre d’autres substances présentant une douceur comparable.
Les substituts
du sucre sont des alcools de sucre, reconnaissables à leur terminaison en
–itol. Le plus connu est le sorbitol (synonyme : glucitol), que l’on trouve
notamment dans les fruits du sorbier (sorbus aucuparia).
Illustration n° 9: le sorbitol
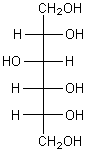
En raison des
besoins importants, le sorbitol est produit par hydrogénation catalytique du
glucose. Dans l’organisme, il est tout d’abord transformé en fructose, mais ne
nécessite pas d’apport d’insuline. Il ne présente en outre qu’une faible valeur
calorique. Les alcools de sucre sont réputés pour leur infime potentiel
cariogène.
Il existe
encore des substituts non caloriques et non cariogènes, qui ne présentent
certes aucune ressemblance chimique avec le sucre, mais possèdent pour certains
un pouvoir sucrant important.
Tableau 2 : Pouvoir sucrant relatifs de certains substituts.
|
Substituts |
Douceur relative |
|
Acesulfam
(E950) |
130 -200 |
|
Aspartame
(E951) |
200 |
|
Cyclamate
(E952) |
30 -50 |
|
Saccharine
(E954) |
300 - 500 |
Traduction en français : Anne-Sophie GOMEZ
VERS
LE DOCUMENT "MIEL DE ROSEAU"