PEINTURES D'ART
Gérard
GOMEZ
Plan
de l'étude :
1) Généralités
2-1) Aquarelle
2-2) Gouache
2-3) Peinture
a tempera
2-4) Peinture
acrylique
2-5) Huiles
2-6) Pastels
2-7) Lavis
et Glacis
3) La chimie dans les peintures d'art
3-1) Les
pigments
3-2-1) Peintures à l'eau
3-2-2) Peintures à l'huile
3-2-3) Peintures a tempera
3-2-4) Un liant breveté
3-3) Les
additifs
3-3-1) Les charges
3-3-2) Les diluants
3-3-3) Siccatifs ou retardateurs de séchage
3-3-4) Des biocides
3-4-1)
Mediums
3-4-2) Les vernis
3-4-3) Les Gesso
Annexe 1
Résine mastic, résine dammar, résine sandaraque, résine térébenthine
Annexe 2 Composition d'un jaune d'œuf
Annexe 3 Emulsion – émulsifiant
Annexe 4 Le fiel de bœuf comme émulsifiant
Annexe 5 Cire d'abeille – cire de carnauba - cires minérales.
Annexe 6 Colle de peau
|
-Le Larzac- Rémy Foulquier –
Huile sur toile -1987- |
-
Définition :
Une peinture utilisée par des artistes est une solution, une suspension ou une
pâte, colorée, qui sert à réaliser des tableaux lorsqu'on la dépose sur un
support. Cette définition, très large, correspond à une multitude
de préparations. Les peintures ont beaucoup évolué au cours des temps au gré
des progrès techniques, des évolutions esthétiques et des exigences des
peintres. -
Composition :
D’une façon générale on trouve dans une peinture : ·
Un
colorant : c’est une substance souvent solide, en solution ou en suspension
(on parle alors de pigment), qui lui donne sa couleur. ·
Un
solvant qui va dissoudre le colorant lorsqu’il ne s’agit pas d’un pigment. ·
Un
liant, dont les fonctions sont de maintenir le pigment en suspension, ainsi que de permettre la fixation de la
couleur sur le support. ·
Des
additifs qui ont des rôles très variés : ils peuvent donner à la peinture sa
brillance, lui permettre d'être plus épaisse ou plus fluide, augmenter son
pouvoir couvrant ou l’aider à sécher plus ou moins vite, etc…. |
Elles se distinguent par la nature du
liant (eau ou huile) des peintures utilisées et des divers ingrédients ajoutés
:
|
- Eau +
Gomme arabique → Aquarelle
ou gouache +
Colle ou œuf →
Tempera à la colle ou à l'œuf
+
Résine acrylique →
Peinture acrylique |
|
Peintures à l'eau |
|
- Huile + Diluant - Huile
+ cire + charge → Pastels gras |
|
Peintures à l'huile |
|
|
Le colorant est un solide en poudre
fine ; il peut se dissoudre dans l'eau qui sert alors de solvant ; il peut ne
pas être soluble et la gomme arabique jouera alors le rôle de liant pour ce
pigment, elle le dispersera dans l'eau et maintiendra cette dispersion dans
le temps. Les caractéristiques de cette
peinture sont les suivantes : -
Son pouvoir couvrant n'est pas très important ce qui a l'avantage de
permettre au peintre de traduire des transparences et des ambiances, mais qui
ne permet pas l'erreur car les retouches sont quasi impossibles. -
Les mélanges faciles de peintures permettent de traduire de subtiles nuances. -
Le support le mieux adapté est une feuille épaisse de papier (au moins 300g/m2). -
L'aquarelle est fragile (sensibilité à l'humidité) ; le tableau doit
obligatoirement être encadré sous verre. |
- Berlin
- Aquarelle 2003 -
Le colorant est un solide en poudre ; la gomme arabique sert
de liant ; on ajoute aussi du talc comme charge pour augmenter son épaisseur et
du blanc de zinc pour augmenter légèrement son pouvoir couvrant.
Ses principaux avantages pour un peintre sont :
- Sa
texture qui permet de dessiner facilement des détails fins.
- Elle est
plus facile à travailler que l'aquarelle car elle a un grand pouvoir couvrant
ce qui permet les retouches.
- Elle
permet un beau rendu des couleurs
- Elle
permet d'utiliser un grand nombre de supports.
- Bonne
tenue dans le temps et bonne résistance aux UV
Quelques défauts cependant :
- Elle est
vulnérable à l'eau et le tableau doit donc être encadré sous verre.
- En
couches épaisses elle peut surtout sur support souple, se craqueler.
2-3) Peinture a tempera
Technique très ancienne puisqu'on retrouve des tableaux
ainsi réalisés dans les civilisations Egyptiennes et Romaines antiques ; de
nombreuses icônes byzantines ont ainsi été peintes. Certaines œuvres ainsi
conçues ont traversé le temps sans être très dégradées, preuve que cette
technique conduit à des réalisations pas trop fragiles.
Elle est assez peu utilisée de nos jours ; elle sert à faire
des ébauches que l'on peint à l'huile ensuite.
C'est une peinture à l'eau ayant le jaune d'œuf pour liant.
Une fois sèche, elle ne se dissout ni dans l'eau, ni dans d'autres solvants
comme l'essence de térébenthine ou l'alcool.
Ses caractéristiques sont les suivantes :
- Elle
sèche très vite ce qui rend difficile la réalisation de dégradés ou de fondus.
- Une fois
sèche, elle est très sensible à l'humidité et aux moisissures. Il faut la
fabriquer au moment de son utilisation.
- Il lui
faut un support absorbant ; on peut utiliser le plâtre ou le bois mais dans ce
dernier cas, il faut au préalable l'enduire de plusieurs couches de plâtre ou
de craie. Quelques tempera à l'œuf ont été réalisées sur toiles
préalablement enduites.
On peut fabriquer la tempera de la façon suivante :
- On isole un jaune d'œuf débarrassé de sa membrane
vitelline et on ajoute un peu d'eau.
- On prépare une pâte en mélangeant de l'eau au pigment broyé en poudre très fine.
- On mélange cette pâte au jaune d'œuf au fur et à mesure
que l'on peint pour éviter que le mélange préparé trop à l'avance ne sèche
avant son utilisation.
La peinture aura un aspect brillant, satiné ou mat suivant
les quantités respectives d'eau et d'œuf utilisés.
Les peintures acryliques apparaissent dans les années 1960
aux Etats-Unis inventées par le chimiste Henry Levison.
Les pigments minéraux ou organiques utilisables sont
similaires à ceux de la peinture à l'huile, mais ils ne doivent pas être broyés
trop finement.
Le liant est l'eau dans laquelle des résines acryliques sont
dispersées.
Il y a souvent beaucoup d'additifs (tensio-actifs, agents
mouillants, épaississants, biocides …..).
Caractéristiques des peintures acryliques
- Elles
n'ont pratiquement pas d'odeur.
- Elles
sèchent rapidement (comme c'est parfois un inconvénient on ajoute un additif
pour ralentir le séchage).
- Elles
sont moins toxiques que les peintures à l'huile.
- Le
nettoyage des pinceaux s'effectue à l'eau.
-
Comme c'est une peinture épaisse et
lourde elle ne peut pas s'utiliser sur tous les supports ; les plus adaptés
sont les toiles tendues sur châssis, les panneaux de bois recouverts de toile,
mais on peut aussi peindre sur papier pour aquarelle ou sur bois traité. Le
support ne doit être ni poreux ni gras.
2-5) Peinture à l'huile
Cette technique est apparue à la fin du Moyen Âge et a
supplanté progressivement la technique a tempera.
Les pigments sont mélangés à de l'huile comme liant (huile
de lin ou d'oeillette) et on obtient une pâte qu'on peut diluer avec une
essence (par exemple l'essence de térébenthine).
Pour améliorer la consistance de la peinture on utilise un
médium à peindre qui est souvent un mélange d'huile, d'essence de térébenthine
et de résine.
Son principal avantage est qu'elle permet la superposition
de fines couches transparentes de couleurs ce qui autorise des effets d'ombre
et de lumière très subtils.
Son principal inconvénient est le temps de séchage qui peut
être plus ou moins long suivant la siccativité des huiles utilisées comme liant
; une règle à respecter (que l'on expliquera plus loin) lorsqu'on veut
superposer des couches de peinture à l'huile : la couche nouvelle doit être
plus grasse que celle sur laquelle on la pose ; c'est ce qu'on appelle la règle
du "gras sur maigre".
Les supports : - toile de lin sur châssis – cartons entoilés
– papiers lourds de qualité aquarelle.
Remarque : la peinture
éludorique (du grec élaion huile et hùdôr eau)
C'est un genre de peinture qui s'exécute en faisant passer
le pinceau à travers une eau très claire pour atteindre le fond sur lequel on couche
les couleurs à l'huile. Le procédé de la peinture éludorique inventé par
Montpetit [Arnaud Vincent de Montpetit – 1713-1800, l'invention date de 1759 ] donne
à la peinture à l'huile toute la délicatesse de la miniature.
Technique commune au dessin et à la peinture.
|
|
Solide en bâtonnet formé : - d'un
pigment organique ou minéral - d'une charge
qui lui donne sa texture, sa consistance ; il s'agit le plus souvent de
carbonate de calcium, de craie ou de plâtre -
d'un liant qui peut être de la gomme arabique, ce sont alors des pastels secs
utilisés dès le XVème siècle et dont l'apogée se situe au XVIIIème, ou une
huile ou une cire (cire d'abeille, cire de carnauba ou cire minérale) (voir annexe 5) et dans ce cas ce sont des pastels gras
inventés au XXème siècle. |
Cette technique a été utilisée par des peintres célèbres
dont Léonard de Vinci (XVème –début du XVIème), Quentin de La Tour (XVIIIème)
le pastelliste par excellence, Toulouse-Lautrec et Degas (XIXème siècle), ne
sont pas les moindres.
Les supports les mieux adaptés sont :
- Pastels
secs : papiers à grain qui retiennent la poudre de pastel. On peut utiliser
le bois, le verre ou le métal mais en déposant au préalable un apprêt.
- Pastels
gras : s'accommodent mieux des surfaces lisses ; on peut utiliser le
papier, le carton, le bois, le verre ou le métal, préalablement préparés.
- Lavis
:
C'est une technique qui n'utilise qu'une couleur ; pour
pouvoir traduire différentes intensités, l'aquarelle ou l'encre de chine sont
plus ou moins diluées. On parle de lavis à la sépia quand la couleur est
extraite des poches de seiche ; mais on peut obtenir de l'encre dite sépia à
partir des tannins extraits des noix de galle du chêne.
- Glacis
:
On dépose sur le tableau en fin d'élaboration, une ou plusieurs
couches transparentes de peinture faite avec plus de liant que de pigment ; ce
voile contribue à renforcer l'effet de profondeur. On peut procéder ainsi avec
la peinture à l'huile, mais aussi la peinture acrylique, l'aquarelle ou la
technique a tempera.
3) La chimie dans les peintures d'art :
|
|
Un aperçu sommaire des différentes
techniques picturales ayant été donné, on va à présent apporter des
précisions sur quelques composants qui
interviennent. Il ne s'agit pas, bien sûr, d'une étude exhaustive mais d'un
examen de l'essentiel permettant d'avoir des idées simples mais claires sur
ces questions. |
Ils sont les éléments essentiels d'une peinture car sans eux
il n'y a pas de tableau et parce qu'ils conditionnent directement le ressenti
de l'observateur devant une œuvre.
Nous traiterons des pigments qui ont été utilisés et dont
certains sont interdits aujourd'hui pour des raisons de sécurité par exemple,
ainsi que des pigments toujours utilisés et des pigments récents.
On peut les séparer en pigments inorganiques et pigments
organiques.
La nomenclature des pigments :
On les repère avec un P comme première lettre sauf pour
certains pigments d'origine naturelle qu'on désigne par N ; une deuxième lettre
indique la couleur en anglais :
W White ; Y Yellow ;
O Orange ; R Red ; B Blue ; G Green ; V Violet
; Br Brown ; Bk Black.
On ajoute un nombre définissant la nature du pigment.
Ainsi
PY74 veut dire Pigment Yellow à base d'arylamide.
NY24 veut dire Natural Yellow à base d'une gomme résine
produite par plusieurs espèces d'arbres de type Garcinia.
Teinte, clarté, saturation d'une couleur :
Les particules de pigments d'un tableau absorbent une partie
de la lumière reçue, c'est cette partie absorbée qui est responsable de la
teinte (du ton) c'est-à-dire de la couleur perçue.
La portion de lumière réfléchie et diffusée par les pigments
et la couche de fond contribue à la clarté (les peintres disent la valeur)
c'est-à-dire l'intensité lumineuse perçue et à la saturation, c'est-à-dire la
pureté de la couleur.
Pouvoir couvrant d'une couleur :
La transparence d'un pigment est liée à la structure des
particules qui le composent.
Le vert émeraude, le bleu de Prusse ou le violet de
cobalt sont transparents c'est-à-dire qu'ils se laissent traverser par la lumière
; au contraire les oxydes de fer de synthèse sont plus denses, se laissent
moins traverser, ils réfléchissent les rayons reçus.
C'est l'écart entre les indices de réfraction du liant et du
pigment qui conditionne la réflexion de la lumière ; plus il est grand, plus le rendu est lumineux et plus la couleur
est couvrante.
Ainsi le blanc de titane a un indice de réfraction d'environ
2,6 ; si on l'associe à de l'huile comme liant (indice de réfraction voisin de
1,5) la différence d'indice étant grande, il a un très grand pouvoir couvrant.
Pouvoir colorant d'une couleur :
Le pouvoir colorant est lié à la granulométrie des pigments
utilisés.
Plus les pigments sont finement broyés plus ils sont
colorants et parfois tellement qu'ils
dominent tous les autres et sont inutilisables.
Blanc de plomb (ou Céruse) - Blanc de zinc – Blanc de lithopone
(ou Blanc de Comines) – Blanc de titane ––
Vert de gris – Vert de schweinfurt (ou Vert
émeraude ou Vert
de Paris ou Vert de Mitis) – Vert de Scheele – Malachite – Vert de chrome –
Jaune de chrome - Jaune de cadmium - Orpiment (ou Jaune royal) – Jaune de cobalt
(ou Auréoline) – Jaune
d'Antimoine (ou Jaune de Naples) –
Bleu de Prusse – Bleu de cobalt - Bleu outremer
– Bleu égyptien (ou bleu
d'Alexandrie) – Smalt – Bleu
céleste (ou Bleu de céruléum) – Bleu d'azurite (ou Azurite)
– Bleu d'Orégon -
Cinabre (ou vermillon véritable) – Hématite
– Ocres – Rouge de Venise – Rouges de cadmium – Minium –
Violet de cobalt – Violet de manganèse -
Terre de Sienne – Terre
de Sienne brûlée –
Noir de fumée – Noir d'ivoire - Noir de graphite et de schiste – Noir de Mars - Noir de manganèse
–
v
Blancs
Blanc de plomb (appelé aussi Céruse) PW 1
C'est un carbonate basique de Plomb 2PbCO3,
Pb(OH)2.
Très tôt (dès le Moyen Âge) on s'est aperçu de la toxicité
du plomb, mais ce fut seulement au XVIIIème siècle qu'on le remplaça par du
blanc de zinc ; il faut attendre le XXème siècle pour qu'il soit interdit.
Le blanc de plomb avait un pouvoir couvrant exceptionnel et
il n'était pas affecté par la lumière.
Un défaut important cependant pour les aquarelles (non
protégées par un vernis protecteur) : en présence de composés soufrés ou de
traces de sulfure d'hydrogène (H2S) dans l'atmosphère le blanc
noircissait car il se formait du sulfure de plomb noir : Pb2+ + S2-
→ PbS.
Remarque :
La plumbonacrite (Pb5O(CO3)3(OH)2),
un hydroxycarbonate de plomb, transparent, voisin de la céruse mais a structure
cristallographique différente, a été utilisée par quelques peintres pour donner
à certaines parties d'un tableau un effet de relief (peinture en couches
épaisses) ; c'est le cas notamment de Bethsheba (1654) et Susanna
(1647) deux œuvres de Rembrandt.
Blanc de zinc PW
4
C'est de l'oxyde de zinc, ZnO.
Beaucoup plus cher que le blanc de plomb il a tardé à
remplacer celui-ci (milieu du XIXème siècle) malgré les dangers encourus.
Il couvre beaucoup moins que le blanc de plomb et de ce fait
il a longtemps été utilisé pour éclaircir les autres couleurs.
Blanc
de lithopone (ou blanc de Comines) PW 5
Composé de sulfure de zinc (ZnS) et de sulfate de baryum
(BaSO4), il est utilisé comme pigment blanc depuis la haute
antiquité.
Ce pigment semi-couvrant (moins couvrant que le blanc de
titane) est stable à la lumière.
On le prépare en faisant réagir le sulfure de baryum avec le
sulfate de zinc :
BaS + ZnSO4 → BaSO4 + ZnS
Blanc de titane PW 6
C'est un oxyde de titane, TiO2.
Il a un bon pouvoir couvrant ; il n'est pas affecté par les
composés chimiques comme par exemple le sulfure d'hydrogène qui faisait noircir
le blanc de plomb, nous l'avons vu, ou les solvants.
Les liants utilisables pour la plupart des techniques,
aqueux, acryliques ou gras lui conviennent.
Cependant il jaunit lorsqu'exposé aux UV.
Il est très utilisé de nos jours malgré son prix relativement
élevé.
v
Verts
-
Obtenus à partir du cuivre (II)
Vert de gris PG
20
Si l'on trempe du cuivre dans du
vinaigre, il se forme peu à peu une couche verte d'acétate de cuivre basique
Cu(CH3CO2)2, que l'on appelle vert de gris ou
verdet, particulièrement sur la face supérieure en contact avec l'air. On a
gratté cette couche et on l'a utilisée comme pigment en peinture depuis
l'antiquité.
La patine sur les surfaces de cuivre
(toitures, statues, …) correspond, elle, a du carbonate de cuivre basique :
CuCO3, Cu(OH)2.
La couleur va du vert bleu au vert émeraude profond.
Vert de Schweinfurt ou vert émeraude ou vert de
Paris ou vert de Mitis PG 21
En 1800, Ignaz von Mitis a découvert à Vienne, un pigment
d'un vert intense composé d'un mélange d'acétate et d'arsénite de cuivre, qu'on
a dans un premier temps appelé vert de Mitis. C'est après la première
fabrication industrielle de cette substance à Schweinfurt qu'on lui a donné le
nom de vert de Schweinfurt.
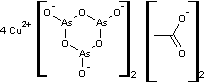
Sous l'influence de microorganismes, se développent, à
partir de ce pigment "grand teint" et de son liant, des composés
organiques contenant de l'arsenic qui, inhalées peuvent conduire à des
empoisonnements. C'est pourquoi ce pigment a été qualifié de "vert
poison". En raison de sa toxicité, le vert de Schweinfurt a été interdit
dès 1882 mais a été utilisé encore quelques années comme insecticide.
Vert de Scheele PG 22
Plusieurs formules suivant les conditions de sa préparation,
mais il est communément admis qu'il s'agit d'hydrogénoarsénite de cuivre CuHAsO3 :
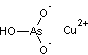
C'est un pigment dont
l'utilisation est interdite compte-tenu de sa toxicité.
Par ailleurs c'est un préservateur du bois.
Vert Malachite naturel : PG 39
Cristaux naturels correspondants à des carbonates de cuivre
CuCO3.Cu(OH)2
La malachite a surtout été utilisée comme pierre ornementale
; elle possède un beau poli.
Elle a été utilisée comme pigment depuis l'antiquité (on
réduisait les cristaux en poudre) ; ce pigment est sensible à la lumière et aux
acides.
Il est plus rarement utilisé de nos jours.
-
Obtenu à partir du chrome
Vert oxyde de chrome : PG 17
C'est l'oxyde de chrome (III), Cr2O3.
De couleur vert olive, il est assez terne et a un pouvoir
couvrant faible.
Il résiste à de hautes températures (1000°C) et peut être
utilisé pour colorer les céramiques. Il résiste aussi à la lumière et aux agents
chimiques extérieurs.
Il a été préparé par Louis Jacques Thenard (ne pas écrire Thénard) le
plus éminent collaborateur de Gay-Lussac, qui a été l'élève de Vauquelin et de
Berthollet.
v
Jaunes
Jaune de chrome
PY 34
C'est du chromate de plomb PbCrO4
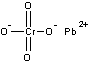
Vauquelin et Berthollet découvrent le chrome dans la
crocoïte.
Les cristaux sont rouges mais le trait sur une plaque de
porcelaine blanche non émaillée est jaune orangé.

Au cours d'essais destinés à obtenir ce colorant en
laboratoire, ils remarquent la belle couleur jaune du chromate de plomb et
l'essayent comme pigment pour les peintures d'art.
En effet, on peut préparer le chromate de plomb par réaction
de l'acétate de plomb Pb(CH3CO2H)2 sur le
chromate de potassium (K2CrO4) ; plus la proportion de
sel de plomb est importante et plus la couleur passe du jaune à l'orangé puis
au rougeâtre foncé.
L'action de la lumière (UV) modifie sa couleur qui vire au
vert ; il se produit une réduction le chrome passant de Cr (VI) à Cr (III).
Il est toxique et présente des risques pour l'environnement.
A ne pas utiliser avec des pigments contenant du soufre.
Jaune de cadmium PY 35
C'est du sulfure de cadmium. La couleur jaune est éclatante.
A l'état naturel il existe dans la greenockite, un des seuls
minerais à contenir des quantités appréciables de composés du cadmium.
On peut aussi le préparer :
![]()
C'est un pigment très stable et au bon pouvoir couvrant,
employé en Europe depuis le XIXème siècle.
Comme tous les pigments de cadmium ils sont autorisés mais
doivent être utilisés avec précautions (risques pour la santé et
l'environnement).
Orpiment ou jaune
royal PY 39
|
|
C'est du trisulfure d'arsenic As2S3. De couleur citron brillant à jaune d'or, il a été utilisé
depuis l'antiquité ; on en a détecté dans les papyrus Egyptiens. Au Moyen Âge on en a retrouvé dans les enluminures ; mais
il a rapidement été délaissé à cause de sa toxicité. Il se forme dans les veines hydrothermales de basse
température (130-140°C) ; il est parfois formé par sublimation dans les
fumerolles. Il peut aussi résulter de l'altération du réalgar As4S4. On trouve des gisements importants en Turquie et au Pérou. |
Jaune de cobalt
ou Auréoline PY 40
C'est l'hexanitritocobaltate(III) de potassium CoK3N6O12
ou K3[Co(NO2)6]
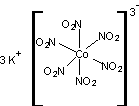
L'équation globale de sa préparation au cours de laquelle il
précipite est la suivante :
![]()
Sa couleur est un beau jaune vif, mais moins éclatant que le
jaune de cadmium ; de plus il est assez peu couvrant et comme tous les sels de
cobalt il est cher. On lui préfère souvent des pigments organiques. Il n'a été
utilisé comme pigment en peinture qu'à partir de 1850 bien qu'ayant été produit
quelques années auparavant.
Jaune d'antimoine
ou Jaune de Naples PY 41
C'est un antimoniate de plomb de formule Pb3(SbO4)
; connu et préparé depuis longtemps (1500 ans av. J.C.) ; c'est pratiquement le
seul pigment jaune utilisé à cette époque.
C'est un pigment très couvrant ; Il ne doit pas être utilisé
avec des pigments contenant du soufre sous peine de voir le jaune noircir
(PbS).
Il est toxique comme tous les pigments au plomb.
v
Bleus
Bleu de Prusse PB 27
Il a été préparé pour la première fois à Berlin (on
l'appelle aussi pour cela le bleu berlinois) par l'artiste peintre
Heinrich Diesbach, en 1710.
C'est un hexacyanoferrate (II) de fer (III)
Fe4III[FeII(CN)6]3.15H2O

Ce complexe adopte un système cristallin cubique à faces
centrées, à structure lacunaire. Il peut s'y introduire des ions alcalins, par
exemple K+ et donner
KFeIII[FeII(CN)6].3H2O.
K+ peut facilement entrer ou sortir des sites
tétraèdriques de cet ensemble.(UdPPC – Fer
curiosités – AIC 2011 –dossier 4d)
C'est un pigment assez peu couvrant.
Remarque :
On peut parfois lui adjoindre des charges, sulfate de baryum
par exemple et l'on obtient le bleu charron
Fe4III[FeII(CN)6]3.15H2O
. BaSO4 .
qui servait autrefois à peindre les charrettes, les portails
; c'est alors un pigment couvrant qui convient pour les fonds.
Bleu de cobalt PB
28
C'est un aluminate de cobalt CoAl2O4
synthétique, de type spinelle (A2+B23+O4
avec A2+ en coordination tétraèdrique et B3+ en
coordination octaèdrique), fabriqué par le chimiste français Louis Jaques
Thenard en 1802.
Plusieurs bleus de cobalt obtenus en mêlant sels d'aluminium
et sels de cobalt et en calcinant le tout ont été utilisés pour décorer la
porcelaine (porcelaine de Saxe ou de Bohême). En 1802 Thenard recherchant un
substitut au bleu outremer naturel, très coûteux, met au point l'aluminate de
cobalt, pigment d'un bleu plus vif.
Il reste très cher ; il est stable et assez couvrant.
Bleu outremer PB 29
|
|
|
Lapis-lazuli |
A l'origine il correspond à une pierre ornementale le
lapis-lazuli, une roche métamorphique que l'on trouve principalement en
Afghanistan, broyée. Le lapis-lazuli est constitué de lazurite, une sodalite
c'est-à-dire un alumino-silicate de sodium avec soufre (Na,Ca)8
[(AlSiO4)6(SO4,S,Cl)1 à 2], de couleur bleu roi à
bleu foncé, associé à un peu de calcite et de pyrite.
C'est la présence d'ions S3- majoritaires
(radical anion trisulfure dans une cage aluminosilicate de type zéolithe) qui
donne la couleur bleue à la lazurite car ils absorbent la lumière rouge
(600-610 nm) ; les ions S2- minoritaires absorbent eux dans le bleu
et donnent une teinte rouge. Si la proportion de S2- est faible la
teinte du pigment est outremer, si elle augmente on va vers le violet ("Les
pigments des manuscrits du Moyen Âge" Claude Coupry CNRS).
Utilisé comme pigment mais très cher il est dès le milieu du
XIXème siècle remplacé par le "bleu Guimet" un aluminosilicate de
synthèse Na7(AlSiO4)6S3 fabriqué en
1826 par le chimiste français Jean-Baptiste Guimet à partir de kaolin (silicate
d'aluminium), de carbonate de calcium de soufre, de sulfate de sodium et de
charbon de bois.
Ce bleu beaucoup moins coûteux (environ 1000 à 2000 fois
moins) que le naturel est utilisé comme pigment où il se révèle très stable,
mais aussi pour l'azurage du linge (l'azurage étant une opération destinée à
faire apparaître le linge plus blanc).
Souvent, pour différencier le bleu synthétique du bleu
outremer naturel, on désigne ce dernier par bleu lapis.
Bleu égyptien (ou bleu d'Alexandrie) PB 31
En chauffant entre 870°C et 1100°C des composés calcaires avec
des composés siliceux et cuivreux pendant plusieurs heures, on obtient des
cristaux bleus de cuprorivaïte (CaO.CuO.4SiO2). La couleur varie du
bleu foncé au bleu clair suivant la température et le temps de chauffage.
Le smalt PB 32
Silicate de potassium et de cobalt préparé à partir de
différents sels de cobalt grillés avec du sable en présence d'air.
Ce pigment a servi de substitut au coûteux bleu outremer
jusqu'au XIXème siècle où il est remplacé par les bleus de cobalt.
Le smalt a surtout été utilisé pour la coloration des
vitraux, des céramiques et des porcelaines.
Bleu Céleste (ou bleu de Céruléum) PB 35
C'est du stannate de cobalt (CoO, nSnO2) un bleu
lumineux au bon pouvoir couvrant, découvert au début du XIXème siècle par
Andreas Höpfner (1805) qui l'obtint en grillant du cobalt et de l'oxyde d'étain
; commercialisé pour la peinture d'art vers 1860 ; il verdit à la lumière.
Un pigment organique, la phtalocyanine de cuivre (II), peut
être substitué au bleu céleste.
Bleu d'azurite (ou azurite)
A ne pas confondre avec la lazurite vue plus haut
(lapis-lazuli).
C'est un carbonate hydraté de cuivre(II) : Cu2(CO3)2,
Cu(OH)2
Ses couleurs vont du bleu au bleu vert. Ce pigment est connu
depuis l'antiquité. C'est le bleu qui a été le plus utilisé par les peintres
médiévaux.
A tendance à devenir gris s'il est utilisé a tempera.
Bleu
YInMn ou Bleu
Orégon
C'est un pigment qui dans sa structure cristalline intègre
de l'Yttrium (Y), de l'Indium (In) et du Manganèse (Mn) ; sa formule de base
est YIn1-xMnxO3 mais on peut jouer sur le
rapport In/Mn pour renforcer ou atténuer le bleu.
Il a été découvert par le Professeur Subramanian à
l'Université de l'état d'Orégon en 2009.
v
Rouges
Cinabre (ou vermillon véritable) PR 106
C'est
le sulfure de mercure (II) : HgS (forme α)
Il a été
utilisé dans la Chine ancienne et était bien connu des Romains.
Toxique (il
contient du mercure) il a été abandonné au profit de pigments azoïques ; il
fonce un peu à la lumière (longue exposition), mais ce n'est pas systématique.
Contenant
du soufre il ne doit pas être utilisé avec des pigments contenant du plomb ou
du cuivre.
Les
"rouges de fer"
De nombreux pigments rouges sont composés de trioxyde de fer
(III) Fe2O3.
Cet oxyde naturel existe sous quatre phases α ou β ou γ ou ϵ.
L'une, la phase α, correspond aux rouges des pigments
naturels utilisés :
- l'hématite PR 102
Minéral très commun
dont la poudre est utilisée depuis très longtemps comme pigment (au
Paléolithique supérieur, déjà, nos ancêtres dessinaient et peignaient avec, sur
les murs des grottes et des cavités).
Son nom dérive du
grec haima, le sang.
Rouge sombre,
l'hématite a un fort pouvoir colorant et couvrant ; elle a une excellente
stabilité à la lumière.
- Les ocres (du grec ôchra, terre jaune)
On distingue :
x
les ocres rouges naturels : PR 102
|
|
C'est de l'argile
pure colorée par l'hématite et agglomérée à des grains de sable (quartz). On en trouve en
Bourgogne ou dans le Vaucluse (Roussillon). La présence d'eau
et d'autres oxydes métalliques (Manganèse, Aluminium) ou de silicates conduit
à toute une gamme de couleurs allant du jaune au rouge. |
x
Les ocres préparés : PR 102
Ils résultent de la
calcination de différentes terres à 950°C.
L'oxyde de fer
déshydraté résultant de cette calcination donne la couleur rouge au pigment
obtenu avec des variantes selon la nature et la quantité des autres oxydes
métalliques présents.
- Le rouge de Venise PR 102
obtenu en calcinant
des oxydes de fer hydratés (Fe2O3, 3H2O).
Les rouges de
cadmium (PO 20 – PR 108)
Ce sont des pigments inorganiques de synthèse qui ont été
fabriqués dans les années 1900 en Allemagne.
Il s'agit d'un ensemble sulfure de cadmium et séléniure de cadmium
(CdS/CdSe) dont la couleur varie du jaune (CdS pur) au noir (CdSe pur) en
passant par le vermillon et le rouge foncé selon la proportion de séléniure de
cadmium.
Ces pigments sont cancérigènes notamment à cause de la
présence de CdSe.
Ils sont relativement coûteux.
Le minium PR 105
C'est un oxyde de plomb Pb3O4.
De couleur rouge orangé il a été utilisé autrefois comme
pigment en peinture d'art.
Sa toxicité a fait qu'il a été abandonné pour cet usage.
Il se dégradait dans le temps et devenait soit noir (PbS),
soit blanc (carbonate basique de Plomb) suivant l'environnement.
v
Violets
Violets de cobalt PV 14
C'est
un pigment inorganique de synthèse.
Il
s'agit de phosphate de cobalt Co3(PO4)2 plus
ou moins hydraté.
Les couleurs varient en fonction de l'hydratation ; anhydre
il est violet foncé, tétrahydraté, il est violet clair, octahydraté il est rose
à rouge clair.
Ils sont peu couvrants et relativement chers.
Remarque : On appelle
aussi violet de cobalt un arséniate de cobalt Co3(AsO4)2.
Violet de manganèse PV 16
Pigment inorganique de synthèse ; c'est un pyrophosphate
d'ammonium et de manganèse (III), NH4MnP2O7
(NH4+, Mn3+, P2O74-).
v
Bruns
Terre de Sienne PBr 7
C'est un pigment minéral naturel. Son nom vient de ce qu'à
l'origine c'était de la terre provenant de la ville italienne de Sienne en
Toscane.
Elle contient environ 50% en masse de trioxyde de fer(III),
Fe2O3, associé à de l'argile et des oxydes d'autres métaux
dont le manganèse.
A différencier des ocres par le fait que dans ceux-ci on a
de l'argile pure colorée par Fe2O3.
Terre de Sienne brûlée PBr 7
La terre de Sienne naturelle, calcinée, s'enrichit en oxydes
de fer et de manganèse et donne un
pigment plus rouge et moins transparent.
Les deux pigments s'accommodent très bien des techniques à
l'huile et a tempera.
v
Noirs
Noirs de carbone
Il s'agit de carbone (C) provenant de la combustion
incomplète de différentes substances organiques ; bonne stabilité à la lumière.
Noir de fumée PBk
6
appelé aussi noir de suie (cheminées).
Noir d'ivoire PBk 9
qui provient de la calcination d'os d'animaux ; autrefois on
calcinait de l'ivoire.
Il s'agit de carbone mélangé à du phosphate de calcium Ca3(PO4)2.
Il est un peu brillant, plus chaud et intense que le noir de fumée.
Ce pigment est utilisé depuis l'antiquité.
Noir de graphite et de schiste PBk 10
Carbone ne provenant pas d'une combustion incomplète.
C'est une poudre gris noir composée à 65% de carbone, le
reste provenant des schistes.
Noir de Mars PBk 11
A base d'oxyde de fer (II), FeO ; le pigment naturel
contient des traces de dioxyde de silicium (SiO2) et de trioxyde
d'aluminium (Al2O3).
Noir de manganèse PBk 14
Il s'agit de dioxyde de manganèse MnO2.
v
Des
mélanges
Tous les pigments précédemment cités
sont des colorants monopigmentaires. Souvent les peintres réalisaient des
mélanges avec ces pigments ; il est impossible de les mentionner tant ils peuvent être nombreux. Une mention
particulière cependant pour :
Obtenus en mélangeant du bleu de Prusse et du jaune de
chrome, mélange auquel on ajoutait en quantités variables du sulfate de baryum.
Vert de
phtalocyanine (ou Vert Monastral) - Vert Naphtol B –
Jaune PY 17 - Jaune PY 55 - Jaune Hansa –
Bleu de
phtalocyanine (ou Bleu monastral) - Bleu d'indanthrène (ou Bleu d'indanthrone) - Indigo -
Rouge de Turquie - Rouge cochenille - Rouge lithol (ou Rouge Tobias) - Rouge de quinacridone - Rouge thioindigo - Rouge de pérylène - Rouge de naphtol - Orangé de pyrrole –
Violet de
quinacridone - Violet de dioxazine (ou Violet permanent) -
Noir d'aniline - Noir de pérylène -
v
Verts
Vert de phtalocyanine ou vert Monastral PG 7
C'est une phtalocyanine de cuivre (II) polychlorée.
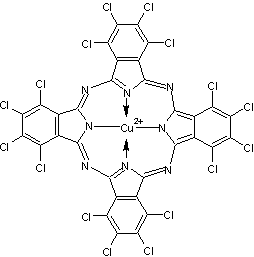
Couleur verte très prononcée, froide, proche de celle de
l'émeraude.
Vert Naphtol B PG 8
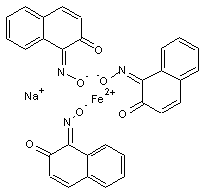
Vert foncé, un peu terne.
v
Jaunes
Pigment jaune PY 17
Pigment azo :
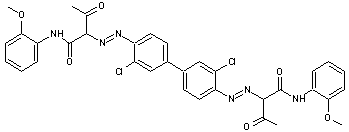
Pigment jaune PY 55
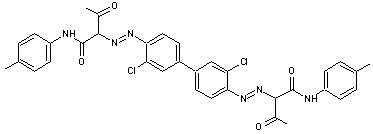
Jaune un peu terne, tirant sur l'orangé.
Jaune Hansa PY 74 ou Arylide Yellow
Pigment azo :
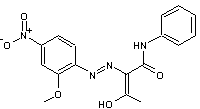
Couleur jaune tirant sur le vert ; pigment semi-transparent,
de permanence moyenne.
Remarque : Les jaunes
Hansa ont été mis au point au début du XXème siècle par les laboratoires Hoechst
(du groupe Hansa) et introduits en peinture en 1909.
v
Bleus
Bleu de phtalocyanine ou
bleu Monastral PB 15
C'est de la phtalocyanine de cuivre (II) :
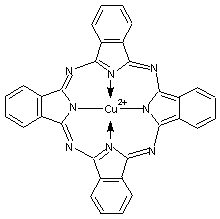
Pigment organique bleu tirant sur le vert (cyan) appartenant
à la famille des tétraazatétrabenzoporphyrines, commercialisé au début du XXème
siècle.
C'est un pigment qui se présente sous forme de poudre
légère,fine à haut pouvoir colorant, très stable à la lumière et à la chaleur.
Convient pour toutes les techniques (eau, huile, a tempera, acrylique).
Cette molécule est obtenue par condensation de 4 molécules
de phtalonitrile :
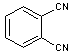
en présence de cuivre métal à 200°C.
On l'utilise aussi beaucoup pour les encres d’imprimerie.
Remarque :
Si on ajoute du sulfate de baryum comme charge, ce pigment
devient un substitut au bleu céleste ou bleu de céruléum
Bleu d'indanthrène ou bleu d'indanthrone PB 60
C'est le 6,15-Dihydro-5,9,14,18-anthrazinetétrone :
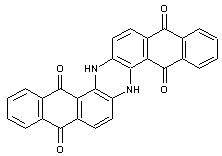
Colorant très résistant à la lumière et à la chaleur.
Il est utilisé comme pigment ou comme teinture du fait de
son fort pouvoir colorant.
C'est vers 1928 qu'on l'utilise dans la peinture d'art.
Il est transparent et assez cher, c'est pourquoi certains
lui préfèrent le bleu phtalo.
Remarque :
En cosmétique sa dénomination colour index (CI) est 69800.
Dans certains pays il est autorisé comme colorant
alimentaire (manascorubine E 130) pour l'azurage du sucre ou du sel (l'azurage
étant une opération destinée à faire apparaître ceux-ci plus blancs), mais est
interdit à cet effet en Europe.
Indigo PB 66
Matière colorante, qui dans sa forme
première est d'un bleu un peu violacé :
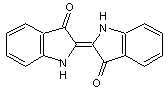
Elle est extraite de l'indigotier (Indigofera
suffruticosa ou indigofera anil plante vivace des régions chaudes
(Salvador...) autrefois cultivée comme plante tinctoriale, de la famille des
papilionacées), ou obtenue par synthèse. L'indican (dérivé de l'indole) est la
molécule première existant dans les feuilles. L'hydrolyse enzymatique suivie
d'une oxydation à l'air conduit à la molécule d'indigo, ainsi que le montre le
chemin de réactions ci-dessous. Cette matière colorante a été pendant des
siècles utilisée comme teinture ; On obtenait
100g d'indigo en traitant 50kg de feuilles. C'est Eliza Lucas Pinckney
(1723-1793) qui est à l'origine des premières plantations d'indigotiers aux
USA.
Cette molécule s'avéra très difficile à synthétiser ; A.Baeyer mit dix ans pour en
établir la constitution puis la synthétiser. C'est le procédé de Karl Heumann qui
fut adopté pour la synthèse industrielle à grande échelle. C'est à partir de
1897 que l'indigo artificiel remplaça l'indigo naturel.
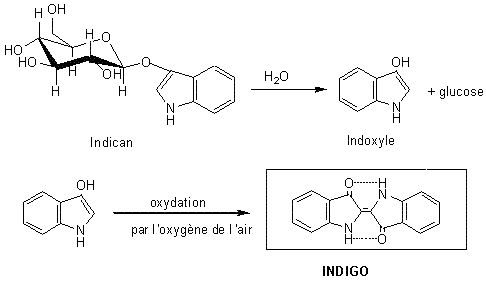
v
Rouges et Orangés
Rouge de Turquie NR 8
Colorant anthraquinonique
rouge connu depuis l’Antiquité (l’archéologue britannique Carter découvre des
textiles teints avec de la garance dans la tombe de Tout-ankh-Amon (1330
environ avant-J.C)).
Pendant des siècles on a produit des
vêtements teints avec le "Rouge de Turquie" comme colorant, tiré de
la racine de garance (Rubia tinctorum plante grimpante de la famille des rubiacées autrefois
cultivée dans le sud de la France pour en tirer cette substance colorante) et
dont le principal produit organique responsable de sa couleur est l'alizarine :
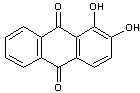
L'alizarine été isolée de la garance pour
la première fois, par Robiquet en 1826.
La synthèse de l'alizarine réalisée en
1868 par Graebe et Liebermann marqua la fin de la culture de la garance.
Le pigment utilisé en peinture aujourd'hui provient d'alizarine de synthèse.
Il a un pouvoir colorant élevé et s'utilise en glacis.
La laque alizarine correspond à ce colorant déposée sur de l'oxyde
d'aluminium (l'alumine) Al2O3.
Un des chemins de synthèse possibles de l'alizarine est :
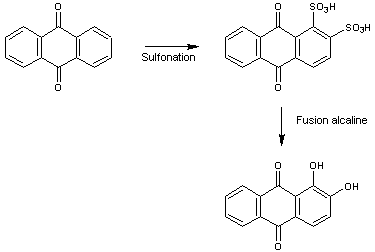
Rouge cochenille – Carmin NR 4
Teinture rouge extraite d'insecte dont le principe colorant
est l’acide carminique :
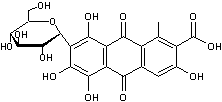
Elle est obtenue à partir d’extraits aqueux, alcoolo-aqueux
ou alcooliques de cochenille, la carapace séchée de l’insecte femelle Dactylopius
coccus Costa.
Dans les produits commercialisés le principe colorant est
associé à des ions ammonium, calcium, potassium ou sodium, seuls ou en
association ; ils peuvent également renfermer des matières protéiniques
provenant de l’insecte d’origine.
On estime que les laques aluminiques
formées à partir de l’acide carminique (les carmins) renferment de l’aluminium
et de l’acide carminique dans un rapport molaire de 1:2.
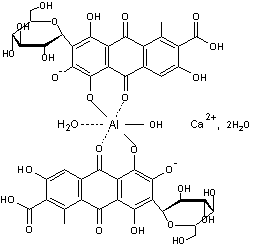
Le carmin de cochenille a été pendant longtemps
la seule matière organique permettant d'obtenir des nuances de rouges et de
roses dans les produits cosmétiques et en particulier dans les rouges à lèvres.
C'est aussi le colorant alimentaire E120.
Au Mexique les cochenilles colonisent
les raquettes d'un cactus le nopal (figuier de barbarie) ; il faut 70 000
insectes pour obtenir 500g de colorant.
Ce pigment a été utilisé en peinture dès le XVIème siècle.
Il donne un beau rouge profond, semi-opaque mais qui est
fragile et a tendance à brunir dans le temps.
Rouge lithol ou Rouge Tobias PR 49
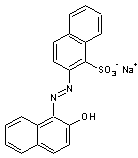
Colorant rouge vif de nuance différente selon le cation
associé ; il est peu stable à la lumière.
Rouge de quinacridone ou Red 122 (PR122)
Le nom est obtenu par contraction de quinoléine
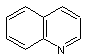
et d'acridone
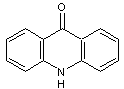
La quinacridone a pour formule
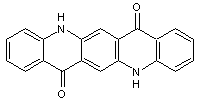
Le rouge de quinacridone correspond, lui, à la quinacridone
diméthylée :
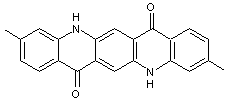
Ce pigment a été commercialisé dans les années 1950.
Il est d'un rouge pourpre transparent et est utilisé pour
réaliser des glacis.
Rouge thioindigo ou Red 88 (PR 88)
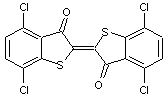
Couleur : rouge violet.
Rouge de pérylène ou Red 179 (PR179)
N,N',diméthyl-3,4,9,10-pérylènetétracarboxylique diimide
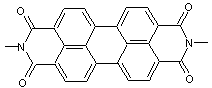
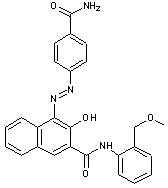
Rouge
de naphtol PR 170
Orangé de pyrrole PO 73
Pigment brillant, lumineux .
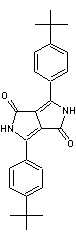
v
Violets
Violet de quinacridone ou Pigment violet 19 (PV
19)
Il correspond à la quinacridone :

C'est un pigment violet rouge brillant, transparent, peu
couvrant qui résiste parfaitement à la lumière.
Remarque :
Les pigments de quinacridone ont été identifiés dès 1896 ;
ils ont été synthétisés par H.Liebermann en 1935 et sont utilisés en peinture
depuis les années 1950-1960.
Violet de dioxazine ou Violet permanent PV 23
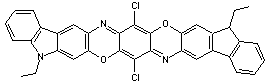
Couleur : violet rouge profond.
v
Bruns
Pigment
Brun 23 PBr 23
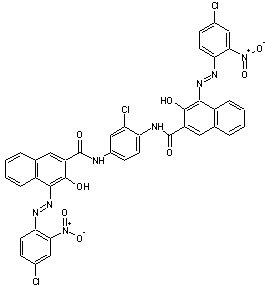
Pigment brun rouge un peu terne.
Pigment
Brun 25 PBr 25
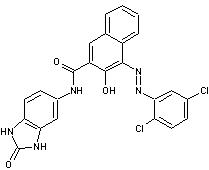
Couleur : Brun violet
rouge, profond.
v
Noirs
Noir d'aniline PBk 1
L'aniline
![]()
s'oxyde facilement ; avec la plupart des oxydants (mélange
sulfochromique, trioxyde de chrome, hypochlorites), on obtient des composés de
couleur rouge foncé. Avec le chlorate de potassium KClO3, on obtient
un colorant noir, le noir d'aniline :
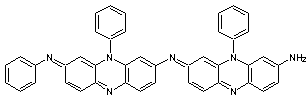
Couleur noire ; excellente résistance à la lumière.
Noir de pérylène PBk 31
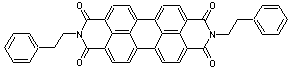
Couleur : noir intense, transparent ; pigment résistant à la
lumière.
Dégradation des pigments
- A la
lumière : les pigments particulièrement sensibles à la lumière et dégradés par
celle-ci, sont le rouge de cinabre, le jaune de chrome, le bleu de Prusse…..
- A
l'humidité : le vert émeraude……
- A la
chaleur : le blanc de plomb….
- Par les
éléments acides : blanc de plomb, le blanc de zinc, le jaune de cadmium, le
bleu d'Alexandrie, le bleu de céruléum, le vert d'émeraude et le vert d'oxyde
de chrome.
- Par les
éléments alcalins : le vert de gris, le bleu de Prusse.
- Par
l'ammoniaque : le rouge de cochenille, le rouge d'alizarine.
3-2) Les liants des peintures :
Pour fabriquer une peinture, un liant est indispensable car
les pigments en poudre ne peuvent être directement appliqués sur un support.
Le liant a deux fonctions :
- Liquide,
il permet le mouillage des pigments en
poudre et leur dispersion ; il maintient ensuite cette dispersion pendant un
temps qui permettra à l'artiste d'étaler la peinture sur la toile.
- Il permet
la fixation de la peinture sur la toile.
On a l'habitude de dire qu'il y a deux liants essentiels
dans une peinture d'art, l'eau et l'huile.
En fait l'eau et l'huile constituent le milieu général
correspondant à ces peintures, la fonction du liant étant assurée, notamment
dans le cas de l'eau, par d'autres substances : gomme arabique, polymère
acrylique, … comme nous allons le voir.
On distingue les gouaches, les aquarelles et les peintures
acryliques.
A) La gomme arabique :
S'utilise essentiellement pour les
gouaches et les aquarelles.
Le liant est ici l'ensemble eau + gomme
arabique à concentration élevée ; La gomme arabique facilitera la dispersion
des grains du pigment dans l'eau et maintiendra ces pigments en suspension.
Elle jouera le rôle de colle et fixera ces pigments sur le support.
La gomme arabique est un exsudat solidifié de la sève de l’Acacia
senegal une variété de mimosa que l'on trouve au Soudan, au Tchad, au
Niger, au Sénégal, au Mali et en Mauritanie.
Elle se présente sous forme d'une poudre jaune clair ou légèrement
ambrée, sans odeur, soluble dans l’eau et très peu soluble dans l’éthanol.
Elle est utilisée comme émulsifiant et comme support d’arômes dans
l’industrie agro-alimentaire sous le code E414.
C’est un polyholoside (ou polysaccharide) complexe de type
arabinogalactane à structure ramifiée ; il s'agit d'un polyanion généralement
associé à des ions calcium, magnésium ou potassium c'est-à-dire un sel d'acide polysaccharidique
; sa masse molaire est comprise entre 4,5.105 et 6.105
g.mol-1. La viscosité de ses solutions aqueuses est faible
comparativement à d'autres polyholosides de masse molaire similaire.
Les principaux éléments qui le constituent sont :
- l’acide
arabique,
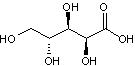
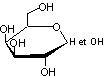
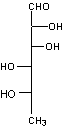
- le
D-galactose,
|
D-galactopyranose |
D(+)-galactose |
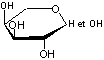
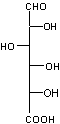
- le
L-arabinose,
|
L-arabinopyranose |
L-arabinose |
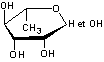
- le
L-Rhamnose,
|
L-(+) Rhamnose |
L-(+) Rhamnose |
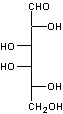
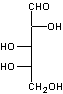
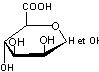
- l’acide
D-glucuronique.
|
Acide glucuronique |
Acide glucuronique |
La chaîne principale est constituée de D-galactopyranose (environ
45%) ; les chaînes latérales courtes, contiennent du D-galactose, du
L-arabinose, du L-rhamnose, et de l'acide D-glucuronique. Ce polyholoside est
souvent accompagné d'une partie protéique (de 0,1% à 10% selon les espèces
d'acacia) formée d'hydroxyproline, de sérine et de proline pour la moitié.
La gomme arabique possède des propriétés tensio-actives
intéressantes.
Comme tous les tensio-actifs, chaque molécule de gomme
arabique possède une partie hydrophile (celle qui va porter une charge ou être
polarisée) et une partie hydrophobe (celle qui ne porte pas de charge).
![]()
·
Elle
va jouer le rôle d'agent mouillant dans
le cas de pigments trop hydrophobes.
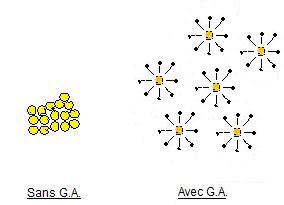
Dans l'eau, en effet, ceux-ci vont avoir tendance à
s'agglomérer.
En présence de gomme arabique le grain hydrophobe
(lipophile) de pigment se lie à la partie lipophile de la gomme et la partie
hydrophile de celle-ci va augmenter l'affinité pour l'eau du grain d'où une
meilleure mouillabilité c'est-à-dire une meilleure dispersion dans l'eau.
·
Elle
va jouer le rôle d'agent dispersant pour les
pigments trop hydrophiles qui lorsqu'on les met dans l'eau ont tendance à faire
des grumeaux.
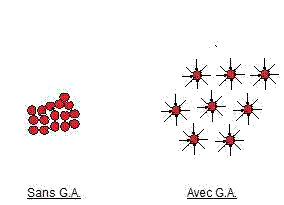
C'est la partie hydrophile de la gomme qui va se fixer au
grain et les parties hydrophobes qui sont à l'extérieur maintiennent les autres
grains à distance.
Remarques : - dans tous les cas, lorsqu'on incorpore les
pigments au liant, il faut mélanger soigneusement et longuement les
ingrédients, opération indispensable pour la dispersion des grains de pigment
dans le liant.
- souvent on ajoute un
autre agent mouillant ou dispersant en même temps que la gomme arabique, par
exemple du fiel de bœuf (voir annexe 4).
Séchage des peintures à l'eau et fixation sur le support (Aquarelles et gouaches) :
Une peinture à l'eau (additionnée de gomme arabique) a donc
comme liant la gomme arabique qui est un polymère comme on l'a indiqué.
Une fois que la peinture est appliquée sur un support l'eau
s'évapore et le polymère se rigidifie (la peinture durcit). En même temps, des
liaisons hydrogène s'établissent entre les éléments de la gomme arabique et des
éléments du support ; c'est le collage qui fixera la peinture durcie.
Les aquarelles et surtout les gouaches doivent être protégées
contre l'humidité en mettant par exemple une vitre de protection car les
processus de durcissement et de collage de la gomme arabique sont réversibles.
Remarque :
- La gomme
arabique n'est pas le seul liant pour fabriquer des gouaches ; on trouve
aussi la méthylcellulose :
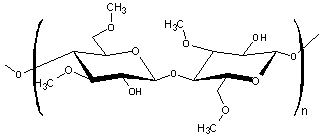
Il s'agit de cellulose :
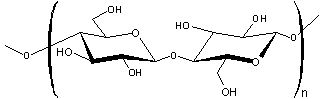
partiellement éthérifiée ; une partie des fonctions alcool
ont été méthylées.
- La gomme adragante est également un liant utilisé
parfois dans la fabrication des aquarelles.
C'est un exsudat obtenu à partir de la sève de plusieurs
espèces de plantes, du genre Astragalus que l'on trouve essentiellement
en Iran, en Turquie, en Syrie.
C'est un mélange de plusieurs polyholosides :
·
65%
environ de tragacanthine un polyholoside ramifié constitué d'unités
arabino-galactanes c'est-à-dire des chaînes de D-galactoses liés en β-1,4 et associées à des unités arabinofuranoses.
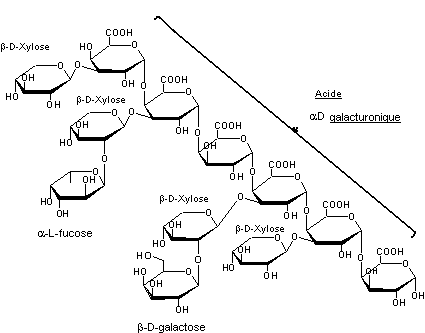
·
35%
environ de bassorine, un polymère formé par des chaînes d'acides
galacturoniques liés en α-1,4 et substituées par des résidus galactose, xylose et
fucose :
|
|
|
Bassorine |
La gomme adragante est l'additif alimentaire E 413.
B) Un polymère acrylique :
Ce sont les peintures acryliques.
Le liant est le mélange eau + résine acrylique soluble dans l'eau
ou en émulsion dans l'eau.
Une des résines acryliques possible, le poly(acide
acrylique).
L'acide acrylique
![]()
peut se polymériser à la lumière, par polymérisation
radicalaire en poly(acide acrylique)
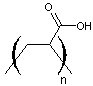
Cette résine est soluble dans l'eau grâce aux groupements
carboxyles qu'elle contient.
Mais on utilise pratiquement toujours des résines acryliques
thermoplastiques obtenues par polymérisation d'esters de l'acide acrylique, par
exemple de l'acrylate d'éthyle : poly(acrylate d'éthyle)
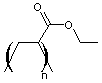
ou d'esters de l'acide méthacrylique par exemple le
méthacrylate de méthyle : poly(méthacrylate de méthyle)
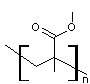
ou encore le poly(méthacrylate d'isobutyle)
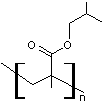
Ces polymères insolubles dans l'eau, constituent une phase
dispersée grâce à l'ajout d'émulsifiants amphiphiles
On peut donc fabriquer une peinture acrylique en mélangeant
pigment et charge (par exemple du carbonate de calcium CaCO3) dans
de l'eau avec un mouillant-dispersant pour éviter les grumeaux et ajouter la
résine acrylique en émulsion dans l'eau, le liant.
- On
mélange très soigneusement et longuement un pigment et un liant, de l'huile,
jusqu'à obtenir une pâte huileuse semblant homogène ; il s'agit en réalité
d'une suspension.
L'huile utilisée est en général de l'huile de lin.
Les huiles sont des triacylglycérides, plus fréquemment
appelés triglycérides. Les 3 groupes hydroxyles de la glycérine
(propane-1,2,3-triol) sont estérifiés par des acides gras.
Les principaux acides gras qui composent l'huile de lin sont
:
·
L'acide
linoléique entre 12 et 24%
![]()
·
L'acide
linolénique entre 40 et 70%
![]()
·
L'acide
oléique entre 12 et 25%
![]()
·
Des
acides gras saturés entre 5 et 12 %
Remarque :
On utilise aussi parfois de l'huile
de tung (encore appelée huile de bois de chine ou d'abrasin) provenant des
graines d'un arbre Aleurites moluccana .
Les principaux acides gras qui
composent cette huile :
·
L'acide
linoléique entre 8 et 10%
![]()
·
Les
acides éléostéariques entre 75 et 85%
α-éléostéarique
![]()
β-éléostéarique
![]()
·
L'acide
oléique entre 5 et 10%
![]()
·
Des
acides gras saturés entre 1 et 5%
- On peut
aussi s'il s'agit de pigments solubles dans l'eau, les dissoudre dans un peu
d'eau puis faire une émulsion par agitation dans de l'huile de lin en y
ajoutant un émulsifiant qui stabilisera cette émulsion ; certains peintres
utilisent la bile de bœuf (fiel de bœuf) comme émulsifiant (voir annexe 4).
"Séchage" des peintures à l'huile
Lorsqu' on abandonne une huile à l'air, il se forme parfois,
plus ou moins rapidement, un film correspondant à une réticulation de cette huile,
pellicule dure et imperméable. On appelle siccativité, l'aptitude d'une huile à
former ce film qui va rigidifier la surface ; on dit souvent, improprement, que
l'huile "sèche" ; ce terme qui fait penser à l'évaporation d'un
solvant ne convient donc pas.
Dans le cas d'une peinture à l'huile ce film va rendre
rigide la peinture, la durcir et permettre sa fixation sur le support.
Le mécanisme est assez complexe et fait intervenir le
dioxygène de l'air qui crée un radical –C* en "arrachant" un atome
d'hydrogène à un carbone en α d'une double
liaison C=C (carbone allylique) des chaînes d'acides gras des triacylglycérides
; par fixation d'une molécule d'oxygène sur ce radical on obtient un autre
radical -O-O* qui va se fixer sur le radical –C* d'une autre molécule d'huile
"activée". Des liens se créent ainsi entre les molécules et un film
solide naît de cette réticulation

Un pont oxygène s'est établi entre deux chaînes.
Plus une huile contient de doubles liaisons et plus dans un
temps donné il se forme de liaisons donc plus vite a lieu la réticulation c'est
à dire le "séchage".
Mais d'autres facteurs interviennent également, par exemple
le fait que les doubles liaisons sur la chaîne de l'acide gras sont ou non
conjuguées, ou bien l'existence de fonctions alcool dans la chaîne, ces
fonctions pouvant par déshydratation conduire à des liaisons doubles. Le temps
de siccativation varie de plusieurs heures à quelques jours suivant les huiles.
Comment mesurer la siccativité d'une huile ?
Une indication sur la siccativité d'une huile est donnée par
son indice d'iode, plus il est élevé et plus
l'huile contient de molécules insaturées (plus il y a de doubles liaisons C=C)
donc est susceptible de se réticuler à l'air. On parle d'huiles siccatives si
l'indice d'iode est supérieur à 150, semi-siccatives s'il est compris entre 110
et 150 et non siccatives si cet indice est inférieur à 110. L'huile de tung a
un indice d'iode moyen de 170 tandis qu'il est de 180 pour l'huile de lin ;
l'huile de carthame également utilisée dans la fabrication des peintures d'art
et qui contient environ 75% d'acide linoléique (diinsaturée) et environ 15%
d'acide oléique (monoinsaturée) a un indice d'iode moyen de 140, elle est donc
semi-siccative.
Principe du gras sur maigre :
On voit que l'oxygène est nécessaire pour que la
réticulation d'une huile ait lieu. Lorsque l'on dépose la première couche de
peinture sur le support, le durcissement de la peinture est progressif et l'air
peut pénétrer au travers du film en formation, permettant à la masse de se
rigidifier.
Si on ajoute une deuxième couche de peinture il faut veiller
à ce que celle-ci durcisse moins vite que la précédente, faute de quoi l'air ne
pourra plus la traverser et la première couche ne recevant plus d'oxygène ne
pourra se rigidifier totalement et restera pâteuse ; cela peut entraîner des
craquelures.
Il faut donc si l'on veut superposer des couches de peinture
à l'huile, commencer par mettre une première couche fine d'une peinture séchant
relativement rapidement (les peintres disent une peinture maigre) ; puis après
un temps de séchage mettre une couche de peinture avec davantage d'huile (les
peintres disent une peinture grasse) et ainsi de suite avec chaque fois une
peinture plus grasse que la précédente. Les peintres appellent cela le principe
"du gras sur maigre".
Utilisation d'un siccatif pour accélérer le
"séchage" de la peinture :
On peut pour accélérer la siccativation utiliser des
composés organiques solubles, par exemple des carboxylates de cobalt comme le
dodécanoate de cobalt (un sel de l'acide laurique donc) :
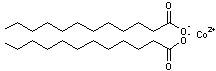
ces composés jouant
le rôle de catalyseur (on en ajoute très peu dans le liant).
Pour éviter qu'une
pellicule ne se forme sur la peinture quand on la met sur la palette, le
fabricant ajoute souvent un inhibiteur de siccativation
- des cétoximes :
![]()
comme par exemple
la méthyléthylcétoxime (ou butan-2-one oxime)
![]()
Les cétoximes
forment avec le siccatif des complexes réversibles inactifs. Volatiles, ces
cétoximes s'évaporent après application de la peinture et les siccatifs
retrouvent leur efficacité.
Les standolies :
Une autre façon de rendre une peinture à l'huile plus
siccative est de modifier l'huile avant de la mélanger à un pigment.
On peut en chauffant vers 280°C sous atmosphère inerte des
huiles végétales "crues" modifier leur consistance, leur viscosité et
même arriver à leur gélification ; Il s'agit d'une réaction d'oligomérisation
(polymérisation entre quelques unités monomères seulement) radicalaire, induite
par la chaleur et non par le dioxygène comme précédemment. Si l'huile contient des
doubles liaisons conjuguées, il peut également se former des dimères ou des
trimères par réaction de Diels-Alder.
Les huiles ainsi modifiées appelées "standolies" sont très utilisées
dans les secteurs des peintures, vernis et encres.
La standolisation, terme hollandais, augmente donc la
viscosité de ces huiles et leur vitesse de "séchage" en favorisant la
formation d'une pellicule protectrice très souple et imperméable. Le temps de
siccativation est diminué mais continue à se compter en heures.
Une théorie pour expliquer la formation de dimères :

Huile alkyde :
Pour diminuer le temps de siccativation d'une peinture à l'huile,
on peut procéder ainsi :
On estérifie la fonction alcool
secondaire du glycérol par un acide gras provenant d'une huile végétale et les
deux fonctions alcool primaire par de l'anhydride phtalique. La polymérisation
de cet ensemble conduit à ce qu'on appelle une résine alkyde très utilisée dans
l'industrie des peintures d'art ou des encres (à forte viscosité). Le séchage
plus ou moins rapide de ces encres étant assujetti à la nature plus ou moins
siccative de l'huile dont l'acide gras est issu.
Un exemple de résine alkyde formée à partir du glycérol, de l'anhydride phtalique et de l'acide linolénique
:
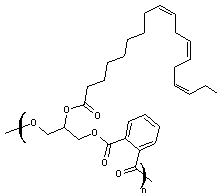
Au long des siècles et notamment à partir du XVème
les peintres ont cherché à améliorer les peintures qu'ils utilisaient, pour
faciliter leur travail : souplesse dans l'application de celles-ci sur la toile
et surtout séchage assez rapide de l'huile siccative, le liant dans lequel le
pigment était dispersé. Il était nécessaire qu'une couche soit sèche avant de
passer à la suivante …..Et cela pouvait durer des semaines, des mois, voire des
années, suivant l'huile utilisée. Celles-ci étaient notamment de l'huile de
lin, de noix, ou celle extraite du pavot (les graines de pavot pressées à froid
donnent une huile alimentaire claire appelée huile d'oeillette ; une seconde
pression à chaud donne une huile siccative utilisée en peinture).
Au XIXème siècle, aidés par des chimistes, des
artistes (le plus connu en la matière étant J.M.William Turner) ont mis au
point des gels qui, ajoutés aux peintures à l'huile, permettaient un séchage
beaucoup plus rapide.
Ces mélanges ont été appelés megilps et gumtions par les
utilisateurs.
Leur composition :
-
Le megilp :
On cuit l'huile siccative en présence d'un oxyde de plomb
orangé (la litharge PbO) jusqu'à ce que l'ensemble soit noir.
On mélange alors cette substance à une résine naturelle, la
résine mastic (voir annexe 1) (une résine qui suinte du
tronc et des branches principales du lentisque ou arbre à mastic (Pistacia
lentiscus) que l'on trouve dans les régions méditerranéennes et notamment
dans l'île grecque de Chio), on obtient un gel orangé foncé ; les peintres
l'utilisaient surtout avec les peintures sombres.
-
Le gumtion :
On utilise l'huile crue (non chauffée) avec de l'acétate de
plomb (Pb(CH3COO)2, 3H2O) et de la résine mastic ; le tout est broyé, mélangé. On
obtient un gel clair utilisé avec les peintures claires.
Ces techniques qui faisaient intervenir parfois de l'essence
de térébenthine ont été largement utilisées.
Un des inconvénients non identifié au moment de leur
découverte est le mauvais vieillissement des peintures sur les toiles qui
finissent (parfois en quelques années seulement) par se craqueler de façon
caractéristique (craquelures en écailles d'alligator).
Un deuxième inconvénient était la dangerosité (que l'on ne
connaissait pas à l'époque) du plomb utilisé ; il est vrai qu'ils l'utilisaient
déjà puisqu'il entrait dans la composition de certains pigments.
-
Tempera maigre :
Un jaune d'œuf (voir annexe 2) seul
ou mélangé à de l'eau joue le rôle de liant pour le pigment.
L'eau, l'huile et les pigments forment une émulsion et les
phospholipides et en particulier les phosphatidylcholines ou lécithines
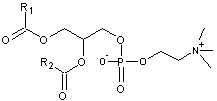
jouent le rôle d'émulsifiant (voir annexe
3).
C'est une technique des plus anciennes. Les tableaux qui ont
été ainsi peints se conservent très bien.
-
Tempera grasse :
On ajoute de l'huile au jaune d'œuf et à l'eau ; c'est en
quelque sorte une peinture à l'huile.
Elle n'a été utilisée qu'à partir des années 1620.
3-2-4) Un liant breveté :
Yves Klein (1928-1962) dépose en 1960 un brevet, pour une
peinture (IKB, International Klein Blue) obtenue à partir d'un pigment bleu
outremer et un liant qui fait l'objet du brevet ; le bleu Klein est devenu
mondialement célèbre.
Le liant dont il s'agit est fait d'une résine en poudre
appelée Rhodopas M, un poly(acétate de vinyle)
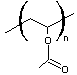
diluée dans de l'acétate d'éthyle et de l'éthanol ; on
l'appelle alors Rhodopas M60A (60% de résine).
Ce sont des substances permettant de modifier, souvent en
les améliorant, les qualités des peintures. Il en existe un très grand nombre
et il serait difficile de tout citer.
Un des rôles principaux d'une charge est d'épaissir la
peinture, lui donner du corps.
Les principales charges :
- le talc : c'est un silicate de magnésium, blanc, de
formule Mg3Si4O10(OH)2.
- le calcaire (ou la craie) : il s'agit de carbonate de
calcium (CaCO3).
- le plâtre composé de sulfate de calcium anhydre, CaSO4 ou
dihydraté CaSO4, 2H2O.
- le mica en poudre, silicates d'aluminium contenant souvent
du potassium.
- le kaolin, une argile blanche faite de silicate
d'aluminium Al2SiO5(OH)4
Une charge ne doit pas avoir un grand pouvoir couvrant pour
ne pas modifier la couleur apportée par le pigment.
Dans les pastels une charge est obligatoire ; dans les
autres peintures on incorpore souvent une charge pour en diminuer le prix.
Ils rendent le liant plus fluide pour une application plus
facile de la peinture.
- C'est
l'eau dans le cas des gouaches, des aquarelles, des peintures acryliques.
- Des essences dans le cas des
peintures à l'huile ; c'est souvent l'essence de térébenthine (voir annexe 1) qui a un bon pouvoir solvant.
On utilise aussi
parfois une "essence de pétrole" c'est-à-dire une essence provenant
de la distillation d'un pétrole ; il s'agit de la fraction recueillie entre 40°C
et 180°C composée d'un mélange d'hydrocarbures dont le nombre de carbones varie
entre 5 et 10, alcanes, cycloalcanes et arènes ayant un pouvoir solvant
variable en fonction de la teneur en arènes (benzène, xylènes…). Plus celle-ci
est élevée et plus le pouvoir solvant est grand, mais aussi leur nocivité.
Remarque :
On peut aussi
vouloir une dilution du pigment pour obtenir un effet. Ainsi lorsqu'on réalise
un glacis, une ou plusieurs couches de peinture transparente, constituée de
plus de liant que de pigment est déposée sur la toile de façon à former un
voile qui augmente l'effet de profondeur du motif ; ceci est valable pour les
peintures à l'huile mais aussi dans une moindre mesure pour les peintures à
l'eau (acrylique, aquarelle, a tempera).
On dilue souvent
la peinture à l'huile avec des huiles standolies qui vont donner une belle
brillance au tableau.
3-3-3)
Siccatifs ou retardateurs de séchage :
- Les siccatifs sont surtout
nécessaires pour les peintures à l'huile dont le séchage est lent. On a vu que
les sels organiques de cobalt pouvaient jouer ce rôle en catalysant la
siccativation des huiles ; c'est le cas par exemple du dodécanoate de cobalt :

D'autres
carboxylates de cobalt peuvent convenir comme par exemple l'octanoate de cobalt
:
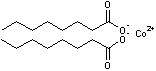
Ils sont moins
utilisés actuellement au profit de sels de lithium, strontium, zirconium ou
manganèse.
- Les retardateurs de séchage ne
sont utiles que pour les peintures acryliques qui sèchent très rapidement.
Le butylglycol ou
2-butoxyéthanol
![]()
par exemple, peu volatil,
peut être utilisé ; mais on utilise aussi le glycérol.
3-3-4) Des biocides
La conservation
des peintures à l'eau, nécessite l'incorporation de molécules biocides
permettant de les protéger de l'action des bactéries, des levures et des
champignons.
On citera parmi
les molécules actives, à large spectre, la 1,2-benzothiazolin-3-one
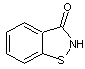
en solution dans
le dipropylène glycol et l'eau.
Dans les peintures
à l'huile, par exemple, lorsqu'on souhaite effectuer un glacis, on peut déposer
une ou plusieurs couches transparentes de peinture faite avec plus de liant que
de pigment ; au lieu d'utiliser l'huile seule pour augmenter la proportion de
liant par rapport de pigment, on peut utiliser un médium constitué d'huile de
lin cuite (c'est-à-dire chauffée entre 100 et 160°C pendant une heure ou deux)
mélangée à un baume de térébenthine contenant essentiellement colophane et
essence de térébenthine (voir annexe 1).
Il existe aussi
des médiums pour peintures à l'eau à base d'eau et de gomme arabique et pour
peintures acryliques à base d'eau et de résines acryliques.
D'une façon
générale, les médiums sont utilisés pour modifier la consistance de la
peinture.
On parlera ici de
vernis de finition destinés à protéger l'oeuvre des agressions extérieures (UV,
poussières,…).
En ce qui concerne
les peintures à l'eau (gouache, aquarelles) sensibles notamment à l'humidité,
la meilleure protection semble être une vitre.
Pour les
acryliques, il existe des vernis à base de résines acryliques en émulsion dans
l'eau, transparentes, mais cela n'est pas obligatoire cette peinture étant
moins sensible aux agressions que gouaches ou aquarelles.
C'est surtout pour
les peintures à l'huile que le vernis s'impose.
Les vernis pour
ces peintures sont faits à partir de résines naturelles (mastic,
dammar ou sandaraque) (voir annexe 1)
dissoutes dans des essences.
Remarque : Pour les peintures à l'huile, il existe aussi des vernis à
retoucher que l'on peut passer entre deux couches et qui sont destinés à
exalter les couleurs et à renforcer l'adhérence des différentes couches et que
l'on prépare en dissolvant de la colophane dans de
l'essence de térébenthine.
Ce sont des
enduits destinés à rendre plus lisses les supports destinés à recevoir de la
peinture.
- Autrefois ils étaient à base de
plâtre (sulfate de calcium) et de colle de peau (voir annexe
6) et n'étaient utilisés que pour les supports autres que les toiles (bois
en particulier).
- Aujourd'hui ce sont des enduits à
base de résines acryliques utilisables sur tous supports, quelle que soit la
technique (huile ou eau).
Résine mastic, résine
dammar, résine sandaraque, résine térébenthine
La plupart des exsudats végétaux appelés résines sont en
fait des oléo-gomme-résines, c'est-à-dire formés de 3 fractions qui peuvent
être séparées :
·
des
huiles essentielles (fraction oléo) qui sont des mono ou des sesquiterpènes
accompagnés d'une partie de polymères de monoterpènes. Les huiles essentielles
sont souvent volatiles et s'évaporent dès que l'exsudat est à l'air.
·
des
polysaccharides (fraction gomme).
Ces deux parties constituant la partie non résineuse de
l'exsudat.
·
une
partie résineuse, non-volatile formée d'acides diterpéniques ou triterpéniques
mélangés avec certains alcools, aldéhydes et esters.
Remarque : Parfois l'une
des fractions est soit absente soit présente en quantité très faible :
Si ce sont les huiles essentielles on dit qu'il s'agit d'une
gomme-résine.
Si ce sont les polysaccharides on dit qu'il s'agit d'une
oléo-résine.
Si c'est la résine on dit que c'est une oléo-gomme.
- Ainsi la résine
mastic, est une oléo-résine on trouve
·
des
huiles essentielles en petites quantités (environ 2%) avec comme molécule
majoritaire de l'α-pinène
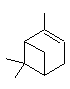
accompagnées d'un polymère, le cis-1,4-poly-β-myrcène
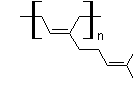
provenant d'un monoterpène le β-myrcène
![]()
·
on
y trouve aussi des triterpénoïdes tels que
l'acide moronique
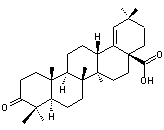
ou l'acide oléanonique
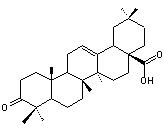
- La résine dammar peut être considérée comme une gomme
résine.
Il s'agit d'un exsudat des arbres de la famille des Dipterocarpaceae
dont Shorea et Hopea.
·
On
y trouve très peu d'huiles essentielles sans monoterpène et avec des
sesquiterpènes en faible quantité
|
α-gurjunène |
β-gurjunène |
accompagnées de polycadinène
·
une
partie saccharidique
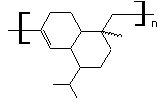
·
des
triterpénoides comme
l'acide oléanonique

ou l'acide ursonique
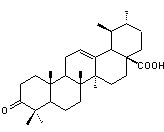
ou l'acide dammarénolique
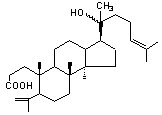
ou l'hydroxydammarénone
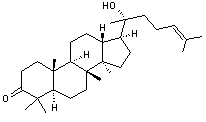
- La résine
sandaraque
Deux définitions pour cette résine qui a été utilisée du XIIème
au XVème siècle comme vernis alcoolique (dissoute dans de l'huile de lin et de
l'alcool) puis de nouveau au XVIIème siècle et au XVIIIème comme vernis maigre
:
- La sandaraque allemande issue du genévrier
(Juniperus)
- La sandaraque commune exsudée d'un conifère Tetraclinis
articulata
C'est
de cette dernière dont il va être question ici.
Elle
est constituée majoritairement de composés diterpéniques (20 carbones) ; des
molécules
|
De type abiétane
|
De
type pimarane
|
De
type labdane
|
- La résine térébenthine :
On dit
aussi baume ou plus simplement térébenthine.
La térébenthine (du latin terebinthina)
est le nom donné à certaines oléo-résines souples, semi-liquides extraites
de différents arbres :
Le
térébinthe (térébenthine de Chio (île grecque de la mer Egée)), qui est un
arbre des régions méditerranéennes (famille des térébinthacées, genre
pistachier).
Le
mélèze (térébenthine de Venise).
Le
sapin (térébenthine d'Alsace).
Le
pin maritime (térébenthine de Bordeaux).
La distillation des térébenthines fournit l'essence de
térébenthine, un liquide à odeur typique et un solide composé d'acides
résiniques.
La composition moyenne d'une résine térébenthine est
environ 15% de colophane, 55 à 60% d'autres acides résiniques et 20% d'essence.
- Colophane:
c'est de l'acide abiétique
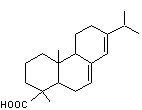
- D'autres
acides résiniques :
|
Acide
pimarique |
Acide
sandaracopimarique |
Acide
isopimarique |
|
Acide lévopimarique |
Acide palustrique |
Acide néoabiétique |
|
Acide déhydroabiétique |
|
|
La distillation des térébenthines, fournit l'essence de
térébenthine, dont les principaux constituants sont
l'α-pinène ou térébenthène.

ainsi que
l'α-terpinéol,
![]()
des
terpènes à odeur caractéristique.
Composition d'un jaune d'œuf :
49% d'eau
32% de lipides dont 65% de triglycérides et 35% de
phospholipides (il s'agit essentiellement des phosphoglycérolipides)
17% de protéines
1% de sels minéraux
1% de glucides
Définitions :
Une molécule de glycérol
![]()
peut être estérifiée par un ou plusieurs acides gras sur ses
trois fonctions alcool ; elle devient un lipide :
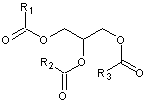
- Si elle
est estérifiée par un ou deux acides gras sur deux de ses fonctions alcool et
par l'acide phosphorique sur la troisième elle devient un acide
phosphatidique :
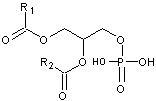
- Si un
acide phosphatidique a une deuxième fonction acide de l'acide phosphorique
estérifiée par :
·
la
choline :
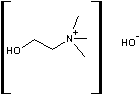
il devient une phosphatidylcholine (abrégée en PC)
que l'on appelle aussi lécithine.

Exemple :
La lécithine présente dans le jaune d'œuf ayant
- pour R1-COOH l'acide stéarique (un acide saturé) :
![]()
- pour R2-COOH l'acide oléique (un acide monoinsaturé) :
![]()
·
la
sérine :
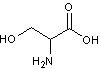
il devient une phosphatidylsérine (abrégée en PS)
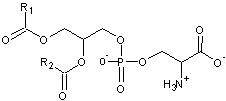
·
L'éthanolamine :
![]()
il devient une phosphatidyléthanolamine (abrégée en PE)
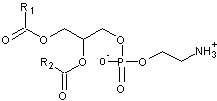
·
l'inositol :
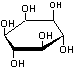
il devient un phosphatidylinositol (abrégée en PI)
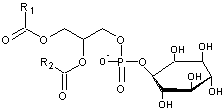
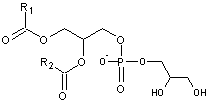
·
Le
glycérol :
![]()
il devient un phosphatidylglycérol (abrégée en PG)
La composition du jaune d'œuf en phospholipides
Phosphoglycérolipides
- 70%
environ de phosphatidylcholine
- 20%
environ de phosphatidyléthanolamine
- 0% de
phosphatidylinositol
- 1%
environ de phosphatidylsérine
- 0%
d'acide phosphatidique
Autres phospholipides
- 9% (dont
4% de sphingomyélines dans lesquelles le glycérol est remplacé par un alcool
complexe, la sphingosine)
Annexe 3
Emulsion – Emulsifiant
-
Emulsion :
Si l'on verse deux liquides non miscibles dans
un récipient, ils se superposent par ordre de densité, le plus dense en bas et
l'autre au dessus.
Exemple eau et huile

Si l'on agite vigoureusement cet ensemble une
émulsion va se former (gouttelettes d'huiles dans l'eau)

Si on laisse cette émulsion au repos, très
rapidement, les gouttes d'huile remontent à la surface, se rassemblent et
fusionnent ; c'est le phénomène de coalescence. La couche supérieure se
reconstitue ; l'émulsion n'est pas stable.
-
Emulsifiant :
Un émulsifiant stabilise une émulsion.
Les tensioactifs jouent souvent le rôle
d'émulsifiant.
Les tensioactifs (que l'on
appelle aussi agents de surface, le terme anglais étant surfactants) sont des
substances solubles dans l'eau et ayant la propriété de se concentrer, de
s'agréger aux interfaces entre l'eau et d'autres substances peu solubles dans
l'eau, les corps gras notamment.
Ces molécules présentent au moins deux
parties d'affinité différente, l'une est hydrophile (affinité pour l'eau) et
l'autre lipophile (affinité pour les graisses) ; de telles substances sont
dites amphiphiles (du grec amphi, “des deux cotés” et philos,
“ami”).
La partie hydrophile est une extrémité généralement ionique de la molécule
; elle peut être :
- anionique :
![]()
c'est le cas des ions carboxylates -COO-
mais aussi des ions sulfonates R( ou Ar)-SO3-.
- cationique :
![]()
c'est le cas des amines protonées,
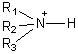
ou des ammoniums quaternaires
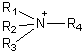 .
.
- zwittérionique :
![]()
bétaïnes,
phospholipides
(lécithines par exemple) : en milieu basique, ces molécules se comportent comme
des anions et en milieu acide comme des cations.
Parfois la partie hydrophile n'est pas
ionique
![]()
mais elle possède alors des groupes
polaires susceptibles de donner avec l'eau des liaisons hydrogène (des
fonctions alcool ou éther-oxyde par exemple) : R-O-(CH2CH2O)n-H.
La partie lipophile est généralement constituée d'une chaîne carbonée
assez longue et qui doit être linéaire (non ramifiée) pour être biodégradable.
Les tensio-actifs forment des micelles
c'est-à-dire qu'ils s'agrègent et par exemple dans l'eau on a :

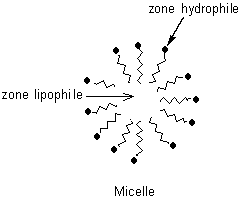
Comment un tensioactif stabilise-t-il une émulsion ?
Si on verse quelques gouttes de tensioactif
dans le récipient contenant l'émulsion eau-huile, les gouttelettes d'huile vont
se placer au centre de la zone lipophile des micelles. Elles restent séparées
et le phénomène de coalescence ne peut avoir lieu.

Annexe 4
Le fiel de bœuf comme émulsifiant
La
bile de bœuf et d'autres animaux contient des combinaisons de l'acide cholique,
un stéroïde
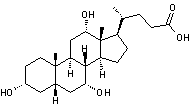
avec
des acides aminés comme
- la glycine
![]()
pour
donner l'acide glycocholique dont le sel de sodium est le glycocholate de
sodium
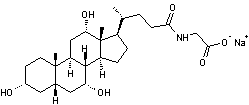
- la
taurine, un produit soufré
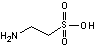
pour
donner l'acide taurocholique dont le sel de sodium est le taurocholate de
sodium
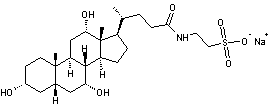
Ces produits biliaires ont des propriétés
tensio-actives. On les trouve dans le canal cholédoque . Ces substances sont
acheminées vers le duodénum où elles émulsionnent les graisses insolubles dans
l'eau en formant des micelles. Les molécules ainsi dispersées peuvent ensuite
être hydrolysées.
Cire
d'abeille – Cire de carnauba - Cires
minérales.
- Cire d'abeille :
La cire d'abeille est produite,
à partir des glandes cirières situées sur la face ventrale de l'abdomen des
ouvrières (la reine et les mâles n'en produisent pas), sous forme de fines
écailles transparentes blanches. Cette cire mélangée à de la salive est ensuite
malaxée par les mandibules, portée à une température d'environ 35°C et sert à
la construction de cellules (ou alvéoles) qui ont la forme de prismes droits à
base hexagonale de 5,4 mm de côté environ et 0,06 mm d'épaisseur pour Apis
mellifera, cette forme parfaitement hexagonale des alvéoles n'étant pas le
fait des abeilles ; elles construisent des cylindres, et les lois physiques qui
régissent le comportement de cylindres groupés, formés d'une substance solide
qui se ramollit à une certaine température (viscosité, tension superficielle …)
font le reste. C'est dans ces cellules que sera déposé le miel, une autre
couche de cire venant ensuite obturer les alvéoles.
C'est à partir du miel
et des sucres que l'abeille synthétise la cire et non à partir du pollen.
La cire d'abeille est
un solide initialement blanc mais qui se colore progressivement en brun sous
l'effet des pigments de plusieurs substances dont le pollen ; cette cire fond
vers 65°C et sa densité est 0,96 ; elle est insoluble dans l'eau, soluble dans
l'éthanol à chaud, le chloroforme et le benzène.
La cire d'abeille est
composée* :
- d'environ 71% d'esters dont 44% de
monoesters (d'acide gras et d'alcool gras), 12% d'hydroxyesters, 14% de di et
triesters et 1% d'esters de stérols.
- d'environ 15% d'hydrocarbures
linéaires à longue chaîne,
- d'environ 13% d'acides libres
- d'environ 1% d'alcools libres
* source "Manuel des corps gras",
technique et documentation Paris 1992, pages 297 et 306.
Pratiquement un quart
de la cire d'abeille est du palmitate de myricyle C15H31-COO-C30H61
et on trouve également une quantité de l'ordre de 12% de cérotate de myricyle C25H51-COO-C30H61.
Son indice d'acidité se
situe entre 15 et 23 ; son indice d'iode entre 6 et 12 ; son indice de
saponification entre 85 et 105 et son indice d'ester entre 70 et 82.
- Cire de carnauba :
Cette cire, dont le
code alimentaire est E903, dont la densité est 0,97 et qui est pratiquement
insoluble dans l'eau et dans l'éthanol, provient de Copernicia cerifera (nom commun
Copernicia prunifera) un palmier haut de 10 à 12m ; ses larges feuilles
vertes en éventail sont enduites de cette cire que l'on appelle aussi cire du
Brésil car ces arbres poussent bien dans le nord-est du pays. On en tire
environ 7 kg par palmier.
Elle représente
environ 60% des cires végétales utilisées dans l'industrie et provient
presqu'exclusivement du Brésil.
C'est un solide dur et
fragile présentant une cassure résineuse, de couleur brun clair à jaune pâle.
Dans le commerce elle se présente en poudre ou en paillettes
La cire de carnauba
résiste un peu mieux à la chaleur que la cire d'abeille ; elle fond vers 85°C.
Elle est formée* d'un mélange d'esters comprenant :
- des esters gras (acides gras en C24
à C28 estérifiant des alcools gras allant de C30 à C34).
- des esters formés à partir
d'acides β-hydroxylés (C22 à C28) et de diols (C24
à C34).
- des esters formés à partir d'acide
p.méthoxycinnamique et de diols (C24 à C34).
On trouve aussi mais
en minorité, des acides et des alcools libres ainsi que des hydrocarbures.
* source Les cires végétales : sources et applications (Jérôme Lecomte , CIRAD,
UMR IATE, Montpellier, F-34398 France)
Son indice d'acidité varie
de 2 à 7, il s'agit donc d'une cire peu acide ; son indice d'iode est de 10
donc peu d'insaturations ; son indice de saponification varie de 78 à 95.
- Cires minérales :
·
Lors de la distillation des pétroles bruts on obtient dans une zone de
température s'étalant entre 400°C et 500°C une coupe correspondant aux
paraffines, et aux cires.
Il s'agit
d'hydrocarbures saturés dont le nombre de carbones se situe entre 18 et 40
(voire même 50 ou 60).
Les cires ont des chaînes
longues et ramifiées ce qui leur confère une structure microcristalline. Il en
résulte une substance molle, blanche, non translucide dont la température de
fusion est supérieure à 70°C.
·
On trouve également des cires de structure semblable à
celles provenant des pétroles, dans les lignites (charbons à 75% environ de
carbone) ; on les appelle ozocérites.
·
Citons enfin les cires montaniques
qui sont des cires minérales provenant de végétaux fossilisés, que l'on
peut extraire des charbons et des lignites ; ce sont des esters de l'acide montanique
:
![]()
Acide montanique (C28H56O2)
et des alcools
suivants :
v Ethylène glycol
v Butan-1,3-diol
v Glycérol
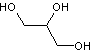
Les cires montaniques
sont très dures ; cette dureté est due à la grande concentration en acides gras
et en alcools libres et à la faible concentration en esters (ce sont ces esters
qui prédominent dans les cires molles).
Elles sont foncées et odorantes
lorsqu'on les extrait mais on peut les purifier pour les commercialiser.
Colle de peau
il
s'agit de gélatine préparée à partir de peaux de lapin, de vache ou de porc.
Une
gélatine est un mélange de protéines résultant de l'hydrolyse partielle du
collagène, une protéine structurale formée de trois chaînes α-polypeptidiques, chacune constituée d'environ
1000 acides aminés, ce réseau étant maintenu par des liaisons hydrogène
latérales induites en particulier par les hydroxylysines et les
hydroxyprolines.